Ingredientes ativos: Tobramicina
TOBRASTILL 0,3% colírio, solução
Por que é usado o Tobrastill? Para que serve?
Grupo Farmacoterapêutico
Antibiótico
Indicações terapêuticas
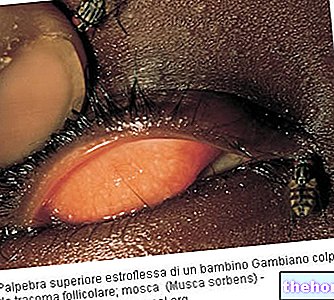
Tobrastill 0,3% colírio, solução é indicada no tratamento de infecções do olho e anexos oculares causadas por bactérias sensíveis à tobramicina: conjuntivite catarral aguda, subaguda e crônica; blefarite; ceratite bacteriana; dacriocistite; profilaxia pré e pós-operatória de intervenções no segmento anterior.
Contra-indicações Quando Tobrastill não deve ser usado
Hipersensibilidade à substância ativa ou a um dos componentes e a substâncias intimamente relacionadas do ponto de vista químico.
Precauções de uso O que você precisa saber antes de tomar Tobrastill
Como com todos os antibióticos, o uso prolongado pode promover o crescimento de microrganismos resistentes, incluindo fungos.Se a administração tópica de tobramicina for acompanhada por tratamento sistêmico com antibióticos aminoglicosídeos, a concentração sérica total deve ser monitorada cuidadosamente.
Interações Quais medicamentos ou alimentos podem alterar o efeito de Tobrastill
O componente tiloxapol é incompatível com a tetraciclina.
Avisos É importante saber que:
Gravidez e amamentação
Em mulheres grávidas e na primeira infância, o produto deve ser administrado em casos de real necessidade, sob supervisão direta do médico. O medicamento veterinário não deve ser utilizado durante a amamentação, caso o médico considere necessário o tratamento, a amamentação deve ser interrompida.
Dosagem e método de uso Como usar Tobrastill: Dosagem
Instilar no saco conjuntival duas gotas quatro vezes ao dia nas formas agudas e três vezes ao dia nas formas crônicas, de acordo com a prescrição médica.
Não exceda as doses ou o período de terapia recomendado pelo médico.
Overdose O que fazer se você tiver tomado muito Tobrastill
Não houve casos de overdose.
Efeitos colaterais Quais são os efeitos colaterais do Tobrastill
Tal como acontece com todos os antibióticos aminoglicosídeos oculares tópicos, podem ocorrer intolerância local ou reações de hipersensibilidade, como comichão, edema palpebral ou eritema conjuntival. Esses fenômenos foram detectados em menos de 3% dos pacientes tratados. O cumprimento das instruções fornecidas neste folheto reduz o risco de efeitos indesejáveis.
O paciente é convidado a relatar qualquer efeito indesejável não descrito no folheto informativo ao seu médico ou farmacêutico.
Expiração e retenção
Verifique a data de validade indicada na embalagem. O prazo de validade refere-se ao produto em embalagem intacta, corretamente armazenado.
Atenção: não use o medicamento após esta data.
Não armazene acima de 25 ° C.
O produto não deve ser usado além de 30 dias após a primeira abertura da embalagem.
Manter este medicamento fora do alcance das crianças.
Outra informação
Composição
100 ml de solução contêm:
- Ingrediente ativo: tobramicina 0,3g
- Excipientes: Tyloxapol, ácido bórico, sulfato de sódio anidro, cloreto de sódio, cloreto de benzalcônio, água purificada
Forma farmacêutica e conteúdo
Colírio, solução. Frasco de 5 ml com conta-gotas.
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
TOBRASTILL
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
100 ml de solução contêm: Princípio ativo: 0,3 g de tobramicina.
03.0 FORMA FARMACÊUTICA
Colírio, solução.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
A solução colírio de Tobrastill 0,3% é indicada no tratamento de infecções oculares e anexiais causadas por bactérias sensíveis à tobramicina: conjuntivite catarral aguda, subaguda e crônica; blefarite; ceratite bacteriana; dacriocistite; profilaxia pré e pós-operatória em intervenções no segmento anterior .
04.2 Posologia e método de administração
Instilar no saco conjuntival duas gotas quatro vezes ao dia nas formas agudas e três vezes ao dia nas formas crônicas, de acordo com a prescrição médica.
04.3 Contra-indicações
Hipersensibilidade a um dos componentes.
04.4 Advertências especiais e precauções adequadas de uso
Como com todos os antibióticos, o uso prolongado pode promover o crescimento de microrganismos resistentes, incluindo fungos. No caso de a administração tópica de tobramicina ser acompanhada por tratamento sistêmico com antibióticos aminoglicosídeos, a concentração sérica total deve ser cuidadosamente monitorada. Exceda as doses ou a terapia período recomendado pelo seu médico Mantenha o medicamento fora do alcance das crianças.
04.5 Interações com outros medicamentos e outras formas de interação
O componente tiloxapol é incompatível com a tetraciclina.
04.6 Gravidez e lactação
Estudos clínicos demonstraram que a tobramicina para uso oftálmico é segura e eficaz em uso pediátrico.Em mulheres grávidas e na infância o produto deve ser administrado em casos de real necessidade, sob a supervisão direta do médico. Ser administrado durante a amamentação. Se o médico considerar o tratamento necessário, a amamentação deve ser interrompida.
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
Eles não são conhecidos.
04.8 Efeitos indesejáveis
Tal como acontece com todos os antibióticos aminoglicosídeos oculares tópicos, podem ocorrer intolerância local ou reações de hipersensibilidade, como comichão, edema palpebral ou eritema conjuntival. Esses fenômenos foram detectados em menos de 3% dos pacientes tratados.
04.9 Overdose
Não há casos conhecidos de sobredosagem.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
A tobramicina é um antibiótico aminoglicosídeo isolado de um complexo produzido por Streptomices tenebrarius, ativo em uma ampla gama de patógenos oculares Gram-positivos e Gram-negativos, em particular em Staphylococcus aureus e Pseudomonas aeruginosa. O espectro antimicrobiano da tobramicina é comparável ao da gentamicina; no entanto, tem mostrado uma melhor atividade in vitro e in vivo, em particular contra Pseudomonas, e também tem um efeito nefro e ototóxico menor do que outros antibióticos aminoglicosídeos. Os estudos clínicos demonstraram que a solução colírio de Tobrastill a 0,3% é segura e eficaz em uso pediátrico.
05.2 Propriedades farmacocinéticas
Estudos sobre a penetração da tobramicina no nível ocular, após administração tópica em coelhos, mostraram que a concentração máxima de tobramicina na córnea é detectada 0,5 horas após a administração e 1,5 - 2 - 5 horas no humor aquoso.
05.3 Dados de segurança pré-clínica
O LD 50 da tobramicina administrada por via intravenosa em camundongos é de 118 mg / kg. Os estudos de toxicidade aguda, por administração tópica ocular em coelhos, demonstraram que a tobramicina não exerce efeitos irritantes locais. A administração ocular tópica repetida de tobramicina em coelhos durante três semanas não mostrou efeitos irritativos locais, bem como efeitos farmacotóxicos sistêmicos. Toxicidade embrio-fetal, carcinogênese e mutagênese: estudos realizados em ratos e coelhos com doses 33 vezes superiores à dose sistêmica humana normal demonstraram que este antibiótico não é mutagênico ou carcinogênico e não exerce efeitos tóxicos a nível embriofetal.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
Tyloxapol, ácido bórico, sulfato de sódio anidro, cloreto de sódio, cloreto de benzalcônio, água purificada.
06.2 Incompatibilidade
O componente tiloxapol é incompatível com a tetraciclina.
06.3 Período de validade
36 meses. O produto não deve ser usado mais de 30 dias após a primeira abertura da embalagem.
06.4 Precauções especiais para armazenamento
Não armazene acima de 25 ° C.
06.5 Natureza da embalagem primária e conteúdo da embalagem
Frasco de polietileno de baixa densidade branco com conta-gotas, selado com uma tampa de polipropileno.
06.6 Instruções de uso e manuseio
Sem instruções especiais.
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
BRUSCHETTINI S.r.l., Via Isonzo 6, Gênova (Itália).
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
A.I.C. n. 035703014.
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
Janeiro de 2004.
10.0 DATA DE REVISÃO DO TEXTO
Janeiro de 2004.