Veja também: pH da urina; PH vaginal.
O pH do sangue, e de qualquer outro fluido, reflete a concentração de íons de hidrogênio (H +) dissolvidos nele. Um valor de pH de 7 é neutro; os valores inferiores e superiores são respectivamente ácidos e básicos.

Ao aumentar a ventilação, ou seja, a frequência respiratória e / ou a profundidade da respiração, o corpo aumenta a quantidade de dióxido de carbono excretado, elevando o pH do sangue. Inversamente, no caso oposto (ocorre hipoventilação como resultado da alcalose sangüínea) .
No rim, existe outro mecanismo compensatório muito importante do pH do sangue, mesmo que seja muito mais lento para entrar em movimento. As células dos néfrons podem de fato responder à acidose reabsorvendo maiores quantidades de bicarbonatos, secretando maiores quantidades de íons hidrogênio, reabsorvendo mais tampões (HCO3-) e promovendo a gênese da amônia (que tem a capacidade de reagir com os íons H + livres , formando o íon amônio: NH3 + H + <→ NH4 +).
- A HOMEOSTASE DO pH SANGUÍNEO DEPENDE DOS SISTEMAS DE TAMPÃO, DO PULMÃO E DO RIM
A acidose e a alcalose podem ter "origem respiratória ou metabólica. No primeiro caso, são devidas a um excesso ou defeito de dióxido de carbono, enquanto no segundo estão associadas a um déficit ou excesso de substâncias metabólicas não voláteis, portanto não elimináveis. com a respiração.
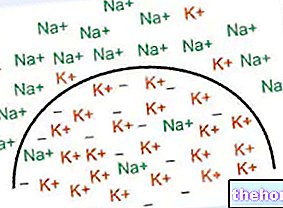
Observação: o dióxido de carbono em si não é ácido, porque não contém nenhum átomo de hidrogênio. No entanto, no ambiente sanguíneo, ele se combina com a água para formar ácido carbônico, que se dissocia em H + e HCO3-; pela lei de ação de massa, se a concentração de dióxido de carbono aumenta (veja a figura em vermelho), o sangue ambiente torna-se acidificado. Na condição oposta (cor verde), a situação se inverte.



- Acidose láctica (devido a hipóxia ou hipoperfusão, comum em exercícios físicos);
- Cetoacidose (produção maciça de corpos cetônicos típica de diabetes), cetose (produção importante de corpos cetônicos típica de jejum particularmente prolongado ou desnutrição grave);
- Falência renal;
- Envenenamento;
- Diarréia severa;
- Hipoventilação (causada por drogas, drogas, doenças particularmente graves, DPOC e em uma forma leve também típica de indivíduos gravemente obesos).
- Ele vomitou;
- Consumo excessivo de agentes alcalinizantes ou drogas (como bicarbonato de sódio)
- Hiperventilação (incluindo aquela induzida por drogas ou por respiração artificial ou drogas).









.jpg)