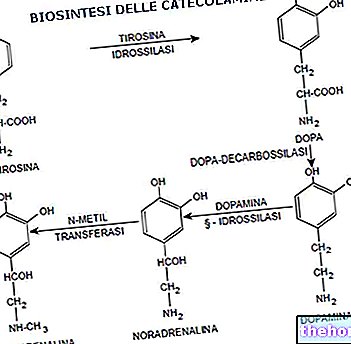
Definição
Enzimas são proteínas produzidas em células vegetais e animais, que agem como catalisadores, acelerando reações biológicas sem serem modificadas.
As enzimas funcionam combinando-se com uma substância específica para transformá-la em uma substância diferente; exemplos clássicos são dados por enzimas digestivas presentes na saliva, estômago, pâncreas e intestino delgado, que desempenham uma função essencial na digestão e ajudam a quebrar os alimentos em constituintes básicos, que podem então ser absorvidos e usados pelo corpo, processados por outras enzimas ou excretado como resíduo.
Cada enzima tem uma função específica: aquela que decompõe as gorduras, por exemplo, não atua sobre proteínas ou carboidratos. As enzimas são essenciais para o bem-estar do organismo. A deficiência, mesmo de uma única enzima, pode causar distúrbios graves. Um exemplo bem conhecido é a fenilcetonúria (PKU), doença caracterizada pela incapacidade de metabolizar um aminoácido essencial, fenilalanina, cujo acúmulo pode causar deformidades físicas e doenças mentais.
Estudo bioquímico
As enzimas são proteínas particulares que têm a característica de serem catalisadores biológicos, ou seja, têm a capacidade de quebrar a energia de ativação (Eatt) de uma reação, modificando seu caminho para que um processo cineticamente lento seja mais rápido.
As enzimas aumentam a cinética das reações termodinamicamente possíveis e, ao contrário dos catalisadores, são mais ou menos específicas: portanto, possuem especificidade de substrato.
A enzima não está envolvida na estequiometria da reação: para que isso aconteça, o sítio catalítico final deve ser idêntico ao inicial.
Na ação catalítica quase sempre há uma fase lenta que determina a velocidade do processo.
Quando falamos de enzimas, não é correto falar de reações de equilíbrio, falamos, em vez disso, de curso estável (estado em que determinado metabólito é formado e consumido continuamente, mantendo sua concentração quase constante ao longo do tempo). O produto de uma reação catalisada por uma enzima é geralmente ele próprio um reagente para uma reação subsequente, catalisado por outra enzima e assim por diante.
Os processos catalisados por enzimas geralmente consistem em sequências de reações.
Uma reação genérica catalisada por uma enzima (E) pode ser resumida da seguinte forma:

E é a enzima
S é o substrato;
ES representa o aduto entre a enzima e o substrato;
P é o produto;
K é a constante de velocidade da reação.
Uma enzima genérica (E) se combina com o substrato (S) para formar o aduto (ES) com uma constante de taxa K1; ela pode se dissociar de volta em E + S, com uma constante de taxa K2, ou (se "viver" por tempo suficiente ) pode prosseguir para formar P com uma constante de velocidade K3.
O produto (P) pode, por sua vez, recombinar-se com a enzima e reformar o aduto com a constante de velocidade K4.
Quando a enzima e o substrato são misturados, há uma fração de tempo em que o encontro entre as duas espécies ainda não ocorreu: ou seja, há um intervalo de tempo extremamente curto (que depende da reação) em que a enzima e o substrato têm ainda não encontrado; após esse período, enzima e substrato entram em contato em quantidades crescentes e o aduto ES é formado. Posteriormente, a enzima atua sobre o substrato e o produto é liberado. Pode-se então dizer que c "é um intervalo de tempo inicial em que a concentração do aduto ES não pode ser definida; após esse período, assume-se que um estado estacionário é estabelecida, ou seja, a velocidade dos processos que levam à obtenção do aduto é igual à velocidade dos processos que levam à destruição do aduto.
A constante de Michaelis-Menten (KM) é uma constante de equilíbrio (referida ao primeiro equilíbrio descrito acima); pode-se dizer, com uma boa aproximação (porque K3 também deve ser considerado), que KM é representado pela razão entre as constantes cinéticas K2 e K1 (referido à destruição e formação do aduto ES no primeiro equilíbrio descrito acima) .
Através da constante de Michaelis-Menten temos uma "indicação da afinidade entre a enzima e o substrato: se o KM for pequeno c" é uma "alta afinidade entre a enzima e o substrato, então o aduto ES é estável.
As enzimas estão sujeitas a regulação (ou modulação).
No passado se falava principalmente em modulação negativa, ou seja, inibição das capacidades catalíticas de uma enzima, mas também pode haver uma modulação positiva, ou seja, existem espécies capazes de potencializar as capacidades catalíticas de uma enzima.
Existem 4 tipos de inibições (obtidas a partir de aproximações feitas em um modelo para combinar dados experimentais com equações matemáticas):
- inibição competitiva
- inibição não competitiva
- inibição incompetitiva
- inibição competitiva
Falamos de inibição competitiva quando uma molécula (inibidor) é capaz de competir com o substrato. Para semelhança estrutural, o inibidor pode reagir no lugar do substrato; daí a terminologia "inibição competitiva" .A probabilidade de a enzima se ligar ao inibidor ou substrato depende da concentração de ambos e de sua afinidade com a enzima; a taxa de reação, portanto, depende desses fatores.
Para obter a mesma taxa de reação sem a presença do inibidor, é necessário ter uma concentração de substrato maior.
É demonstrado experimentalmente que, na presença de um inibidor, a constante de Michaelis-Menten aumenta.
Já no que se refere à "inibição não competitiva, a interação entre a molécula que deveria funcionar como moduladora (inibidora positiva ou negativa) e a" enzima, ocorre em um local diferente daquele em que ocorre a interação ocorre entre a enzima e o substrato; portanto, falamos de modulação alostérica (do grego allosteros → outro site).
Se o inibidor se ligar à enzima, pode induzir uma alteração na estrutura da enzima e, consequentemente, pode diminuir a eficiência com que o substrato se liga à enzima.
Nesse tipo de processo, a constante de Michaelis-Menten permanece constante, pois esse valor depende do equilíbrio entre a enzima e o substrato e, mesmo na presença de um inibidor, esse equilíbrio não se altera.
O fenômeno da inibição incompetitiva é raro; um inibidor incompetitivo típico é uma substância que se liga reversivelmente ao aduto ES, dando origem a ESI:

A inibição do excesso de substrato às vezes pode ser incompetitiva, pois isso ocorre quando uma segunda molécula de substrato se liga ao complexo ES, dando origem ao complexo ESS.
Um inibidor competitivo, por outro lado, só pode se ligar ao substrato enzima aduto como no caso anterior: a ligação do substrato à enzima livre induz uma modificação conformacional que torna o local acessível para o inibidor.
A constante de Michaelis Menten diminui à medida que a concentração do inibidor aumenta: aparentemente, portanto, a afinidade da enzima pelo substrato aumenta.
Serina protease
Eles são uma família de enzimas à qual pertencem a quimiotripsina e a tripsina.
A quimotripsina é uma enzima proteolítica e hidrolítica que corta à direita dos aminoácidos hidrofóbicos e aromáticos.
O produto do gene que codifica a quimiotripsina não está ativo (é ativado com um comando); a forma inativa da quimiotripsina é representada por uma cadeia polipeptídica de 245 aminoácidos. A quimiotripsina tem uma forma globular devido a cinco pontes dissulfeto e outras interações menores (eletrostática, forças de Van der Waals, ligações de hidrogênio, etc.).
A quimiotripsina é produzida pelas células quimiose do pâncreas, onde é contida em membranas especiais e expelida através do ducto pancreático para o intestino, no momento da digestão dos alimentos: a quimiotripsina é de fato uma enzima digestiva. As proteínas e nutrientes que ingerimos através da dieta são submetidos à digestão para serem reduzidos a cadeias menores e para serem absorvidos e transformados em energia (por exemplo, amilases e proteases quebram nutrientes em glicose e aminoácidos que chegam às células, através dos vasos sanguíneos chegam à veia porta e daí são transportados para o fígado, onde são submetidos a tratamento adicional).
As enzimas são produzidas de forma inativa e são ativadas apenas quando chegam ao "local onde devem operar"; uma vez que sua ação é concluída, eles são desativados. Uma enzima, uma vez desativada, não pode ser reativada: para ter uma "ação catalítica adicional, ela deve ser substituída por" outra molécula de enzima. Se a quimitripsina fosse produzida na forma ativa já no pâncreas, ela atacaria este último: pancreatite são patologias devido a enzimas digestivas que já estão ativadas no pâncreas (e não nos locais necessários); algumas delas se não tratadas a tempo, levar à morte.
Na quimiotripsina e em todas as serina proteases, a ação catalítica se deve à existência do ânion álcool (-CH2O-) na cadeia lateral de uma serina.
As serina proteases levam esse nome precisamente porque sua ação catalítica é devida a uma serina.
Uma vez que toda a enzima tenha realizado sua ação, antes de poder voltar a operar no substrato novamente, ela deve ser restaurada com água; a "liberação" da serina pela água é a etapa mais lenta do processo, e é nesta fase que determina a velocidade da catálise.
A ação catalítica ocorre em duas fases:
- formação do ânion com propriedades catalíticas (anion alcoolato) e subsequente ataque nucleofílico ao carbono carbonílico (C = O) com clivagem da ligação peptídica e formação do éster;
- ataque da água com restauração do catalisador (capaz de exercer novamente sua ação catalítica).
As várias enzimas pertencentes à família da serina protease podem ser constituídas por diferentes aminoácidos, mas, para todas elas, o sítio catalítico é representado pelo ânion alcoólico da cadeia lateral de uma serina.
Uma subfamília de serina proteases é a das enzimas envolvidas na coagulação (que consiste na transformação da proteína, de sua forma inativa em uma "outra forma ativa). Essas enzimas garantem que a coagulação seja tão eficaz quanto possível e limitada em o espaço e o tempo (a coagulação deve ocorrer rapidamente e deve ocorrer apenas nas proximidades da área lesada). As enzimas envolvidas na coagulação são ativadas em cascata (a partir da ativação de uma única enzima, bilhões de enzimas são obtidos: cada enzima ativada , por sua vez ativa muitas outras enzimas).
A trombose é uma patologia decorrente do mau funcionamento das enzimas da coagulação: é causada pela ativação, sem necessidade (porque não há lesão), das enzimas utilizadas na coagulação.
Existem enzimas moduladoras (reguladoras) e enzimas inibitórias para outras enzimas: interagindo com as últimas, regulam ou inibem sua atividade; até mesmo o produto de uma enzima pode ser um inibidor da enzima.Também existem enzimas que funcionam quanto mais, maior é o substrato presente.
Lisozima
Luigi Pasteur descobriu, espirrando em uma placa de Petri, que no muco existe uma enzima capaz de matar bactérias: lisozima; do grego: liso = que tamanho; zimo = enzima.
A lisozima é capaz de quebrar a parede celular das bactérias. As bactérias e os organismos unicelulares em geral precisam de estruturas mecanicamente resistentes que limitem sua forma; dentro das bactérias há uma pressão osmótica muito alta, de modo que atraem água. A membrana plasmática explodiria se não houvesse parede celular que se opusesse à entrada de água e limitasse o volume da bactéria.
A parede celular consiste em uma cadeia polissacarídica na qual as moléculas de N-acetil-glucosamina (NAG) e as moléculas de ácido N-acetil-murâmico (NAM) se alternam; a ligação entre NAG e NAM é quebrada por hidrólise. O grupo carboxila do NAM, na parede celular, está envolvido em uma ligação peptídica com um aminoácido.
Entre as várias cadeias, formam-se pontes constituídas por ligações pseudo-peptídicas: a ramificação deve-se à molécula de lisina; a estrutura como um todo é muito ramificada e isso lhe confere uma grande estabilidade.
A lisozima é um antibiótico (mata as bactérias): age fazendo uma rachadura na parede bacteriana; quando essa estrutura (que é mecanicamente resistente) se quebra, a bactéria puxa água até estourar. A lisozima consegue quebrar a ligação β-1,4 glucosídica entre NAM e NAG.
O sítio catalítico da lisozima é representado por uma ranhura que corre ao longo da enzima na qual a cadeia de polissacarídeo está inserida: seis anéis glucosídicos da cadeia são colocados na ranhura.
Na posição três da ranhura c "está um estrangulamento: nesta posição apenas um NAG pode ser colocado, porque o NAM, que é de dimensões superiores, não pode entrar. O sítio catalítico real está entre as posições quatro e cinco: uma vez que existe um NAG na posição três, o corte ocorrerá entre um NAM e um NAG (e não vice-versa), o corte, portanto, é específico.
O pH ideal para a lisozima funcionar é cinco. No sítio catalítico da enzima, isto é, entre as posições quatro e cinco, estão as cadeias laterais de um ácido aspártico e de um ácido glutâmico.
Grau de homologia: mede o parentesco (ou seja, similaridade) entre as estruturas da proteína.
Existe uma forte relação entre a lisozima e a lactose-sintase.
A lactose sintetase sintetiza a lactose (que é o principal açúcar do leite): a lactose é um galactosil glicosídeo em que c "é uma ligação β-1,4 glucosídica entre a galactose e a glicose.
Portanto, a lactose sintetase catalisa a reação oposta àquela catalisada pela lisozima (que, em vez disso, divide a ligação β-1,4 glucosídica)
A lactose sintetase é um dímero, ou seja, é composta por duas cadeias de proteínas, uma das quais possui propriedades catalíticas e é comparável à lisozima e a outra é uma subunidade reguladora.
Durante a gravidez, as glicoproteínas são sintetizadas pelas células da glândula mamária pela ação da galatosil-tranferase (tem uma "homologia de sequência de 40% com a lisozima): esta enzima é capaz de transferir um grupo galactosil de uma estrutura de alta energia para uma estrutura glicoproteica. Durante a gravidez, a expressão do gene que codifica para a galactosisil-transferase é induzida (há também a expressão de outros genes que também dão outros produtos): há um aumento no tamanho da mama porque ela é ativada a glândula mamária (anteriormente inativa) que deve produzir leite Durante o parto, a α-lactalbumina é produzida, que é uma proteína reguladora: é capaz de regular a capacidade catalítica da galactosil-transferase (por discriminação do substrato). Galactosil-transferase modificada por α-lactalalbumina é capaz de transferir um galactosil para uma molécula de glicose: formando uma ligação glicosídica β-1,4 e dando lactose (lactose sintetase).
Conseqüentemente, a galactose transferase prepara a glândula mamária antes do parto e produz leite após o parto.
Para produzir glicoproteínas, a galactosil transferase liga-se a um galactosil e a um NAG; durante o parto, a albumina lactal liga-se à galactosiltransferase, fazendo com que esta reconheça a glicose e não mais NAG para dar lactose.