Ingredientes ativos: ésteres etílicos de ácidos graxos poliinsaturados
ESKIM 500 mg cápsulas moles
ESKIM 1000 mg cápsulas moles
Por que o Eskim é usado? Para que serve?
Grupo Farmacoterapêutico
Substâncias hipolipemiantes - substâncias hipocolesterolêmicas e hipotiglicerídeos - Triglicerídeos ômega-3.
Indicações terapêuticas
Hipertrigliceridemia
Redução dos níveis elevados de triglicéridos quando a resposta às dietas e outras medidas não farmacológicas por si só se revelou insuficiente (o tratamento deve ser sempre associado a uma dieta adequada).
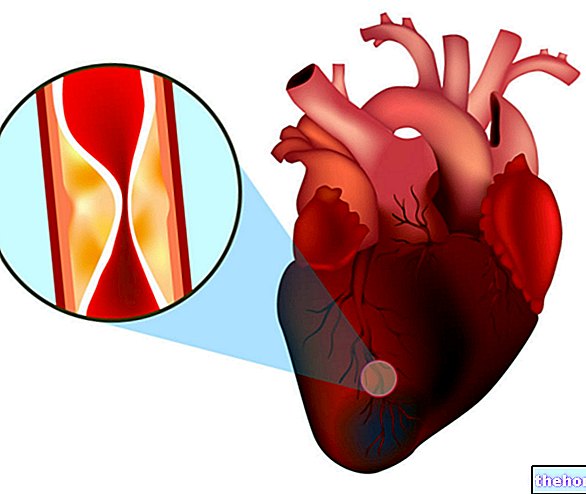
Prevenção secundária em paciente com infarto do miocárdio prévio
Em pacientes com infarto do miocárdio prévio, em combinação com outras medidas terapêuticas quando apropriado, é indicado para reduzir o risco de mortalidade.
Contra-indicações Quando Eskim não deve ser usado
Hipersensibilidade à substância ativa ou a qualquer um dos excipientes.
Geralmente contra-indicado na gravidez e lactação (ver “Advertências especiais”).
Precauções de uso O que você precisa saber antes de tomar Eskim
Como precaução, recomenda-se vigilância especial para indivíduos com diátese hemorrágica e tratamento com anticoagulantes, nos quais pode ocorrer um aumento alterado no tempo de sangramento.
Interações Quais drogas ou alimentos podem modificar o efeito de Eskim
O uso concomitante do medicamento com anticoagulantes pode resultar em um aumento modesto no tempo de sangramento.
Avisos É importante saber que:
A segurança do uso na gravidez e lactação não foi estabelecida.
Dose, método e tempo de administração Como usar o Eskim: Posologia
Hipertrigliceridemia
1 cápsula de 1000 mg 1-3 vezes ao dia s.p.m.
Cápsulas de 500 mg podem ser usadas para ajuste da dose e terapia de manutenção.
Prevenção secundária em paciente com infarto do miocárdio prévio
1 cápsula de 1000 mg por dia.
Efeitos colaterais Quais são os efeitos colaterais do Eskim
Foram observadas manifestações leves e transitórias de náusea e diarreia.
O paciente é convidado a relatar qualquer efeito indesejável não descrito no folheto informativo ao seu médico ou farmacêutico.
Expiração e retenção
Verifique a data de validade indicada na embalagem.
O prazo de validade refere-se ao produto em embalagem intacta, corretamente armazenado. Atenção: não use o medicamento após esta data.
MANTENHA O MEDICAMENTO FORA DO ALCANCE E DA VISTA DAS CRIANÇAS
Composição
Cada capsula contém:
Cápsulas de 500 mg
Princípio ativo: ésteres etílicos de ácidos graxos poliinsaturados 500 mg com um teor de EPA e DHA não inferior a 85% e em uma proporção de 0,9 - 1,5 entre si.
Cápsulas de 1000 mg
Princípio ativo: ésteres etílicos de ácidos graxos poliinsaturados 1000 mg com um teor de EPA e DHA não inferior a 85% e em uma proporção de 0,9-1,5 entre si.
Excipientes: D, La-tocoferol, succinato de gelatina, glicerol, etil p-oxibenzoato de sódio, propil p-oxibenzoato de sódio.
Forma farmacêutica e conteúdo
Caixa de 30 cápsulas moles de 500 mg
Caixa de 20 cápsulas moles de 1000 mg
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
ESKIM
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Cada capsula contém:
Cápsulas de 500 mg
Princípio ativo:
Ésteres etílicos de ácidos graxos poliinsaturados 500 mg com um teor de EPA e DHA não inferior a 85% e em uma proporção de 0,9-1,5 entre si
Cápsulas de 1000 mg
Princípio ativo:
Ésteres etílicos de ácidos graxos poliinsaturados 1000 mg com um teor de EPA e DHA não inferior a 85% e em uma proporção de 0,9-1,5 entre si
03.0 FORMA FARMACÊUTICA
Cápsulas moles.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
Hipertrigliceridemia
Redução dos níveis elevados de triglicérides quando a resposta às dietas e outras medidas não farmacológicas por si só se mostrar insuficiente (o tratamento deve ser sempre associado a um regime alimentar adequado).
Prevenção secundária em paciente com infarto do miocárdio prévio
Em pacientes com infarto do miocárdio prévio, em combinação com outras medidas terapêuticas quando apropriado, é indicado para reduzir o risco de mortalidade.
04.2 Posologia e método de administração
Hipertigliceridemia
1 cápsula de 1000 mg 1-3 vezes ao dia s.p.m.
Cápsulas de 500 mg podem ser usadas para ajuste da dose e terapia de manutenção.
Prevenção secundária em paciente com infarto do miocárdio prévio
1 cápsula de 1000 mg por dia.
04.3 Contra-indicações
Hipersensibilidade à substância ativa ou a qualquer um dos excipientes.
Geralmente contra-indicado durante a gravidez e lactação (ver pág. 4.6)
04.4 Advertências especiais e precauções adequadas de uso
Como precaução, recomenda-se vigilância especial para indivíduos com diátese hemorrágica e tratamento com anticoagulantes, nos quais pode ocorrer um aumento alterado no tempo de sangramento.
04.5 Interações com outros medicamentos e outras formas de interação
O uso concomitante do medicamento com anticoagulantes pode resultar em um aumento modesto no tempo de sangramento.
04.6 Gravidez e lactação
A segurança do uso na gravidez e lactação não foi estabelecida.
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
ESKIM não afeta a capacidade de conduzir ou utilizar máquinas.
04.8 Efeitos indesejáveis
Foram observadas manifestações leves e transitórias de náusea e diarreia.
04.9 Overdose
Nenhum caso de sobredosagem foi relatado.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
Grupo farmacoterapêutico: Substâncias hipolipemiantes - Hipocolesterolêmicos e hipotigliceridêmicos - Triglicerídeos ômega-3.
Código ATC: C10AX06.
Uma vez incorporado aos fosfolipídios da membrana, o EPA fornecido diretamente com a droga ou formado a partir do DHA compete com o ácido araquidônico como substrato para vários processos enzimáticos em plaquetas, endotélio e leucócitos, resultando em maior relaxamento endotelial, redução da agregabilidade plaquetária e redução da quimiotática e pró-inflamatória potencial, mostrando assim um efeito antiaterosclerótico e antitrombótico.
O EPA e o DHA, como outros ácidos n-3 poliinsaturados, apresentam, mesmo em doses baixas, uma ação antiarrítmica, provavelmente por um efeito estabilizador direto sobre os cardiomiócitos. A redução significativa na mortalidade total e cardiovascular, especialmente mortes súbitas, observada em um grande estudo prospectivo de prevenção secundária em pacientes com infarto do miocárdio prévio, está ligada à sua ação antiarrítmica.
Os efeitos cardiovasculares favoráveis do EPA e do DHA também incluem a redução dos níveis plasmáticos de triglicerídeos, VLDL e fibrinogênio e o aumento da deformabilidade eritrocitária com conseqüente redução da viscosidade sanguínea.
05.2 Propriedades farmacocinéticas
A absorção, a excreção, a distribuição das proteínas nos tecidos e no plasma foram estudadas usando o produto marcado em ratos e cães.
Mais de 95% da radioatividade é absorvida pelo canal alimentar e uma quantidade modesta, como material solúvel em água, é excretada na urina. Após 24 horas da administração, cerca de 35% da radioatividade encontra-se nos tecidos e, em particular, nos tecidos envolvidos no metabolismo dos lípidos.
O tempo de pico plasmático foi de 3,40 e 6,75 horas em ratos e cães, respectivamente.
As frações do plasma com os níveis mais altos de radioatividade foram VLDL e quilomícrons.
Estudos clínicos farmacocinéticos confirmaram que os ésteres etílicos de EPA e DHA são hidrolisados e incorporados nas várias frações lipídicas, proporcionando, após administração repetida, concentrações de EPA e DHA da mesma ordem que as obtidas pela administração de triglicerídeos naturais.
05.3 Dados de segurança pré-clínica
Os estudos toxicológicos realizados no produto com tratamentos agudos e crônicos excluíram fenômenos tóxicos, mesmo após a administração de altas doses.
Não foram observados efeitos teratogênicos e gerais na função reprodutiva durante os estudos de reprodução. Estudos conduzidos em ratos por 24 meses não revelaram a presença de potencial carcinogênico.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
D, L a-tocoferol; gel de succinato; glicerol; p-oxibenzoato de sódio de etil; propil p-oxibenzoato de sódio.
06.2 Incompatibilidade
Não é relevante.
06.3 Período de validade
36 meses.
06.4 Precauções especiais de armazenamento
Não há precauções especiais.
06.5 Natureza da embalagem primária e conteúdo da embalagem
ESKIM 500 mg cápsulas moles
30 cápsulas de 500 mg em blister de alumínio e PVC / PVDC acoplado
ESKIM 1000 mg cápsulas moles
20 cápsulas de 1000 mg em blister de alumínio e PVC / PVDC acoplado
06.6 Instruções de uso e manuseio
Sem instruções especiais.
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
Sigma-Tau Industrie Farmaceutiche Riunite S.p.A.
Viale Shakespeare, 47
00144 Roma
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
ESKIM 500 mg cápsulas moles
30 cápsulas moles de 500 mg AIC n. 027618038
ESKIM 1000 mg cápsulas moles
20 cápsulas moles de 1000 mg AIC n. 027618040
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
Autorização:12/09/91
Renovação: 01/06/2000
10.0 DATA DE REVISÃO DO TEXTO
Setembro de 2001