Ingredientes ativos: Trastuzumab
Herceptin 150 mg pó para concentrado para solução para perfusão
As bulas de Herceptin estão disponíveis para os tamanhos de embalagem:- Herceptin 150 mg pó para concentrado para solução para perfusão
- Solução injetável de Herceptin 600 mg em frasco
- Solução injetável de Herceptin 600 mg via dispositivo de administração
Por que o Herceptin é usado? Para que serve?
O Herceptin contém a substância ativa trastuzumab, que é um anticorpo monoclonal. Os anticorpos monoclonais ligam-se a proteínas ou antígenos específicos. O trastuzumabe foi projetado para se ligar seletivamente a um antígeno denominado receptor 2 do fator de crescimento epidérmico humano (HER2). O HER2 está presente em grandes quantidades na superfície de algumas células cancerosas, estimulando seu crescimento. Quando o Herceptin se liga ao HER2, ele interrompe o crescimento dessas células e faz com que elas morram.
O seu médico pode prescrever Herceptin para o tratamento do câncer de mama e estômago se:
- Você tem câncer de mama em estágio inicial com altos níveis de uma proteína chamada HER2.
- Você tem câncer de mama metastático (câncer de mama que se espalhou para longe do câncer primário) com níveis elevados de HER2. Herceptin pode ser prescrito em combinação com os medicamentos de quimioterapia paclitaxel ou docetaxel como o primeiro tratamento para o cancro da mama metastático ou pode ser prescrito sozinho quando outros tratamentos se revelaram ineficazes. Também é usado em combinação com medicamentos chamados inibidores da aromatase para tratar pacientes com níveis elevados de HER2 e câncer de mama metastático positivo para receptores hormonais (câncer que é sensível à presença de hormônios sexuais femininos).
- Você tem câncer gástrico metastático com altos níveis de HER2, em combinação com os outros medicamentos anticâncer capecitabina ou 5-fluorouracil e cisplatina.
Contra-indicações Quando Herceptin não deve ser usado
Não use Herceptin se:
- você é alérgico ao trastuzumabe, às proteínas murinas (de camundongo) ou a qualquer um dos outros ingredientes.
- tem problemas respiratórios graves em repouso devido ao câncer ou se precisar de tratamento com oxigênio.
Precauções de uso O que você precisa saber antes de tomar Herceptin
O seu médico supervisionará de perto a sua terapia.
Verificações cardíacas
O tratamento com Herceptin administrado isoladamente ou com um taxano pode afetar o seu coração, especialmente se já tiver tomado uma "antraciclina (taxanos e antraciclinas são dois outros tipos de medicamentos usados para tratar o câncer). Portanto, sua função cardíaca será avaliada primeiro., Durante (a cada três meses) e após (até dois a cinco anos) tratamento com Herceptin. Se tiver sinais de insuficiência cardíaca (ou seja, o coração não bombeia o sangue corretamente), pode ser necessário interromper o tratamento com Herceptin.
Fale com o seu médico, farmacêutico ou enfermeiro antes de tomar Herceptin se:
- teve insuficiência cardíaca, doença da artéria coronária, doença das válvulas cardíacas (sopros no coração), hipertensão, tomou ou está tomando algum medicamento para tratar a hipertensão.
- tomou ou está a tomar um medicamento denominado doxorrubicina ou epirrubicina (medicamentos utilizados para tratar o cancro). Estes medicamentos (ou qualquer outra antraciclina) podem danificar o músculo cardíaco e aumentar o risco de problemas cardíacos ao tomar Herceptin.
- você sofre de falta de ar, principalmente se estiver tomando taxano. Herceptin pode causar dificuldade em respirar, especialmente na primeira vez que é administrado. Isso pode ser mais sério se você já estiver sofrendo de falta de ar. Muito raramente, os doentes com dificuldades respiratórias graves antes do tratamento morreram quando receberam Herceptin.
- já recebeu outros tratamentos de câncer.
Se está a receber tratamento com Herceptin em associação com outros medicamentos usados para tratar o cancro, como paclitaxel, docetaxel, um inibidor da aromatase, capecitabina, 5-fluorouracilo ou cisplatina, deve também ler o folheto informativo destes medicamentos.
Crianças e adolescentes
Herceptin não é recomendado para menores de 18 anos.
Interações Quais medicamentos ou alimentos podem alterar o efeito de Herceptin
Informe o seu médico, farmacêutico ou enfermeiro se estiver a tomar ou tiver tomado recentemente ou se vier a tomar outros medicamentos.
Pode levar até 7 meses para que o Herceptin seja eliminado do corpo. Portanto, deve informar o seu médico, farmacêutico ou enfermeiro que tomou Herceptin se iniciar novos medicamentos nos 7 meses seguintes à interrupção do tratamento.
Avisos É importante saber que:
Gravidez
- Se está grávida, pensa estar grávida ou planeia engravidar, informe o seu médico, farmacêutico ou enfermeiro antes de tomar este medicamento.
- Deve utilizar métodos contracetivos eficazes durante o tratamento com Herceptin e pelo menos 7 meses após a interrupção do tratamento.
- O seu médico irá discutir consigo os riscos e benefícios de tomar Herceptin durante a gravidez.Em casos raros, foi observada uma diminuição do líquido (amniótico) à volta do bebé em desenvolvimento no útero em mulheres grávidas tratadas com Herceptin. Essa condição pode ser prejudicial ao bebê no útero e tem sido associada à maturação pulmonar incompleta, que resultou na morte do feto.
Hora da alimentação
Não amamente enquanto estiver a tomar Herceptin e nos 7 meses após a última dose de Herceptin, uma vez que Herceptin pode passar para o bebé através do leite materno Consulte o seu médico ou farmacêutico antes de tomar qualquer medicamento.
Condução e utilização de máquinas
Não se sabe se Herceptin afetará a sua capacidade de conduzir ou utilizar máquinas. No entanto, se sentir sintomas como calafrios ou febre, não deve dirigir ou operar máquinas até que esses sintomas desapareçam.
Dosagem e método de uso Como usar Herceptin: Dosagem
Antes de iniciar o tratamento, seu médico determinará a quantidade de HER2 em seu tumor. Apenas os pacientes com níveis elevados de HER2 serão tratados com Herceptin. Herceptin só deve ser administrado por um médico ou enfermeiro. O seu médico irá prescrever a dose e esquema de tratamento adequados para si. A dose de Herceptin depende do seu peso corporal.
Existem dois tipos diferentes (formulações) de Herceptin:
- um é administrado por infusão em uma veia (infusão intravenosa)
- o outro é administrado por injeção sob a pele (injeção subcutânea).
É importante verificar o rótulo do produto para garantir que está a ser administrada a formulação correta prescrita pelo seu médico.A formulação intravenosa de Herceptin não se destina a administração subcutânea e só deve ser administrada por injeção intravenosa.
A formulação intravenosa de Herceptin é administrada como uma "infusão intravenosa (" gotejamento ") diretamente nas suas veias. A primeira dose do seu tratamento é administrada durante um período de 90 minutos e será observado por um profissional de saúde durante a administração, caso desenvolva algum efeito secundário. Se a primeira dose for bem tolerada, as doses subsequentes podem ser administradas ao longo de um período de 30 minutos (ver secção 2 “Advertências e precauções”). O número de perfusões que receberá dependerá da sua resposta ao tratamento. O seu médico irá discuta isso com ela.
Em pacientes com câncer de mama em estágio inicial, câncer de mama metastático e câncer gástrico metastático, Herceptin é administrado a cada 3 semanas. Herceptin também pode ser administrado uma vez por semana para o tratamento do cancro da mama metastático.
Para evitar erros de medicação, é importante verificar os rótulos dos frascos para garantir que o medicamento a ser preparado e administrado é Herceptin (trastuzumab) e não trastuzumab emtansina.
Sobredosagem O que fazer se você tiver tomado muito Herceptin
Não existem efeitos conhecidos que possam ser atribuídos à sobredosagem com Herceptin.
Se você parar de usar Herceptin
Não pare de tomar este medicamento sem primeiro falar com o seu médico. Todas as doses devem ser tomadas no momento certo todas as semanas ou a cada três semanas (dependendo do seu esquema de dosagem). Isso ajuda o medicamento a funcionar da melhor forma.
Pode levar até 7 meses para que o Herceptin seja eliminado do corpo. Portanto, o seu médico pode decidir continuar a monitorar a função cardíaca mesmo após terminar o tratamento.
Caso ainda tenha dúvidas sobre a utilização deste medicamento, fale com o seu médico, farmacêutico ou enfermeiro
Efeitos colaterais Quais são os efeitos colaterais do Herceptin
Como todos os medicamentos, Herceptin pode causar efeitos secundários, embora nem todas as pessoas os tenham. Alguns desses efeitos colaterais podem ser graves e exigir hospitalização.
Reações como calafrios, febre e outros sintomas semelhantes aos da gripe podem ocorrer durante a infusão de Herceptin. Esses efeitos são muito comuns (podem afetar mais de 1 em 10 pessoas). Outros sintomas relacionados à infusão são: náuseas, vômitos, dor, aumento muscular tensão e tremores, dor de cabeça, tontura, dificuldade em respirar, respiração ruidosa, pressão alta ou baixa, distúrbios do ritmo cardíaco (palpitações, batimento cardíaco rápido ou irregular), inchaço da face ou lábios, erupção cutânea e sensação de cansaço. Alguns desses sintomas podem ser graves e alguns pacientes morreram (ver seção 2 "Advertências e precauções").
Estes efeitos ocorrem principalmente com a primeira perfusão intravenosa (“gota a gota” na veia) e durante as primeiras horas após o início da perfusão. Eles geralmente são temporários. Você será monitorado por um profissional de saúde durante a infusão e por pelo menos seis horas após o início da primeira infusão e por duas horas após o início das outras infusões. Se tiver uma reação, a infusão será retardada ou interrompida e você poderá receber um tratamento para neutralizar os efeitos indesejáveis. A infusão pode ser continuada após a melhora dos sintomas.
Ocasionalmente, os sintomas começam mais de seis horas após o início da infusão. Se isso acontecer com você, entre em contato com seu médico imediatamente. Às vezes, os sintomas podem melhorar e piorar mais tarde.
Podem ocorrer outros efeitos secundários em qualquer altura durante o tratamento com Herceptin, não apenas em associação com uma perfusão. Por vezes, podem ocorrer problemas cardíacos durante o tratamento e ocasionalmente após o fim do tratamento e podem ser graves. Incluem enfraquecimento do sangue. Músculo cardíaco que pode levar a insuficiência cardíaca, inflamação (inchaço, vermelhidão, calor e dor) do revestimento do coração e distúrbios do ritmo cardíaco. Isso pode levar a sintomas como:
- falta de ar (mesmo à noite),
- tosse,
- retenção de líquidos (inchaço) nas pernas ou braços,
- palpitações (batimento cardíaco rápido ou irregular).
O seu médico irá monitorizar o seu coração regularmente durante o tratamento, mas deve informá-lo imediatamente se notar algum dos sintomas acima.
Se sentir algum dos sintomas anteriores quando terminar o tratamento com Herceptin, deve consultar o seu médico e informá-lo sobre o seu tratamento anterior com Herceptin.
Efeitos colaterais muito comuns de Herceptin (podem afetar mais de 1 em 10 pessoas):
- infecções
- diarréia
- constipação
- queimaduras no peito (dispepsia)
- fraqueza
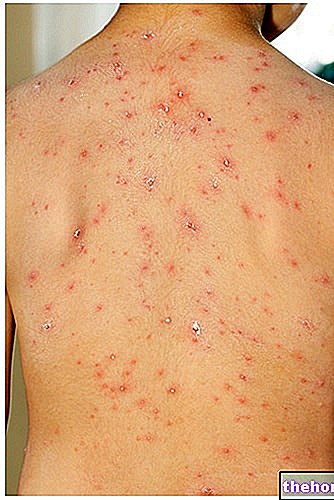
- erupção cutânea
- dor no peito
- dor abdominal
- dor nas articulações
- contagens baixas de glóbulos vermelhos e glóbulos brancos (que ajudam a combater infecções), às vezes associadas à febre
- dor muscular
- conjuntivite
- rasgo excessivo
- sangramento nasal
- um nariz escorrendo
- perda de cabelo
- tremor
- ondas de calor
- tontura
- problemas de unhas
- perda de peso
- perda de apetite
- incapacidade de dormir (insônia)
- Gosto alterado
- Baixa contagem de plaquetas
- Dormência ou formigamento dos dedos das mãos e dos pés
- Vermelhidão, inchaço ou bolhas na boca e / ou garganta
- Dor, inchaço, vermelhidão ou dormência nas mãos e / ou pés
Efeitos colaterais comuns de Herceptin (podem afetar até 1 em 10 pessoas):
- Reações alérgicas
- boca e pele secas
- infecções de garganta
- olhos secos
- infecções da bexiga e da pele
- suando
- Cobreiro
- fadiga e mal-estar
- inflamação dos seios da face
- estava ansioso
- inflamação do pâncreas ou fígado
- depressão
- distúrbios renais
- mudanças no pensamento
- aumento do tônus ou tensão muscular (hipertonia)
- asma
- dor nos braços e / ou pernas
- doenças pulmonares
- erupção cutânea com coceira
- dor nas costas
- sonolência
- dor de pescoço
- contusões
- dor no osso
- hemorróidas
- acne
- coceira
- cãibras nas pernas
Os efeitos secundários pouco frequentes de Herceptin podem afetar até 1 em 100 pessoas:
- surdez
- erupção cutânea com pápulas
Efeitos colaterais raros de Herceptin: podem afetar até 1 em 1000 pessoas:
- fraqueza
- icterícia
- inflamação / cicatrizes dos pulmões
Outros efeitos colaterais que foram relatados com o uso de Herceptin: a frequência não pode ser estimada a partir dos dados disponíveis:
- anormalidades ou alterações na coagulação do sangue
- reações anafiláticas
- altos níveis de potássio
- inchaço do cérebro
- inchaço ou sangramento atrás dos olhos
- inchaço da membrana do coração
- ritmo cardíaco lento
- choque
- ritmo cardíaco anormal
- dificuldade respiratória
- Parada respiratória
- acúmulo agudo de fluido nos pulmões
- estreitamento agudo das vias aéreas
- redução anormal dos níveis de oxigênio no sangue
- inchaço da garganta
- dificuldade em respirar ao deitar
- dano / insuficiência hepática
- inchaço da face, lábios e garganta
- insuficiência renal redução anormal dos níveis de fluidos ao redor do bebê no útero
- falha de desenvolvimento pulmonar no útero
- desenvolvimento anormal de rim no útero
Alguns dos efeitos colaterais que ocorrem podem ser causados pelo câncer de mama. Se receber Herceptin em combinação com quimioterapia, alguns destes efeitos secundários também podem ser devidos à quimioterapia.
Se tiver algum dos efeitos secundários, informe o seu médico, farmacêutico ou enfermeiro.
Relatório de efeitos colaterais
Se tiver quaisquer efeitos secundários, fale com o seu médico, farmacêutico ou enfermeiro. Isto inclui quaisquer efeitos secundários possíveis não listados neste folheto. Também pode comunicar os efeitos secundários diretamente através do sistema nacional de notificação listado no Apêndice V. efeitos secundários pode ajudar fornecer mais informações sobre a segurança deste medicamento.
Expiração e retenção
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após o prazo de validade impresso na embalagem exterior e no rótulo do frasco, após VAL. O prazo de validade corresponde ao último dia desse mês.
Conservar no frigorífico (2 ° C - 8 ° C).
As soluções de infusão devem ser usadas imediatamente após a diluição. Não utilize Herceptin se notar quaisquer partículas ou alterações de cor antes da administração.
Os medicamentos não devem ser eliminados na canalização ou no lixo doméstico. Pergunte ao seu farmacêutico como deitar fora os medicamentos que já não utiliza. Isto ajudará a proteger o ambiente.
Composição e forma farmacêutica
O que Herceptin contém
- A substância ativa é o trastuzumab. Cada frasco para injetáveis contém 150 mg de trastuzumab que deve ser dissolvido em 7,2 ml de água para preparações injetáveis.A solução resultante contém aproximadamente 21 mg / ml de trastuzumab.
- Os outros componentes são cloridrato de L-histidina, L-histidina, α di-hidratado, α-trealose, polissorbato 20.
Qual a aparência de Herceptin e conteúdo da embalagem
Herceptin é um pó para concentrado para solução para perfusão fornecido em frasco para injectáveis de vidro selado com rolha de borracha que contém 150 mg de trastuzumab. O pó é um grânulo liofilizado branco a amarelo claro. Cada embalagem contém 1 frasco para injetáveis de pó.
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
HERCEPTIN 150 MG PÓ PARA CONCENTRADO PARA SOLUÇÃO PARA INFUSÃO
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Um frasco contém 150 mg de trastuzumab, anticorpo monoclonal IgG1 humanizado, produzido por cultura de células de mamíferos (células de ovário de hamster chinês) em suspensão, purificado por cromatografia de afinidade e troca iônica, com procedimentos específicos de inativação e remoção viral.
A solução reconstituída de Herceptin contém 21 mg / ml de trastuzumab.
Para a lista completa de excipientes (ver seção 6.1).
03.0 FORMA FARMACÊUTICA
Pó para concentrado para solução para perfusão.
Pó liofilizado branco a amarelo claro.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
Câncer de mama
Câncer de mama metastático
Herceptin é indicado para o tratamento de pacientes adultos com câncer de mama metastático HER2 positivo (MBC):
• como monoterapia para o tratamento de pacientes que receberam pelo menos dois regimes de quimioterapia para doença metastática. A quimioterapia administrada anteriormente deve conter pelo menos uma antraciclina e um taxano, a menos que o paciente não seja adequado para tais tratamentos. Pacientes com receptor hormonal positivo também devem ter falhado em responder à terapia hormonal, a menos que o paciente seja inadequado para tais tratamentos.
• em combinação com paclitaxel para o tratamento de pacientes que não receberam quimioterapia para a sua doença metastática e para os quais o tratamento com antraciclinas não está indicado.
• em combinação com docetaxel para o tratamento de pacientes que não receberam quimioterapia para sua doença metastática.
• em combinação com um inibidor da aromatase no tratamento de pacientes pós-menopáusicas com MBC positivo para receptores hormonais não previamente tratados com trastuzumab.
Câncer de mama em estágio inicial
Herceptin é indicado para o tratamento de pacientes adultos com câncer de mama precoce HER2 positivo (EBC):
• após cirurgia, quimioterapia (neoadjuvante ou adjuvante) e radioterapia (se aplicável) (ver seção 5.1)
• após quimioterapia adjuvante com doxorrubicina e ciclofosfamida, em combinação com paclitaxel ou docetaxel.
• em combinação com quimioterapia adjuvante com docetaxel e carboplatina.
• em combinação com quimioterapia neoadjuvante, seguida de terapia adjuvante com Herceptin, na doença localmente avançada (incluindo forma inflamatória) ou em tumores> 2 cm de diâmetro (ver secções 4.4 e 5.1).
Herceptin só deve ser utilizado em doentes com cancro da mama metastático ou em estádio inicial cujos tumores exibam sobreexpressão de HER2 ou amplificação do gene HER2, conforme determinado por um teste acurado e validado (ver secções 4.4 e 5.1).
Câncer gástrico metastático
Herceptin em combinação com capecitabina ou 5-fluorouracil e cisplatina é indicado para o tratamento de pacientes adultos com adenocarcinoma metastático do estômago ou junção gastroesofágica HER2 positivo que não tenham recebido tratamento anticâncer para doença metastática.
Herceptin só deve ser administrado a doentes com cancro gástrico metastático (MGC) cujos tumores tenham sobreexpressão de HER2, definida como um resultado IHC2 + e confirmado por um resultado SISH ou FISH, ou definido como um resultado IHC3 +. Devem ser usados métodos de determinação precisos e validados (ver seções 4.4 e 5.1).
04.2 Posologia e método de administração
A medição da expressão de HER2 é obrigatória antes do início da terapêutica (ver secções 4.4 e 5.1). O tratamento com Herceptin só deve ser iniciado por um médico com experiência na administração de quimioterapia citotóxica (ver secção 4.4) e só deve ser administrado por um profissional de saúde .
É importante verificar a rotulagem do medicamento para garantir que a formulação correta (dose fixa intravenosa ou subcutânea) está sendo administrada ao paciente conforme prescrito. A formulação intravenosa de Herceptin não se destina à administração subcutânea e só deve ser administrada por infusão intravenosa.
A mudança do tratamento com a formulação intravenosa de Herceptin para o tratamento com a forma subcutânea de Herceptin e vice-versa, administrado de três em três semanas (q3w), foi investigada no estudo MO22982 (ver secção 4.8).
Para evitar erros de medicação, é importante verificar os rótulos dos frascos para garantir que o medicamento que está a preparar e administrar é Herceptin (trastuzumab) e não Kadcyla (trastuzumab emtansina).
Dosagem
Câncer de mama metastático
Administração a cada três semanas
A dose de carga inicial recomendada é de 8 mg / kg de peso corporal. A dose de manutenção recomendada em intervalos de três semanas é de 6 mg / kg de peso corporal, começando três semanas após a dose de carga.
Administração semanal
A dose de carga inicial recomendada de Herceptin é de 4 mg / kg de peso corporal. A dose de manutenção semanal recomendada de Herceptin é de 2 mg / kg de peso corporal, começando uma semana após a dose de carga.
Administração em combinação com paclitaxel ou docetaxel
Nos estudos principais (H0648g, M77001), paclitaxel ou docetaxel foram administrados no dia após a primeira dose de Herceptin (para a dose, ver o Resumo das Características do Medicamento (RCM) de paclitaxel ou docetaxel) e imediatamente após as doses subsequentes de Herceptin se o anterior A dose de Herceptin foi bem tolerada.
Administração em combinação com um inibidor de aromatase
No estudo principal (BO16216), Herceptin e anastrozol foram administrados a partir do dia 1. Não houve restrições no momento da administração de Herceptin e anastrozol (para a dose, consulte o RCM para anastrozol ou outros inibidores da aromatase).
Câncer de mama em estágio inicial
Administração a cada três semanas e semanalmente
Quando administrado três vezes por semana, a dose inicial recomendada de Herceptin é de 8 mg / kg de peso corporal. A dose de manutenção recomendada de Herceptin em intervalos de três semanas é de 6 mg / kg de peso corporal, começando três semanas após a dose de carga.
Na administração semanal (dose de ataque inicial de 4 mg / kg seguida de 2 mg / kg uma vez por semana) concomitantemente com paclitaxel após quimioterapia com doxorrubicina e ciclofosfamida.
Ver secção 5.1 para a dose de quimioterapia combinada.
Câncer gástrico metastático
Administração a cada três semanas
A dose de carga inicial recomendada é de 8 mg / kg de peso corporal. A dose de manutenção recomendada em intervalos de três semanas é de 6 mg / kg de peso corporal, começando três semanas após a dose de carga.
Câncer de mama metastático e em estágio inicial e câncer gástrico metastático
Duração do tratamento
Os doentes com cancro da mama metastático ou cancro gástrico metastático devem ser tratados com Herceptin até à progressão da doença. Os doentes com cancro da mama em fase inicial devem ser tratados com Herceptin durante 1 ano ou até ocorrer recorrência, o que ocorrer primeiro. Não é recomendado o prolongamento do tratamento com EBC por mais de um ano (ver secção 5.1).
Redução da dosagem
Não foram feitas reduções de dose de Herceptin nos ensaios clínicos. Os doentes podem continuar a terapêutica com Herceptin durante os períodos de mielossupressão induzida por quimioterapia reversível, mas devem ser cuidadosamente monitorizados durante este período quanto a complicações relacionadas com neutropenia. Consulte o RCM do paclitaxel, docetaxel ou o inibidor da aromatase para reduzir ou atrasar a dosagem.
Se a porcentagem da fração de ejeção do ventrículo esquerdo (FEVE) diminuir ≥ 10 pontos da linha de base e cair abaixo de 50%, a dosagem deve ser suspensa e a avaliação da FEVE repetida em aproximadamente 3 semanas. Se a FEVE não melhorar ou diminuir ainda mais, ou se houver desenvolvimento de insuficiência cardíaca congestiva (ICC) sintomática, a interrupção de Herceptin deve ser seriamente considerada, a menos que os benefícios para o paciente individual superem os riscos. Todos esses pacientes terão que ser avaliados por um cardiologista e acompanhados ao longo do tempo.
Doses perdidas
Se o doente tiver esquecido uma dose de Herceptin durante uma semana ou menos, a dose de manutenção habitual de Herceptin (semanal: 2 mg / kg, cada 3 semanas: 6 mg / kg) deve ser administrada o mais rapidamente possível. Não espere pelo próximo ciclo programado. As doses de manutenção subsequentes de Herceptin devem ser administradas 7 ou 21 dias mais tarde, dependendo do respetivo regime posológico: semanalmente ou a cada três semanas.
Se o paciente perdeu uma dose de Herceptin por mais de uma semana, uma nova dose de ataque de Herceptin deve ser administrada em aproximadamente 90 minutos (dose semanal: 4 mg / kg, dose a cada 3 semanas: 8 mg / kg) assim que possível. As doses de manutenção subsequentes de Herceptin (administração semanal: 2 mg / kg, administração a cada 3 semanas: 6 mg / kg, respetivamente) devem ser administradas 7 ou 21 dias mais tarde, dependendo do respetivo regime posológico: semanalmente ou a cada três semanas.
Populações particulares
Não foram realizados estudos farmacocinéticos na população idosa e em indivíduos com disfunção renal ou hepática. Numa análise farmacocinética populacional, a idade e a insuficiência renal não alteraram a disponibilidade de trastuzumab.
População pediátrica
Não há indicação de um uso específico de Herceptin na população pediátrica.
Método de administração
A dose de carga de Herceptin deve ser administrada por perfusão intravenosa de 90 minutos. Não administrar por injeção intravenosa ou bólus intravenoso. A perfusão intravenosa de Herceptin deve ser administrada por profissionais de saúde com formação no tratamento da anafilaxia e na presença de equipamento de emergência. Os pacientes devem ser observados por pelo menos seis horas após o início da primeira infusão e por duas horas após o início das infusões subsequentes quanto a sintomas, como febre e calafrios ou outros sintomas relacionados à infusão (ver seções 4.4 e 4.8. Esses sintomas podem ser controlada interrompendo a infusão ou diminuindo a taxa. A infusão pode ser reiniciada assim que os sintomas forem aliviados.
Se a dose de ataque inicial for bem tolerada, as doses subsequentes podem ser administradas como uma infusão de 30 minutos.
Para obter instruções sobre a reconstituição da formulação intravenosa de Herceptin antes da administração, ver secção 6.6.
04.3 Contra-indicações
• Hipersensibilidade conhecida ao trastuzumab, às proteínas de rato ou a qualquer um dos excipientes listados na secção 6.1.
• Pacientes com dispneia grave em repouso, devido a complicações de neoplasias avançadas, ou pacientes que requerem terapia de oxigênio suplementar.
04.4 Advertências especiais e precauções adequadas de uso
Para melhorar a rastreabilidade dos medicamentos biológicos, o nome comercial e o número do lote do produto administrado devem ser claramente registrados (ou declarados) no prontuário do paciente.
O teste para HER2 deve ser realizado em um laboratório especializado que possa garantir a validação adequada dos procedimentos analíticos (ver seção 5.1).
Atualmente, não existem dados de ensaios clínicos sobre o retratamento de doentes previamente expostos a Herceptin para tratamento adjuvante.
Disfunção cardíaca
Considerações gerais
Os pacientes tratados com Herceptin apresentam risco aumentado de desenvolver ICC (Classe II-IV de acordo com New York Heart Association [NYHA]) ou disfunção cardíaca assintomática. Estes acontecimentos foram observados em doentes tratados apenas com Herceptin ou em terapêutica combinada com paclitaxel ou docetaxel, particularmente após quimioterapia com antraciclinas (doxorrubicina ou epirrubicina). Têm intensidade moderada a grave e foram associados à morte (ver parágrafo 4.8). Além disso, deve-se ter cuidado especial ao tratar pacientes com risco cardíaco aumentado, por ex. hipertensão, doença arterial coronariana confirmada, ICC, fração de ejeção do ventrículo esquerdo (FEVE) velhice.
Todos os candidatos ao tratamento com Herceptin, mas particularmente os pacientes previamente expostos ao tratamento com antraciclina e ciclofosfamida (AC), devem ser submetidos a avaliação do estado cardíaco inicial, incluindo história e exame físico, eletrocardiograma (ECG), ecocardiograma e / ou Varredura de aquisição de múltiplas portas (MUGA) ou ressonância magnética. O monitoramento pode ajudar a identificar pacientes que desenvolvem disfunção cardíaca. A avaliação da função cardíaca, conduzida da mesma forma que a inicial, deve ser repetida a cada 3 meses durante o tratamento e a cada 6 meses após a interrupção do tratamento até 24 meses após a última administração de Herceptin.
Com base na análise farmacocinética da população de todos os dados disponíveis (ver secção 5.2), o trastuzumab pode permanecer na circulação até 7 meses após a interrupção de Herceptin. Os doentes que recebem antraciclinas após terminar o tratamento com Herceptin podem ter um risco aumentado de disfunção cardíaca. Se possível, os médicos devem evitar a terapia com antraciclinas até 7 meses após a interrupção do Herceptin.Se forem usadas antraciclinas, a função cardíaca do paciente deve ser monitorada de perto.
A avaliação cardiológica formal deve ser considerada em pacientes que apresentaram problemas cardiológicos após a triagem inicial. A função cardíaca deve ser monitorada durante o tratamento em todos os pacientes (por exemplo, a cada 12 semanas). O monitoramento pode auxiliar na identificação de pacientes que desenvolvem disfunção cardíaca. Os pacientes que desenvolvem disfunção cardíaca assintomática podem se beneficiar de um monitoramento mais frequente (por exemplo, a cada 6-8 semanas). No caso de pacientes que relatam diminuição contínua da função ventricular esquerda, mas permanecem assintomáticos, o médico deve considerar a interrupção da terapia se não houver benefício clínico da terapia com Herceptin.
A segurança de continuar ou reiniciar Herceptin em pacientes com disfunção cardíaca não foi investigada em estudos prospectivos. Se a FEVE diminuir ≥ 10 pontos da linha de base e cair abaixo de 50%, a dosagem deve ser suspensa e a FEVE avaliada novamente em aproximadamente 3 semanas. Se a FEVE diminuir não melhorar ou diminuir ainda mais, ou desenvolver ICC sintomática, a descontinuação de Herceptin deve ser seriamente considerada, a menos que os benefícios para o paciente individual sejam considerados maiores que os riscos. Esses pacientes devem ser avaliados por um cardiologista e acompanhados ao longo do tempo.
Se ocorrer insuficiência cardíaca sintomática durante a terapia com Herceptin, ela deve ser tratada com terapias medicamentosas padrão para ICC. A maioria dos pacientes que desenvolveram ICC ou disfunção cardíaca assintomática nos estudos principais melhorou com o tratamento padrão com um inibidor da enzima de conversão da angiotensina (ECA) ou bloqueador do receptor da angiotensina (ARB) e um bloqueador beta. A maioria dos pacientes com sintomas cardíacos e evidência de benefício clínico associado ao Herceptin o tratamento continuou a terapia sem outros eventos clínicos cardíacos.
Câncer de mama metastático
Herceptin não deve ser administrado concomitantemente com antraciclinas no contexto do MBC.
Os doentes com MBC que receberam anteriormente antraciclinas também correm o risco de disfunção cardíaca com o tratamento com Herceptin, embora este risco seja inferior do que com a utilização concomitante de Herceptin e antraciclinas.
Câncer de mama em estágio inicial
Para pacientes com CEP, a avaliação cardiológica, realizada da mesma forma que a inicial, deve ser repetida a cada 3 meses durante o tratamento e a cada 6 meses após a interrupção do tratamento, até 24 meses após a última administração de Herceptin. Recomenda-se monitorização adicional em doentes a receber quimioterapia à base de antraciclina e deve ser efectuada anualmente até 5 anos após a última administração de Herceptin, ou mais tempo se for observada uma diminuição contínua da FEVE.
Pacientes com histórico de infarto do miocárdio (MI), angina de peito que requer tratamento médico, ICC anterior ou atual (NYHA Classe II-IV), cardiomiopatia FEVE, arritmia cardíaca que requer tratamento médico, doença cardíaca valvar clinicamente relevante, hipertensão baixa controlada (hipertensão controlada por tratamento médico padrão apropriado) e derrame pericárdico hemodinamicamente significativo foram excluídos dos estudos principais de tratamento com EBC adjuvante e neoadjuvante com Herceptin. Portanto, o tratamento não pode ser recomendado nesses pacientes.
Tratamento adjuvante
Herceptin não deve ser administrado concomitantemente com antraciclinas no contexto de tratamento adjuvante.
Um aumento da incidência de eventos cardíacos sintomáticos e assintomáticos foi observado em pacientes com câncer de mama inicial quando Herceptin foi administrado após quimioterapia à base de antraciclina em comparação com a administração de um regime de carboplatina com docetaxel e carboplatina não antraciclina e foi mais pronunciado quando Herceptin foi administrado concomitantemente com taxanos do que quando administrado sequencialmente aos taxanos. Independentemente do regime usado, a maioria dos eventos cardíacos sintomáticos ocorreu nos primeiros 18 meses. Em um dos 3 estudos principais em que a acompanhamento mediana de 5,5 anos (BCIRG006), foi observado um aumento sustentado na taxa cumulativa de eventos cardíacos sintomáticos ou FEVE em pacientes recebendo Herceptin concomitantemente com um taxano após terapia com antraciclina de até 2,37% em comparação com aproximadamente 1. "1% nas duas comparações braços (antraciclina mais ciclofosfamida seguida de um taxano e taxano, carboplatina e Herceptin).
Quatro grandes estudos conduzidos no cenário adjuvante identificaram fatores de risco cardíaco, incluindo: idade avançada (> 50 anos), baixa FEVE (medicamentos anti-hipertensivos. Em pacientes tratados com Herceptin após a conclusão da quimioterapia adjuvante, o risco de disfunção cardíaca está associado a um dose cumulativa mais elevada de antraciclinas administradas antes do início da terapêutica com Herceptin e índice de massa corporal (IMC)> 25 kg / m2.
Tratamento neoadjuvante-adjuvante
Em pacientes com EBC que são candidatos ao tratamento neoadjuvante, Herceptin deve ser administrado concomitantemente com antraciclinas apenas em pacientes virgens de quimioterapia e apenas com regimes de antraciclina de baixa dosagem, ou seja, doses cumulativas máximas de doxorrubicina 180 mg / m2 ou epirrubicina 360 mg / m2.
Se os pacientes foram tratados concomitantemente com um ciclo completo de antraciclinas em baixas doses e Herceptin no cenário neoadjuvante, nenhuma quimioterapia citotóxica adicional deve ser administrada após a cirurgia. Em outras situações, a decisão sobre a necessidade de quimioterapia citotóxica adicional deve ser feita de acordo com fatores individuais.
Até à data, a experiência de administração concomitante de trastuzumab com regimes de antraciclina em dose baixa está limitada a dois estudos (MO16432 e BO22227).
No estudo principal MO16432, Herceptin foi administrado concomitantemente com quimioterapia neoadjuvante, contendo três ciclos de doxorrubicina (dose cumulativa de 180 mg / m2).
A incidência de disfunção cardíaca sintomática foi de 1,7% no braço contendo Herceptin.
O estudo principal BO22227 foi desenhado para demonstrar a não inferioridade do tratamento com a formulação subcutânea de Herceptin em comparação com a formulação intravenosa de Herceptin com base em desfechos co-primários de PK e eficácia (Ctrough da pré-dose de trastuzumabe Ciclo 8 e taxa de pCR na cirurgia definitiva, respectivamente ) (ver Seção 5.1 do RCM da formulação subcutânea de Herceptin). No estudo principal BO22227, Herceptin foi administrado concomitantemente com quimioterapia neoadjuvante contendo quatro ciclos de epirrubicina (dose cumulativa de 300 mg / m2); em um acompanhamento médio de 40 meses, a incidência de insuficiência cardíaca congestiva foi de 0,0% no braço do Herceptin IV.
A experiência clínica em pacientes com mais de 65 anos é limitada.
Reações relacionadas à infusão e hipersensibilidade
Foram notificadas reações adversas graves relacionadas com a perfusão de Herceptin, incluindo dispneia, hipotensão, respiração ruidosa, hipertensão, broncoespasmo, taquiarritmia supraventricular, diminuição da saturação de oxigénio, anafilaxia, dificuldade respiratória, urticária e angioedema (ver secção 4.8). A pré-medicação pode ser usada para reduzir o risco de tais eventos. A maioria destes acontecimentos ocorre durante ou nas 2,5 horas após o início da primeira perfusão. Se houver uma reação à perfusão, a perfusão de Herceptin deve ser interrompida ou a velocidade de perfusão reduzida e o doente deve ser monitorizado até à resolução de todos os sintomas observados (ver secção 4.2 ). Esses sintomas podem ser tratados com um analgésico / antipirético, como meperidina ou paracetamol, ou com um anti-histamínico, como difenidramina. A maioria dos pacientes apresentou resolução dos sintomas. Sintomas e subsequentemente recebeu mais infusões de Herceptin. As reações graves foram tratadas com sucesso com terapia de suporte, como oxigênio, beta-agonistas e corticosteroides. Em casos raros, essas reações foram associadas a um curso clínico que culminou em um desfecho fatal. Os pacientes que apresentam dispneia em repouso, devido a complicações de tumores avançados e comorbidades, podem ser em maior risco É mais elevado experimentar uma reação fatal à perfusão. Por conseguinte, estes doentes não devem ser tratados com Herceptin (ver secção 4.3).
Também foram relatadas melhorias iniciais seguidas de piora clínica e reações tardias com rápida deterioração clínica. As mortes ocorreram dentro de horas e até uma semana após a perfusão. Em ocasiões muito raras, os doentes tiveram o início de reações à perfusão e sintomas pulmonares mais de seis horas após o início da perfusão de Herceptin. Os doentes devem ser avisados desta possibilidade. um início tardio e deve ser instruído a entrar em contato com seu médico se isso acontecer.
Eventos pulmonares
Foram notificados acontecimentos pulmonares graves com a utilização de Herceptin no período pós-comercialização (ver secção 4.8). Estes acontecimentos foram ocasionalmente fatais. Foram também notificados casos de doença pulmonar intersticial incluindo infiltrados pulmonares, síndrome da dificuldade respiratória aguda, pneumonia., Pulmão inflamação, derrame pleural, dificuldade respiratória, edema pulmonar agudo e insuficiência respiratória. Os fatores de risco associados à doença pulmonar intersticial incluem terapia prévia ou concomitante com outros tratamentos antineoplásicos, como taxanos, gencitabina, vinorelbina e radioterapia, para os quais essa associação já é conhecida .Estes eventos podem ocorrer no contexto de uma reação à infusão ou ter um início tardio. Pacientes que apresentam dispneia em repouso, devido a complicações de tumores avançados e comorbidades, podem estar em maior risco de sofrer eventos. nti não deve, portanto, ser tratado com Herceptin (ver secção 4.3). Na presença de inflamação pulmonar, deve-se ter cuidado, especialmente em pacientes tratados concomitantemente com taxanos.
04.5 Interações com outros medicamentos e outras formas de interação
Não foram realizados estudos formais de interação medicamentosa. Não foram observadas interações clinicamente significativas entre Herceptin e medicamentos administrados concomitantemente em estudos clínicos.
Efeito do trastuzumabe na farmacocinética de outros antineoplásicos
Os dados farmacocinéticos dos estudos BO15935 e M77004 em mulheres com câncer de mama metastático HER2 positivo sugeriram que a exposição ao paclitaxel e doxorrubicina (e seus metabólitos principais 6-α hidroxil-paclitaxel, POH e doxorrubicinol, DOL) não foi alterada pela presença de trastuzumabe (Dose de carga IV de 8 mg / kg ou 4 m / kg seguida de 6 mg / kg q3w ou 2 mg / kg q1w IV, respectivamente).
No entanto, o trastuzumab pode aumentar a exposição total de um metabolito da doxorrubicina (7-desoxi-13 di-hidro-doxorrubicinona, D7D). A bioatividade do D7D e o efeito clínico do aumento deste metabolito não foram claros.
Os dados do estudo JP16003, de braço único com Herceptin (dose de ataque IV 4 mg / kg e IV 2 mg / kg semanalmente) e docetaxel (60 mg / m2 IV), realizado em mulheres japonesas com câncer de mama metastático HER2 positivo, sugeriram que a administração de Herceptin não teve efeito na farmacocinética de dose única do docetaxel. JP19959 é um subestudo do estudo BO18255 (ToGA) realizado em pacientes japoneses do sexo masculino e feminino com câncer gástrico avançado para estudar o perfil farmacocinético da capecitabina e da cisplatina administrada com ou sem Herceptin. Os resultados deste subestudo sugerem que a exposição aos metabolitos bioativos (por exemplo, 5-FU) da capecitabina não foi alterada pelo uso concomitante de cisplatina em monoterapia ou cisplatina com Herceptin. No entanto, a própria capecitabina mostrou concentrações mais elevadas e uma semivida mais longa quando combinada com Herceptin. Os dados também sugerem que a farmacocinética da cisplatina não foi alterada pelo uso concomitante de capecitabina ou capecitabina em combinação com Herceptin.
Os dados farmacocinéticos do estudo H4613g / GO01305 em pacientes com câncer de mama HER2-positivo metastático ou localmente avançado inoperável sugeriram que o trastuzumabe não teve impacto na farmacocinética da carboplatina.
Efeitos dos antineoplásicos na farmacocinética do trastuzumabe
A comparação das concentrações séricas simuladas de trastuzumabe após a monoterapia com Herceptin (4 mg / kg dose de carga / 2 mg / kg q1w IV) e as concentrações séricas observadas em mulheres japonesas com câncer de mama metastático HER2 positivo (estudo JP16003) mostrou que a administração concomitante de docetaxel não teve efeito na farmacocinética do trastuzumab.
Uma comparação dos dados farmacocinéticos de dois estudos de Fase II (BO15935 e M77004) e um estudo de Fase III (H0648g), em que os pacientes receberam tratamento concomitante com Herceptin e paclitaxel, e dois estudos de Fase II nos quais Herceptin foi administrado como monoterapia (W016229 e MO16982), em mulheres com câncer de mama metastático HER2 positivo, indica que as concentrações mínimas séricas individuais e médias de trastuzumabe variam dentro e entre os estudos, mas não está claro o efeito da administração concomitante de paclitaxel na farmacocinética de trastuzumabe. Uma comparação dos dados farmacocinéticos do trastuzumabe do estudo M77004 no qual mulheres com câncer de mama metastático HER2-positivo receberam tratamento concomitante com Herceptin, paclitaxel e doxorrubicina, e dados farmacocinéticos do trastuzumabe nos estudos nos quais Herceptin foi administrado sozinho (H0649g) ou em combinação com antraciclina mais ciclofosfamida ou paclitaxel (Estudo H0648g), sugeriu que a doxorrubicina e o paclitaxel não têm efeito na farmacocinética do trastuzumabe.
Os dados farmacocinéticos do estudo H4613g / GO01305 sugeriram que a carboplatina não teve efeito na farmacocinética do trastuzumab.
A coadministração de anastrozol não parece ter afetado a farmacocinética do trastuzumab.
04.6 Gravidez e lactação
Mulheres em idade fértil
As mulheres com potencial para engravidar devem ser avisadas da necessidade de utilizar métodos contracetivos eficazes durante o tratamento com Herceptin e 7 meses após o final do tratamento (ver secção 5.2).
Gravidez
Estudos de reprodução foram conduzidos em macacos cinomolgo em doses até 25 vezes a dose de manutenção humana semanal de 2 mg / kg da formulação intravenosa de Herceptin e não revelou evidência de fertilidade prejudicada ou dano fetal. A transferência placentária de trastuzumab foi observada durante o período de desenvolvimento. fetal precoce (dias 20-50 de gestação ) e tardia (dias 120-150 de gestação). Não se sabe se Herceptin pode afetar a capacidade reprodutiva. Como os estudos de reprodução animal nem sempre são preditivos de efeitos em "machos, Herceptin deve ser evitado na gravidez, a menos que haja benefícios potenciais para a mãe superam os riscos potenciais para o feto.
Houve notificações pós-comercialização de comprometimento do desenvolvimento e / ou função renal em associação com oligoidrâmnio, alguns associados a hipoplasia pulmonar fetal fatal, em mulheres grávidas tratadas com Herceptin. Em caso de gravidez, a mulher deve ser informada da possibilidade de danos ao feto. É aconselhável uma monitorização cuidadosa por uma equipa multidisciplinar se uma mulher grávida for tratada com Herceptin ou se ocorrer gravidez durante o tratamento com Herceptin ou nos 7 meses após a última dose do medicamento.
Hora da alimentação
Um estudo em macacos Cynomolgus Durante a lactação, em doses 25 vezes superiores à dose de manutenção humana semanal de 2 mg / kg da formulação intravenosa de Herceptin, demonstrou que o trastuzumab é excretado no leite. A presença de trastuzumab no soro neonatal do macaco não foi associada a quaisquer efeitos adversos no crescimento ou desenvolvimento desde o nascimento até 1 mês de idade. Não se sabe se o trastuzumab é excretado no leite materno. Uma vez que a IgG1 humana é excretada no leite materno e o risco potencial de danos para o recém-nascido é desconhecido, as mulheres não devem amamentar durante a terapêutica com Herceptin e nos 7 meses após a última dose.
Fertilidade
Não há dados de fertilidade disponíveis.
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
Herceptin não tem ou tem uma influência negligenciável sobre a capacidade de conduzir e utilizar máquinas. No entanto, os doentes que desenvolverem sintomas relacionados com a perfusão (ver secção 4.4) devem ser aconselhados a não conduzir e utilizar máquinas até que os sintomas desapareçam.
04.8 Efeitos indesejáveis
Resumo do perfil de segurança
Entre as reações adversas mais graves e / ou frequentes notificadas até à data com a utilização de Herceptin (formulação intravenosa e formulação subcutânea) encontram-se: disfunção cardíaca, reações à perfusão, hematotoxicidade (particularmente neutropenia), infecções e reações adversas pulmonares.
Lista tabelada de reações adversas
Nesta seção, foram utilizadas as seguintes categorias de frequência: muito comuns (≥1 / 10), comuns (≥1 / 100,
A Tabela 1 apresenta as reações adversas que foram notificadas com a utilização de Herceptin intravenoso em monoterapia ou em combinação com quimioterapia em ensaios clínicos essenciais e no contexto pós-comercialização.
Todos os termos incluídos referem-se à percentagem mais elevada observada em estudos clínicos essenciais.
Tabela 1: Efeitos indesejáveis notificados com Herceptin intravenoso em monoterapia ou em combinação com quimioterapia em ensaios clínicos essenciais (N = 8386) e no período pós-comercialização
+ Indica reações adversas relatadas em associação com um resultado fatal.
1 Indica reações adversas notificadas em grande parte em associação com Reações Relacionadas com a Infusão.Não existem percentagens específicas disponíveis para estas.
* Observado com terapia combinada após tratamento com antraciclinas, em combinação com taxanos.
Descrição de reações adversas específicas
Disfunção cardíaca
A insuficiência cardíaca congestiva (NYHA Classe II-IV) é uma reação adversa frequente associada à utilização de Herceptin e foi associada a um resultado fatal (ver secção 4.4). Em doentes tratados com Herceptin foram observados sinais e sintomas de disfunção cardíaca, tais como dispneia, ortopneia, tosse aumentada, edema pulmonar, galope s3, fração de ejeção ventricular reduzida (ver secção 4.4).
Em 3 ensaios clínicos essenciais com Herceptin como adjuvante administrado em combinação com quimioterapia, a incidência de disfunção cardíaca de grau 3/4 (especificamente insuficiência cardíaca congestiva sintomática) foi semelhante em doentes a receber apenas quimioterapia (por exemplo, aqueles que não receberam Herceptin) e em doentes receber Herceptin sequencialmente após um taxano (0,3-0,4%). A percentagem mais elevada foi observada em doentes a receber Herceptin concomitantemente com um taxano (2,0%). A experiência com a administração concomitante de Herceptin e antraciclinas em baixas doses no quadro neoadjuvante é limitada (ver secção 4.4).
Quando o Herceptin foi administrado após a conclusão da quimioterapia adjuvante, foi observada insuficiência cardíaca NYHA Classe III-IV em 0,6% dos doentes no braço tratado durante um ano após um seguimento médio de 12 meses. No estudo BO16348 após um acompanhamento médio de 8 anos, a incidência de ICC grave (NYHA Classes III e IV) no braço de 1 ano do Herceptin foi de 0,8% e a taxa de disfunção ventricular esquerda foi levemente sintomática e assintomática foi de 4,6% .
Reversibilidade grave de ICC (definida como uma sequência de pelo menos duas FEVE consecutivas ≥50% pós-evento) foi observada em 71,4% dos pacientes tratados com Herceptin. A reversibilidade foi demonstrada em 79,5% dos pacientes. De disfunção ventricular esquerda levemente sintomática e assintomática. Aproximadamente 17% dos eventos relacionados com a disfunção cardíaca ocorreram após a conclusão do tratamento com Herceptin.
Nos estudos principais sobre o tratamento da doença metastática com a formulação intravenosa de Herceptin, a incidência de disfunção cardíaca variou entre 9% e 12% quando o fármaco foi administrado em combinação com paclitaxel em comparação com 1% - 4% para o paclitaxel sozinho. Em monoterapia, a taxa foi de 6% - 9%. A taxa mais elevada de disfunção cardíaca ocorreu em doentes a receber Herceptin concomitantemente com antraciclinas / ciclofosfamida (27%) e foi significativamente mais elevada do que com antraciclinas / ciclofosfamida isoladamente (7% - 10%). Num estudo clínico subsequente com monitorização prospectiva da função cardíaca, a incidência de insuficiência cardíaca congestiva sintomática foi de 2,2% em doentes tratados com Herceptin e docetaxel em comparação com 0% em doentes tratados com monoterapia com docetaxel. Parte dos doentes (79% ) que desenvolveram disfunção cardíaca nesses ensaios clínicos melhoraram após receber tratamento médico padrão para insuficiência cardíaca congestiva.
Reações à infusão, reações do tipo alérgico e hipersensibilidade
Estima-se que aproximadamente 40% dos pacientes tratados com Herceptin apresentarão alguma forma de reação à infusão. No entanto, a maioria das reações à infusão são de intensidade leve a moderada (sistema de pontuação NCI-CTC) e tendem a ocorrer no início do tratamento, ou seja, durante uma infusão , dois e três, com menor frequência nas infusões subsequentes. Essas reações incluem calafrios, febre, dispneia, hipotensão, respiração ofegante, broncoespasmo, taquicardia, redução da saturação de oxigênio, dificuldade respiratória, erupção cutânea, náuseas, vômitos e dor de cabeça (ver seção 4.4). A taxa de reações relacionadas à infusão em todos os graus variou entre os estudos. dependendo da indicação, método de aquisição de dados e administração de trastuzumabe concomitantemente com quimioterapia ou monoterapia.
As reações anafiláticas graves que requerem intervenções adicionais imediatas podem ocorrer geralmente durante a primeira e a segunda perfusão de Herceptin (ver secção 4.4) e foram associadas a um resultado fatal.
Reações anafilactóides foram observadas em casos isolados.
Hematotoxicidade
Neutropenia febril e leucopenia são eventos muito comumente observados. As reações adversas comumente desenvolvidas incluem: anemia, trombocitopenia e neutropenia. A frequência dos episódios de hipoprotrombinemia é desconhecida. O risco de neutropenia pode aumentar ligeiramente quando trastuzumab é administrado com docetaxel após terapia com antraciclina.
Eventos pulmonares
As reações adversas pulmonares graves ocorrem em associação com o uso de Herceptin e têm sido associadas a um desfecho fatal. Estas incluem, mas não estão limitadas a, infiltrados pulmonares, síndrome da dificuldade respiratória aguda, pneumonia, inflamação pulmonar, derrame pleural, dificuldade respiratória, aguda edema pulmonar e insuficiência respiratória (ver secção 4.4).
Os detalhes sobre as medidas de minimização de risco que estão de acordo com o Plano Europeu de Gestão de Risco são apresentados em Advertências e precauções especiais de utilização (secção 4.4).
Imunogenicidade
No contexto do tratamento com EBC neoadjuvante-adjuvante, 8,1% (24/296) dos doentes tratados com Herceptin intravenoso desenvolveram anticorpos contra o trastuzumab (independentemente da presença de anticorpos na linha de base). Os anticorpos neutralizantes do trastuzumab foram detectados em amostras pós-linha de base em 2 de 24 doentes tratados com Herceptin intravenoso.
A relevância clínica destes anticorpos é desconhecida; no entanto, a farmacocinética, eficácia (determinada pela resposta patológica completa [pCR]) e segurança de Herceptin intravenoso determinada pela ocorrência de reações relacionadas com a administração (ARRs) não parecem estar comprometidas por estes anticorpos.
Não existem dados de imunogenicidade disponíveis para Herceptin no cancro gástrico.
Mudança do tratamento com a formulação intravenosa de Herceptin para o tratamento com a forma subcutânea de Herceptin e vice-versa
O estudo MO22982 examinou a transição do tratamento com formulação intravenosa de Herceptin para o tratamento com formulação subcutânea de Herceptin com o objetivo principal de avaliar a preferência do paciente por administração intravenosa ou subcutânea de trastuzumab. O ensaio analisou 2 coortes (uma tratada com a formulação subcutânea em frasco e a outra com a formulação subcutânea via dispositivo de distribuição) usando um desenho cruzado de 2 braços, em que 488 pacientes foram randomizados para uma de duas sequências de tratamento diferentes de Herceptin dadas a cada três semanas (iv [Ciclos 1-4] → sc [Ciclos 5-8] ou sc [Ciclos 1-4] → iv [Ciclos 5-8]). Assuntos virgens de tratamento com Herceptin IV (20,3%) ou Herceptin IV previamente exposto ( 79,7%). Para a sequência IV → sc (coortes combinadas de formulação de frasco subcutâneo e formulação de dispositivo de administração subcutânea), as taxas relacionadas a eventos adversos (de todos os graus) foram respectivamente descritos antes da troca (ciclos 1-4) e após a troca ( ciclos 5-8) como 53,8% vs. 56,4%; para a sequência sc → ev (coortes combinadas de scin frasco e s.c. via dispositivo de entrega), as taxas de eventos adversos (todos os graus) foram descritas antes da mudança e após a mudança como 65,4% vs. 48,7%.
Antes da mudança (ciclos 1-4), as taxas de início de eventos adversos graves, eventos adversos de grau 3 e descontinuação do tratamento devido a eventos adversos eram baixas (
Notificação de suspeitas de reações adversas
A notificação de suspeitas de reações adversas ocorridas após a autorização do medicamento é importante porque permite a monitorização contínua da relação benefício / risco do medicamento. Os profissionais de saúde são solicitados a notificar quaisquer suspeitas de reações adversas através do sistema nacional de notificação. "Endereço www. agenziafarmaco.gov.it/it/responsabili.
04.9 Overdose
Não foram relatados casos de sobredosagem em estudos clínicos em humanos. Doses únicas de Herceptin, usadas isoladamente, superiores a 10 mg / kg não foram administradas em estudos clínicos. Até este nível, as doses foram bem toleradas.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
Grupo farmacoterapêutico: agentes antineoplásicos, anticorpos monoclonais, código ATC: L01XC03
O trastuzumab é um anticorpo monoclonal IgG1 humanizado recombinante contra o receptor 2 do fator de crescimento epitelial humano (HER2). A superexpressão de HER2 é observada em 20% -30% dos cânceres de mama primários. Estudos sobre as taxas de positividade de HER2 em câncer gástrico (GC) detectado por imunohistoquímica (IHC) e hibridização no local fluorescente (FISH) ou hibridização no local cromogênica (CISH) mostraram que há uma "ampla variabilidade na positividade de HER2 em uma faixa de 6,8% a 34,0% para IHC e 7,1% a 42,6% para FISH." Estudos mostraram que pacientes com câncer de mama com superexpressão de HER2 têm uma sobrevida livre de doença mais curta do que pacientes com câncer sem superexpressão de HER2. O domínio extracelular do receptor (ECD, p105) pode ser liberado na corrente sanguínea e medido em amostras de soro.
Mecanismo de ação
Trastuzumabe se liga com "alta afinidade e especificidade ao subdomínio IV, uma região perimembranosa do domínio extracelular de HER2. A ligação de trastuzumabe a HER2 inibe a sinalização independente de ligante de HER2 e impede a clivagem proteolítica de seu domínio extracelular, um mecanismo de ativação de HER2 Consequentemente, o trastuzumabe demonstrou, ambos em vitro que em animais, ser capaz de inibir a proliferação de células tumorais humanas que superexpressam HER 2. Além disso, o trastuzumabe é um mediador potente da citotoxicidade dependente de anticorpos mediada por células (ADCC). Em vitro Foi demonstrado que o ADCC mediado por trastuzumabe é preferencialmente exercido em células tumorais com superexpressão de HER2 em relação às células tumorais sem superexpressão de HER2.
Detecção de superexpressão de HER2 ou amplificação do gene HER2
Detecção de superexpressão de HER2 ou amplificação do gene HER2 no câncer de mama
Herceptin só deve ser usado em pacientes com câncer com superexpressão de HER2 ou amplificação do gene HER2, conforme determinado por um teste preciso e validado. A superexpressão de HER2 deve ser detectada por exame imunohistoquímico (IHC) de seções fixas de tumor (ver seção 4.4). A amplificação do gene HER2 deve ser detectada por hibridização no local por fluorescência (FISH) ou hibridização no local cromogênica (CISH) de seções tumorais fixas. Os doentes que apresentam uma sobreexpressão acentuada de HER2 com uma indicação de uma pontuação IHC de 3+ ou um resultado FISH ou CISH positivo são candidatos ao tratamento com Herceptin.
Para garantir resultados precisos e reprodutíveis, os testes devem ser realizados em laboratórios especializados e capazes de garantir a validação dos procedimentos analíticos.
O sistema recomendado para pontuação de modelos de etiquetagem IHC é o mostrado na Tabela 2:
Tabela 2 Sistema recomendado para pontuação de padrões de marcação IHC em câncer de mama
Em geral, o teste FISH é considerado positivo se a razão entre o número de cópias do gene HER2 por célula tumoral e o número de cópias do cromossomo 17 for maior ou igual a 2, ou se houver mais de 4 cópias do Gene HER2 para células tumorais se o cromossomo 17 não for usado como referência.
Em geral, o teste CISH é considerado positivo se houver mais de 5 cópias do gene HER2 por núcleo em mais de 50% das células cancerosas.
Para obter instruções completas sobre a realização e interpretação dos testes, consulte os folhetos anexos aos pacotes de teste FISH e CISH validados. Recomendações oficiais sobre o teste de HER2 também podem ser aplicadas.
Para qualquer outro método que possa ser usado para avaliar a expressão da proteína ou gene HER2, as análises devem ser realizadas apenas por laboratórios que garantam o desempenho ideal dos métodos validados. Esses métodos devem ser claros, precisos e precisos o suficiente para demonstrar a superexpressão de HER2 e devem ser capazes de distinguir a superexpressão moderada (nível 2+) da alta (nível 3+) de HER2.
Detecção de superexpressão de HER2 ou amplificação do gene HER2 em câncer gástrico
Apenas um teste preciso e validado deve ser usado para determinar a superexpressão de HER2 ou amplificação do gene HER2. IHC é recomendado como um primeiro teste e, nos casos em que a avaliação da amplificação do gene HER2 também é necessária, uma hibridização in situ de íons de prata (SISH) ou técnica de FISH deve ser usada. No entanto, a tecnologia SISH é recomendada para permitir a avaliação paralela da histologia e morfologia do tumor. Para garantir a validação dos procedimentos de avaliação e a produção de resultados precisos e reproduzíveis, o teste HER2 deve ser realizado em laboratório com pessoal treinado. Instruções completas sobre como realizar o teste e interpretar os resultados devem ser encontradas na folha de informações do produto fornecida com os testes usados para avaliação do HER2.
No estudo ToGA (BO18255), os pacientes cujos tumores eram IHC3 + ou FISH positivos foram definidos como HER2-positivos e, portanto, incluídos no estudo. Com base nos resultados do estudo clínico, os efeitos positivos foram limitados a pacientes com um nível mais alto de superexpressão da proteína HER2, definida como 3+ com IHC ou 2+ com IHC e um resultado FISH positivo.
Em um estudo de comparação de metodologia (estudo D008548), um alto grau de concordância (> 95%) foi observado entre as técnicas SISH e FISH para a determinação da amplificação do gene HER2 em pacientes com câncer gástrico.
A superexpressão de HER2 deve ser determinada por exame imunohistoquímico (IHC) de seções de tumor fixas. A amplificação do gene HER2 deve ser detectada por hibridização no local, usando SISH ou FISH, em secções tumorais fixas.
O sistema recomendado para pontuação de modelos de etiquetagem IHC é o mostrado na Tabela 3:
Tabela 3 Sistema recomendado para pontuação de padrões de marcação IHC em câncer gástrico
Em geral, os testes SISH ou FISH são considerados positivos se a razão entre o número de cópias do gene HER2 por célula tumoral e o número de cópias do cromossomo 17 for maior ou igual a 2.
Eficácia clínica e segurança
Câncer de mama metastático
O Herceptin foi utilizado isoladamente em ensaios clínicos em doentes com MBC com tumores caracterizados por sobreexpressão de HER2 e falha de um ou mais regimes de quimioterapia anteriores para doença metastática (apenas Herceptin).
Herceptin também foi usado em combinação com paclitaxel ou docetaxel para tratar pacientes virgens de quimioterapia para doença metastática. Os doentes pré-tratados com quimioterapia adjuvante à base de antraciclina foram tratados com paclitaxel (175 mg / m2 administrado como perfusão de 3 horas) com ou sem Herceptin. No estudo principal com docetaxel (100 mg / m2 administrado como perfusão de 1 hora) com ou sem Herceptin, 60% dos doentes tinham anteriormente recebido quimioterapia adjuvante à base de antraciclina. Os pacientes foram tratados com Herceptin até a progressão da doença.
A eficácia de Herceptin em combinação com paclitaxel em pacientes que não receberam terapia adjuvante com antraciclina não foi estudada.No entanto, a combinação de Herceptin com docetaxel foi eficaz, independentemente de os pacientes terem recebido terapia adjuvante anterior ou não com antraciclinas.
O método usado para analisar a superexpressão de HER2 e determinar a elegibilidade dos pacientes para participar de ensaios clínicos essenciais de monoterapia com Herceptin e Herceptin mais paclitaxel empregou a coloração imuno-histoquímica de HER2 de material fixo de tumores de mama usando anticorpos monoclonais murinos CB11 e 4D5. Esses tecidos foram fixados em formalina ou fixador de Bouin. Este método de ensaio usado em estudos clínicos e realizado em um laboratório central usou uma escala de 0 a 3+. Pacientes classificados por uma coloração 2+ ou 3+ foram incluídos, enquanto aqueles com uma coloração 0 ou 1+ foram excluídos Mais de 70% dos pacientes inscritos tinham 3+ "superexpressão". Os dados adquiridos sugerem que os efeitos benéficos foram maiores em pacientes com níveis mais elevados de superexpressão de HER2 (3+).
O método analítico primário usado para determinar a positividade de HER2 no estudo principal com docetaxel, com ou sem Herceptin, foi a imunohistoquímica.Uma minoria de pacientes foi testada por hibridização. no local em fluorescência (FISH). Neste estudo, 87% dos pacientes inscritos foram caracterizados por doença IHC3 +, e 95% por doença IHC3 + e / ou FISH-positiva.
Administração semanal em câncer de mama metastático
Os resultados de eficácia de estudos de monoterapia e combinação estão resumidos na Tabela 4:
Tabela 4 Resultados de eficácia de estudos de monoterapia e terapia combinada
TTP = tempo de progressão; "n / D." indica que não pôde ser avaliado ou que ainda não foi alcançado.
1 Estudo H0649g: Subpopulações de pacientes IHC3 +
2 Estudo H0648g: Subpopulações de pacientes IHC3 +
3 Estudo M77001: População com intenção de tratar, resultados em 24 meses
Tratamento de combinação de Herceptin com anastrozol
Herceptin foi estudado em combinação com anastrozol para o tratamento de primeira linha de pacientes na pós-menopausa com CBM superexpressando HER2 positivo para receptor hormonal (por exemplo, receptor de estrogênio (ER) e / ou receptor de progesterona (PR)). A sobrevida livre de progressão dobrou no braço com Herceptin em combinação com anastrozol em comparação com o braço com anastrozol sozinho (4,8 meses versus 2,4 meses). Para os outros parâmetros, as melhorias observadas no braço de combinação foram: resposta total (16,5% vs 6,7%), benefício clínico (42,7% vs 27,9%), tempo de progressão (4, 8 meses versus 2,4 meses). Não houve diferença entre os dois braços em termos de tempo de resposta e duração da resposta. A sobrevida global mediana foi prolongada em 4,6 meses para os pacientes no braço da combinação. A diferença não foi estatisticamente significativa, no entanto, mais da metade dos pacientes inscritos no braço de anastrozol sozinho foram tratados com um regime contendo Herceptin após a progressão da doença.
Administração a cada três semanas em câncer de mama metastático
Os dados de eficácia de estudos não comparativos de monoterapia e terapia de combinação estão resumidos na Tabela 5 abaixo:
Tabela 5 Resultados de eficácia de estudos não comparativos conduzidos como monoterapia e em terapia combinada
TTP = tempo de progressão; "n / D." indica que não pôde ser avaliado ou que ainda não foi alcançado.
1. Estudo WO16229: dose de carga de 8 mg / kg, seguida por 6 mg / kg a cada 3 semanas
2. Estudo MO16982: dose de carga 6 mg / kg por semana 3 vezes; seguido por 6 mg / kg a cada 3 semanas
3. Estudo BO15935
4. Estudo MO16419
Sites de progressão
A frequência de progressão hepática foi significativamente reduzida em pacientes tratados com a combinação Herceptin-paclitaxel em comparação com paclitaxel sozinho (21,8% versus 45,7%; p = 0,004). Mais pacientes tratados com Herceptin e paclitaxel apresentaram progressão do sistema nervoso central em comparação com pacientes tratados com paclitaxel sozinho (12,6% versus 6,5%; p = 0,377).
Câncer de mama em estágio inicial (configuração adjuvante)
O câncer de mama em estágio inicial é definido como câncer de mama primário não metastático, invasivo.
O uso de Herceptin no contexto da terapia adjuvante foi investigado em 4 grandes estudos multicêntricos, randomizados:
• O estudo BO16348 foi desenhado para comparar o tratamento com Herceptin a cada três semanas por um e dois anos versus observação apenas em pacientes com EBC HER2 positivo após a cirurgia, quimioterapia padrão e radioterapia (se aplicável). Também foi feita uma comparação entre o tratamento com Herceptin durante um ano e o tratamento com Herceptin durante dois anos. Os doentes que pretendiam receber Herceptin receberam uma dose de ataque inicial de 8 mg / kg, seguida de 6 mg / kg a cada três semanas durante um ou dois anos.
• Os estudos NSAPB B-31 e NCCTG N9831, incluindo uma análise agrupada, foram concebidos para avaliar a utilidade clínica da combinação do tratamento com Herceptin com paclitaxel após quimioterapia AC; além disso, o estudo NCCTG N9831 também avaliou a adição sequencial de quimioterapia com Herceptin versus AC → P em pacientes com EBC HER2 positivo após a cirurgia.
• O estudo BCIRG 006 foi concebido para avaliar a associação do tratamento com Herceptin com docetaxel após quimioterapia AC ou docetaxel e carboplatina em doentes com EBC HER2 positivo após cirurgia.
O câncer de mama inicial no estudo HERA foi limitado a adenocarcinoma de mama invasivo primário operável com linfonodos axilares positivos ou linfonodos axilares negativos, se com tumor de pelo menos 1 cm de diâmetro.
Na análise conjunta de NSAPB B-31 e NCCTG N9831, EBC foi limitado a mulheres com câncer de mama de alto risco operável, definido como HER2 positivo e linfonodo axilar positivo ou HER2 positivo e linfonodo axilar negativo com características de alto risco (tamanho do tumor > 1 cm e ER negativo ou tamanho do tumor> 2 cm, independentemente do estado hormonal).
No estudo BCIRG 006, EBC HER2 positivo foi limitado a pacientes com linfonodo positivo ou negativo com alto risco definido como envolvimento de linfonodo ausente (pN0) e pelo menos 1 dos seguintes: tamanho do tumor maior que 2 cm, receptores de estrogênio e para progesterona negativa, histológica e / ou nuclear de grau 2-3 ou idade
A Tabela 6 resume os resultados de eficácia do estudo BO16348 após um acompanhamento médio de 12 meses * e 8 anos **:
Tabela 6 Resultados de eficácia do estudo BO16348
* O endpoint co-primário DFS de 1 ano versus observação atingiu o limite estatístico padrão
** Análise final (incluindo cruzamento de 52% dos pacientes do braço de observação para Herceptin)
*** Há uma discrepância geral da amostra devido a um pequeno número de pacientes randomizados após a data de corte para a análise de acompanhamento mediano de 12 meses
Os resultados da análise de eficácia provisória excederam o limite estatístico predeterminado do protocolo para comparar Herceptin por 1 ano versus observação. Após um acompanhamento médio de 12 meses, a razão de risco (HR) para sobrevida livre de doença (DFS) foi de 0,54 (IC de 95% 0,44-0,67) que se traduz em um benefício absoluto, em termos de taxa de sobrevida livre de doença em 2 anos, de 7,6 pontos percentuais (85,8% versus 78,2%) em favor do braço de Herceptin.
Após um acompanhamento médio de 8 anos, foi realizada uma análise final que descobriu que o tratamento com Herceptin por um ano estava associado a uma redução do risco de 24% em comparação com a observação isolada (HR = 0,76, IC de 95% 0,67 - 0,86). se traduz em um benefício absoluto em termos de uma taxa de sobrevida livre de progressão de 8 anos de 6,4 pontos percentuais a favor do tratamento com Herceptin por um ano.
Nesta análise final, prolongar o tratamento com Herceptin por dois anos não mostrou nenhum benefício adicional sobre o tratamento por 1 ano [HR DFS na população com intenção de tratar (ITT) de 2 anos versus 1 ano = 0,99 (IC de 95%: 0,87 - 1,13), valor de p = 0,90 e HR OS = 0,98 (0,83 - 1,15); valor de p = 0,78] A taxa de disfunção ventricular esquerda assintomática foi aumentada no braço de tratamento por 2 anos (8,1% versus 4,6% em o braço de tratamento por 1 ano). Mais pacientes tiveram pelo menos um evento adverso de grau 3 ou 4 no braço de tratamento de 2 anos (20,4%) versus o braço de tratamento de 1 ano (16,3%).
Nos estudos NSAPB B-31 e NCCTG N9831, Herceptin foi administrado em combinação com paclitaxel, após quimioterapia AC.
A doxorrubicina e a ciclofosfamida foram administradas concomitantemente da seguinte forma:
• doxorrubicina push intravenosa, 60 mg / m2, administrada a cada 3 semanas durante 4 ciclos.
• ciclofosfamida intravenosa, 600 mg / m2 durante 30 minutos, administrada a cada 3 semanas por 4 ciclos
Paclitaxel, em combinação com Herceptin, foi administrado da seguinte forma:
• paclitaxel intravenoso - 80 mg / m2 como uma infusão intravenosa contínua, administrado uma vez por semana durante 12 semanas,
ou
• paclitaxel intravenoso - 175 mg / m2 em perfusão intravenosa contínua, administrado uma vez a cada 3 semanas durante 4 ciclos (dia 1 de cada ciclo).
Os resultados de eficácia da análise conjunta de NSAPB B-31 e NCCTG 9831 no momento da análise final de DFS * estão resumidos na Tabela 7. A duração média do acompanhamento foi de 1,8 anos para pacientes no braço AC. → P e 2,0 anos para pacientes no braço AC → PH.
Tabela 7 Resumo dos resultados de eficácia da análise agrupada de NSABP B-31 e NCCTG 9831 no momento da análise final de DFS *
A: doxorrubicina; C: ciclofosfamida; P: paclitaxel; H: trastuzumab
* Na duração mediana de acompanhamento de 1,8 anos para pacientes no braço AC → P e 2,0 anos para pacientes no braço AC → PH.
** O valor p para OS não excedeu o limite estatístico predeterminado para a comparação AC → PH versus AC → P.
Relativo ao "ponto final primário, DFS, a adição de Herceptin à quimioterapia com paclitaxel resultou em uma redução de 52% no risco de recorrência da doença. A taxa de risco se traduz em um benefício absoluto, em termos de taxa de sobrevida livre de doença em 3 anos de 11,8% (87,2% versus 75,4 %) a favor do braço AC → PH (Herceptin).
No momento de uma atualização de segurança, após um acompanhamento médio de 3,5-3,8 anos, uma "análise DFS reconfirmou a extensão do benefício mostrado na análise DFS final". cruzamento de Herceptin no braço de controle, adicionar Herceptin à quimioterapia com paclitaxel resultou em uma redução de 52% no risco de recorrência da doença. Adicionar Herceptin à quimioterapia com paclitaxel também resultou em uma redução de 37% na recorrência da doença. risco de morte.
A análise OS final pré-planejada da análise combinada dos estudos NSABP B-31 e NCCTG 9831 foi realizada no momento de 707 mortes (acompanhamento médio de 8,3 anos no grupo AC → PH). Comparado ao que foi observado com o tratamento AC → P, o tratamento AC → PH resultou em uma melhora estatisticamente significativa no OS (HR estratificado = 0,64; IC de 95% [0,55 - 0,74]; valor de p log-rank
Os resultados finais de OS da análise agrupada de NSABP B-31 e NCCTG 9831 estão resumidos na Tabela 8 abaixo.
Tabela 8 Análise final de sobrevida global a partir da análise combinada de NSABP B-31 e NCCTG 9831
A: doxorrubicina; C: ciclofosfamida; P: paclitaxel; H: trastuzumab
A análise DFS também foi conduzida na análise OS final que emergiu da análise combinada de NSABP B-31 e NCCTG N9831. Os resultados atualizados da análise DFS (HR estratificado = 0,61; IC de 95% [0,54 - 0,69]) mostraram um Benefício de DFS semelhante ao observado na análise primária definitiva de DFS, apesar de 24,8% dos pacientes no braço AC → P cruzarem para o tratamento com Herceptin. Uma taxa de sobrevida livre de doença de 77,2% (IC 95%: 75,4% - 79,1% ) no braço AC → PH foi estimado em 8 anos, com um benefício absoluto de 11,8% em comparação com o braço AC → P.
No estudo BCIRG 006, Herceptin foi administrado em combinação com docetaxel, após quimioterapia com AC (AC → DH) ou em combinação com docetaxel e carboplatina (DCarbH).
O docetaxel foi administrado da seguinte forma:
• docetaxel intravenoso - 100 mg / m2 como uma infusão intravenosa de 1 hora administrada a cada 3 semanas por 4 ciclos (dia 2 do primeiro ciclo de docetaxel, então dia 1 de cada ciclo subsequente)
ou
• docetaxel intravenoso - 75 mg / m2 como uma infusão intravenosa de 1 hora, administrado a cada 3 semanas por 6 ciclos (dia 2 do primeiro ciclo, a seguir dia 1 de cada ciclo subsequente)
seguido pela:
• carboplatina - na AUC alvo = 6 mg / ml / min administrada como uma infusão intravenosa com duração de 30-60 minutos, repetida a cada 3 semanas por um total de seis ciclos
Herceptin foi administrado uma vez por semana em combinação com quimioterapia e a cada 3 semanas daí em diante durante um total de 52 semanas.
Os resultados de eficácia do BCIRG 006 estão resumidos nas Tabelas 9 e 10. A duração mediana do acompanhamento foi de 2,9 anos no braço AC → D e 3,0 anos em cada um dos braços AC → DH e DCarbH.
Tabela 9 Resumo das análises de eficácia do estudo BCIRG 006 AC → D contra AC → DH
AC → D = doxorrubicina em combinação com ciclofosfamida, seguida de docetaxel; AC → DH = doxorrubicina em combinação com ciclofosfamida, seguida de docetaxel em combinação com trastuzumabe; CI = intervalo de confiança.
Tabela 10 Resumo das análises de eficácia do estudo BCIRG 006 AC → D contra DCarbH
AC → D = doxorrubicina em combinação com ciclofosfamida, seguida de docetaxel; DCarbH = docetaxel, carboplatina e trastuzumab; CI = intervalo de confiança
No estudo BCIRG 006 sobre o "ponto final primária, DFS, a taxa de risco se traduz em um benefício absoluto, em termos de sobrevida livre de doença em 3 anos, de 5,8 pontos percentuais (86,7% contra 80,9%) em favor do braço AC → DH (Herceptin) e 4,6 pontos percentuais (85,5% versus 80,9%) em favor do braço DCarbH (Herceptin) sobre AC → D.
No estudo BCIRG 006, 213/1075 pacientes no braço DCarbH (TCH), 221/1074 pacientes no braço AC DH (AC TH) e 217/1073 no braço AC → D (AC T) tinham um status de desempenho de Karnofsky ≤90 (80 ou 90). Nenhum benefício de sobrevida livre de doença (DFS) foi observado neste subgrupo de pacientes (razão de risco = 1,16; IC 95% [0,73, 1,83] para o braço DCarbH (TCH) versus AC. D (AC T); razão de risco 0,97; IC de 95% [0,60, 1,55] para o braço AC DH (AC TH) versus AC D).
Além disso, uma análise foi conduzida post-hoc dados exploratórios da análise conjunta (JA) de NSABP B-31 / NCCTG N9831 e do estudo clínico BCIRG006, combinando DFS e eventos cardíacos sintomáticos, conforme resumido na Tabela 11:
Tabela 11 Análise post-hoc exploração dos resultados da análise conjunta (JA) do NSABP B-31 / NCCTG N9831 e do estudo clínico BCIRG006, combinando DFS e eventos cardíacos sintomáticos
A: doxurobicina; C: ciclofosfamida; P: paclitaxel; D: docetaxel; Carb: carboplatina; H: trastuzumab
CI = intervalo de confiança
* No momento da análise DFS final. A duração mediana do acompanhamento foi de 1,8 anos no braço AC → P e 2,0 anos no braço AC → PH.
Câncer de mama em estágio inicial (contexto neoadjuvante-adjuvante)
Até à data, não existem resultados disponíveis comparando a eficácia de Herceptin administrado com quimioterapia na configuração adjuvante versus a configuração neoadjuvante / adjuvante.
No contexto do tratamento neoadjuvante-adjuvante, o estudo MO16432, um ensaio clínico multicêntrico randomizado, foi desenhado para avaliar a eficácia clínica da administração concomitante de Herceptin com quimioterapia neoadjuvante contendo uma antraciclina e um taxano, seguido por Herceptin como um adjuvante. para um total de 1 ano de tratamento. O estudo envolveu pacientes com EBC localmente avançado (estágio III) ou inflamatório recém-diagnosticado. Pacientes com tumores HER2 + foram randomizados para receber quimioterapia neoadjuvante concomitantemente com Herceptin neoadjuvante-adjuvante ou quimioterapia neoadjuvante isolada.
No estudo MO16432, Herceptin (dose de carga de 8 mg / kg, seguido de 6 mg / kg em manutenção a cada 3 semanas) foi administrado concomitantemente com 10 cursos de quimioterapia neoadjuvante como segue:
• Doxorrubicina 60 mg / m2 e paclitaxel 150 mg / m2, administrados a cada 3 semanas por 3 ciclos,
seguido pela
• Paclitaxel 175 mg / m2 administrado a cada 3 semanas por 4 ciclos,
seguido pela
• CMF no dia 1 e 8 a cada 4 semanas por 3 ciclos,
seguido após a cirurgia por
• cursos adicionais de Herceptin adjuvante (após a conclusão de 1 ano de terapia).
Os resultados de eficácia do estudo MO16432 estão resumidos na Tabela 12. A duração mediana do acompanhamento no braço com Herceptin foi de 3,8 anos.
Tabela 12 Resultados de eficácia do estudo MO16432
* definido como a ausência de carcinoma invasivo na mama e nódulos linfáticos axilares
Foi estimado um benefício absoluto de 13 pontos percentuais em favor do braço do Herceptin em termos de taxa de sobrevida livre de eventos em 3 anos (65% versus 52%).
Câncer gástrico metastático
O Herceptin foi estudado num estudo ToGA de fase III, aleatório e aberto (BO18255) em combinação com quimioterapia versus quimioterapia isolada.
A quimioterapia foi administrada da seguinte forma:
• capecitabina - 1000 mg / m2 por via oral duas vezes ao dia por 14 dias a cada 3 semanas por 6 ciclos (à noite do dia 1 à manhã do dia 15 de cada ciclo)
ou
• 5-fluorouracil intravenoso - 800 mg / m2 / dia como uma infusão intravenosa contínua por 5 dias, administrado a cada 3 semanas por 6 ciclos (dias 1 a 5 de cada ciclo)
Cada um dos dois medicamentos foi administrado com:
• cisplatina - 80 mg / m2 a cada 3 semanas durante 6 ciclos, administrada no dia 1 de cada ciclo.
Os resultados de eficácia do estudo BO18225 estão resumidos na Tabela 13:
Tabela 13 Resultados de eficácia do estudo BO18225
FP + H: Fluoropirimidina / Cisplatina + Herceptina
FP: fluoropirimidina / cisplatina
uma razão de probabilidade
Pacientes não tratados anteriormente para adenocarcinoma HER2 positivo localmente avançado ou recidivante e / ou metastático inoperável do estômago ou junção gastroesofágica, não candidatos para tratamento curativo, foram incluídos no estudo. EU"ponto final primária foi a sobrevida global, definida como o tempo desde a data da randomização até a data da morte por qualquer causa. No momento da análise, um total de 349 pacientes randomizados haviam morrido: 182 pacientes (62,8%) no braço de controle e 167 pacientes (56,8%) no braço de tratamento relacionados ao tumor subjacente.
A análise post-hoc de subgrupo indica que os efeitos positivos do tratamento são limitados a tumores com níveis mais elevados de proteína HER2 (IHC 2 + / FISH + ou IHC 3+). A sobrevida global média no subgrupo com altos níveis de superexpressão de HER2 foi de 11,8 meses versus 16 meses, HR 0,65 (IC 95% 0,51-0,83) e sobrevida livre de progressão foi de 5,5 meses versus 7,6 meses, HR 0,64 (IC 95% 0,51-0,79) no braço FP versus o braço FP + H, respectivamente. a sobrevida global foi de 0,75 (IC 95% 0,51-1,11) no grupo IHC2 + / FISH + e 0,58 (IC 95% 0,41-0,81) no grupo IHC3 + / FISH +.
Em uma análise exploratória de subgrupo realizada no estudo ToGA (BO18255), não houve benefício de sobrevida global aparente com a adição de Herceptin em pacientes com ECOG PS 2 basal [HR 0,96 (IC 95% 0, 51-1,79)], não mensurável [ HR 1,78 (IC 95% 0,87-3,66)] e doença localmente avançada [HR 1,20 (IC 95% 0,29-4,97)].
População pediátrica
A Agência Europeia de Medicamentos retirou a obrigação de apresentação dos resultados dos estudos com Herceptin em todos os subgrupos na população pediátrica no cancro gástrico e da mama (ver secção 4.2 para informação sobre utilização pediátrica).
05.2 Propriedades farmacocinéticas
A farmacocinética do trastuzumabe foi avaliada por análise de modelo farmacocinético populacional usando dados agrupados de 1.582 indivíduos com MBC HER2-positivo, EBC ou câncer gástrico avançado (AGC), ou outros cânceres., E voluntários saudáveis, em 18 estudos de fase I, II e III em que Herceptin foi administrado IV. Um modelo de dois compartimentos com eliminação paralela linear e não linear do compartimento central foi usado para descrever o perfil concentração / tempo. Devido à eliminação não linear, a depuração total aumentou com a diminuição da concentração. nenhum valor de meia-vida constante para trastuzumabe pode ser deduzido. t1 / 2 diminui com concentrações decrescentes ao longo de um intervalo de dose (ver Tabela 16). Pacientes com MBC e EBC tinham valores semelhantes de parâmetros farmacocinéticos [por exemplo, depuração (CL), volume do compartimento à exposição central (Vc) e à exposição em estado estacionário prevista da população (Cmin, Cmax e AUC)]. A depuração linear foi de 0,136 L / dia para MBC, 0,112 L / dia para EBC e 0,176 L / dia para AGC. Os valores do parâmetro de eliminação não linear foram de 8,81 mg / dia. Para a taxa de eliminação máxima (Vmax) e 8,92 mcg / mL para a constante de Michaelis-Menten (Km) para pacientes com MBC, EBC e AGC. O volume do compartimento central foi de 2,62 l para pacientes com MBC e EBC e 3,63 l para pacientes com AGC. Além da forma de tumor primário, o modelo farmacocinético da população final identificou peso corporal, aspartato aminotransferase sérica e albumina como covariáveis estatisticamente efeitos significativos que afetam a exposição ao trastuzumabe. No entanto, a magnitude do efeito dessas covariáveis na exposição ao trastuzumabe sugeriu um efeito clinicamente significativo improvável nas concentrações de trastuzumabe.
Os valores de exposição previstos a partir da farmacocinética populacional (mediana com 5º - 95º percentil) e os valores dos parâmetros farmacocinéticos em concentrações clinicamente relevantes (Cmax e Cmin) para pacientes com MBC, EBC e AGC tratados pelos regimes de dosagem aprovados q1w (dosagem semanal) e q3w (dosagem a cada três semanas) são mostrados na Tabela 14 (Ciclo 1), Tabela 15 (estado estacionário) e Tabela 16 (parâmetros farmacocinéticos).
Tabela 14 Valores Farmacocinéticos de Exposição Prevista da População no Ciclo 1 (Mediana 5º - 95º percentil) para regimes de Herceptin IV em pacientes com MBC, EBC e AGC
Tabela 15 Valores de exposição farmacocinética em estado estacionário previsto para a população (percentil 5 a 95) para regimes de Herceptin IV em pacientes com MBC, EBC e AGC
* Cmin, ss - Cmin em estado estacionário
** Cmax, ss = Cmax em estado estacionário
*** tempo a 90% do estado estacionário
Tabela 16 Valores de parâmetros farmacocinéticos previstos para a população no estado estacionário para regimes IV de Herceptin em pacientes com MBC, EBC e AGC
Lavagem de trastuzumabe
O período de eliminação de trastuzumab foi avaliado após a administração intravenosa q1w ou q3w usando o modelo farmacocinético populacional. Os resultados dessas simulações indicam que pelo menos 95% dos pacientes atingirão as concentrações
Antígeno solúvel circulante
Análises exploratórias de covariáveis com informações para apenas um subgrupo de pacientes sugeriram que indivíduos com níveis mais elevados de antígeno solúvel HER2-ECD (SHED) tiveram depuração não linear mais rápida (Km inferior) (p SGOT / AST; impacto do antígeno solúvel na depuração é atribuível a Níveis SGOT / AST.
Não há dados sobre o nível de domínio extracelular circulante do receptor HER2 (antígeno solúvel) no soro de pacientes com câncer gástrico.
05.3 Dados de segurança pré-clínica
Não houve evidência de toxicidade relacionada à dose única ou repetida em estudos de até 6 meses de duração, nem de toxicidade reprodutiva em estudos de teratologia, fecundidade feminina ou toxicidade no último período de gestação / passagem pela placenta. Herceptin não é genotóxico.A O estudo da trealose, um dos principais excipientes da formulação, não revelou toxicidade.
Não foram realizados estudos a longo prazo em animais para determinar o potencial carcinogénico de Herceptin ou para determinar os seus efeitos na fertilidade masculina.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
Cloridrato de L-histidina
L-histidina
dihidrato de a, a-trealose
polissorbato 20
06.2 Incompatibilidade
Este medicamento não deve ser misturado ou diluído com outros medicamentos além dos mencionados na secção 6.6.
Não dilua com soluções de glicose, pois elas causam agregação da proteína.
06.3 Período de validade
4 anos
Após reconstituição com água para preparações injetáveis, a solução reconstituída permanece física e quimicamente estável durante 48 horas entre 2 ° C e 8 ° C. Os resíduos da solução reconstituída devem ser eliminados.
As soluções de Herceptin para perfusão em sacos de cloreto de polivinilo, polietileno ou polipropileno contendo 9 mg / mL (0,9%) de solução para injecção de cloreto de sódio permanecem física e quimicamente estáveis durante 24 horas a temperaturas não superiores a 30 ° C.
Do ponto de vista microbiológico, a solução reconstituída e a solução para perfusão de Herceptin devem ser utilizadas imediatamente. O produto não deve ser armazenado depois de reconstituído e diluído, a menos que isso tenha sido feito em condições assépticas controladas e validadas. Se o produto não for usado imediatamente, os tempos e as condições de armazenamento em uso são de responsabilidade do usuário.
06.4 Precauções especiais de armazenamento
Conservar na geladeira (2 ° C - 8 ° C)
Para condições de armazenamento após a primeira abertura, consulte as seções 6.3 e 6.6.
06.5 Natureza da embalagem primária e conteúdo da embalagem
Frasco de Herceptin:
Um frasco de 15 ml de vidro transparente tipo I com fecho de borracha butílica laminada com filme de fluororesina contém 150 mg de trastuzumab.
Cada embalagem contém um frasco para injetáveis.
06.6 Instruções de uso e manuseio
Siga as técnicas assépticas adequadas. Cada frasco para injetáveis de Herceptin é reconstituído com 7,2 ml de água estéril para preparações injetáveis (não fornecida). Evitar o uso de outros solventes para reconstituição. Isso dá 7,4 mL de solução unidose, contendo aproximadamente 21 mg / mL de trastuzumabe, com pH de aproximadamente 6,0. Um volume excedente de 4% garante a aspiração do frasco do programado dose de 150 mg.
Herceptin deve ser manuseado com cuidado durante o procedimento de reconstituição. A formação excessiva de espuma causada durante a reconstituição ou agitação da solução reconstituída pode causar problemas com a quantidade de Herceptin que pode ser retirada do frasco para injetáveis.
A solução reconstituída não deve ser congelada.
Instruções para reconstituição:
1) Usando uma seringa estéril, injete lentamente 7,2 mL de água para preparações injetáveis no frasco que contém o Herceptin liofilizado, direcionando o jato para a substância liofilizada.
2) Agite o frasco lentamente para facilitar a reconstituição. NÃO AGITE!
Uma ligeira formação de espuma durante a reconstituição não é incomum. Deixe o frasco na posição vertical por aproximadamente 5 minutos. Uma vez reconstituído, Herceptin assume o aspecto de uma solução límpida, incolor a amarelo claro, sem partículas visíveis.
Determine o volume da solução necessária:
• com base em uma dose de carga de 4 mg de trastuzumabe / kg de peso corporal, ou uma dose semanal subsequente de 2 mg de trastuzumabe / kg de peso corporal:
• com base em uma dose de carga de 8 mg de trastuzumabe / kg de peso corporal, ou uma dose subsequente de 6 mg de trastuzumabe / kg de peso corporal a cada 3 semanas:
Retire a quantidade necessária de solução do frasco e adicione ao saco de infusão contendo 250 mL de solução de cloreto de sódio a 0,9%. Não use soluções contendo glicose (ver seção 6.2). O saco deve ser invertido cuidadosamente para misturar a solução para evitar a formação de espuma. Depois de preparada, a infusão deve ser administrada imediatamente.Se diluída de acordo com métodos assépticos, pode ser conservada por 24 horas (conservar abaixo de 30 ° C).
As soluções para administração parenteral devem ser inspecionadas visualmente quanto a quaisquer partículas ou descoloração antes da administração.
Herceptin destina-se a uma única utilização, uma vez que o produto não contém conservantes. O medicamento não utilizado e os resíduos derivados deste medicamento devem ser eliminados de acordo com os regulamentos locais.
Não foram observadas incompatibilidades entre o Herceptin e as bolsas de policloreto de vinila, polietileno ou polipropileno.
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
Roche Registration Limited
6 Falcon Way
Shire Park
Welwyn Garden City
AL7 1TW
Reino Unido
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
EU / 1/00/145/001
034949014
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
Data da primeira autorização: 28 de agosto de 2000
Data da última renovação: 28 de agosto de 2010
10.0 DATA DE REVISÃO DO TEXTO
Setembro 2015






















-allenamento-per-dimagrire.jpg)