O que é Mirvaso - tartarato de brimonidina e para que é utilizado?
O Mirvaso é um medicamento que contém a substância ativa tartarato de brimonidina. É indicado para o tratamento do eritema facial (vermelhidão da pele do rosto) em adultos com rosácea, uma alteração patológica de longa duração da pele que frequentemente causa rubor e vermelhidão.
Como é usado o Mirvaso - tartarato de brimonidina?
Mirvaso está disponível na forma de gel (3 mg / g) e só pode ser obtido mediante receita médica. Mirvaso só deve ser aplicado na pele do rosto. Uma pequena quantidade de gel, do tamanho de uma ervilha pequena, deve ser aplicada em uma camada fina na pele da testa, queixo, nariz e bochechas. Antes de aplicar outros cremes ou cosméticos, as áreas afetadas devem secar. Para mais informações, consulte o Folheto Informativo.
Como funciona o tartarato de Mirvaso - brimonidina?
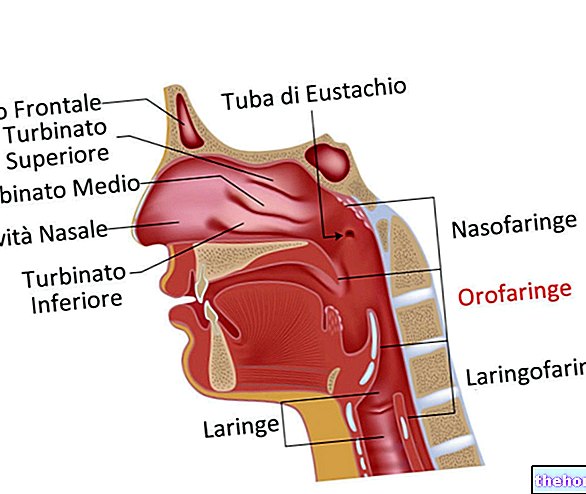
A rosácea é uma alteração que afeta principalmente a pele do rosto. Seus sintomas incluem episódios de vermelhidão que têm sido relacionados à dilatação dos pequenos vasos sanguíneos que irrigam a pele do rosto, com conseqüente aumento do fluxo. área afetada.
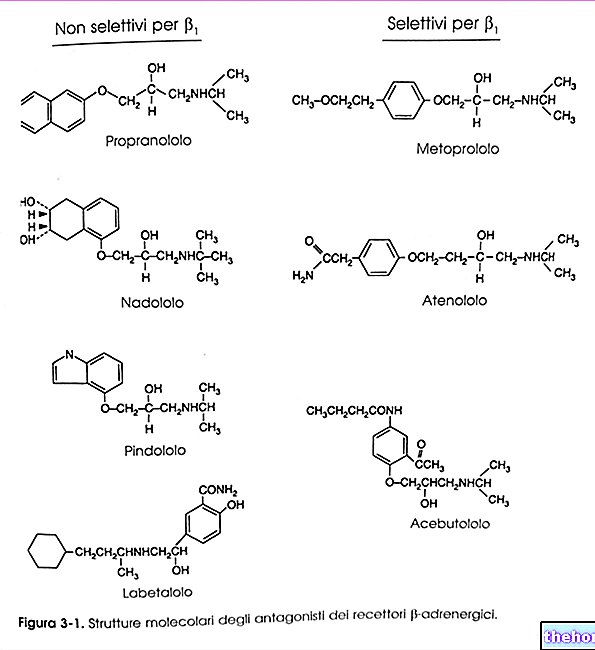
A substância ativa do Mirvaso, o tartarato de brimonidina, atua ligando-se a e ativando certos recetores, denominados recetores alfa2-adrenérgicos, encontrados nas células dos vasos sanguíneos da pele. Isso causa o estreitamento dos vasos sanguíneos, o que reduz o fluxo de sangue para o rosto, diminuindo assim a vermelhidão.
Qual o benefício demonstrado pelo tartarato de Mirvaso - brimonidina durante os estudos?
O Mirvaso foi estudado em dois estudos principais que incluíram um total de 553 doentes com vermelhidão induzida pela rosácea moderada a grave Ambos os estudos compararam o Mirvaso com um placebo (um gel simulado) durante um período de tratamento de quatro semanas. O principal parâmetro de eficácia foi a percentagem de doentes nos quais se observou uma redução acentuada da vermelhidão facial 3, 6, 9 e 12 horas após a aplicação nos dias 1, 15 e 29 desde o início da terapêutica. Em ambos os estudos, o Mirvaso, aplicado uma vez ao dia, foi mais eficaz do que o placebo na redução da vermelhidão facial nestes pacientes.
- No contexto do primeiro estudo, uma redução da vermelhidão facial foi observada 3 horas após a primeira aplicação (dia 1) em 16,3% (21 de 129) dos pacientes tratados com Mirvaso em comparação com 3,1% (4 de 131) tratados com placebo. O efeito durou 12 horas após a aplicação, embora tenha começado a desaparecer após 6 horas. No dia 29, 31,5% (40 em 127) dos pacientes mostraram uma redução na vermelhidão facial 3 horas após a aplicação com Mirvaso em comparação com uma resposta de 10,9% (14 em 128) registrada com o placebo.
- No segundo estudo, foi observada uma redução na vermelhidão facial 3 horas após a primeira aplicação (dia 1) em 19,6% (29 de 148 pacientes) dos pacientes tratados com Mirvaso em comparação com 0% (nenhum de 145 pacientes) tratados com placebo . Também neste caso, o efeito positivo durou 12 horas após a aplicação, embora tenha começado a desaparecer após 6 horas. No dia 29, 25,4% (36 em 142) dos pacientes mostraram uma redução na vermelhidão facial 3 horas após a aplicação com Mirvaso em comparação com uma resposta de 9,2% (13 em 142) registrada com o placebo.
Qual é o risco associado ao tartarato de Mirvaso - brimonidina?
Os efeitos secundários mais frequentes associados ao Mirvaso (que podem afetar mais de 1 100 pessoas), geralmente de grau ligeiro a moderado, são eritema (vermelhidão), comichão, rubor e sensação de queimadura na pele. Para a lista completa dos efeitos secundários notificados com Mirvaso, consulte o Folheto Informativo Mirvaso não deve ser utilizado em crianças com menos de 2 anos de idade ou em doentes tratados com outros medicamentos, incluindo inibidores da monoamina oxidase (MAO) ou certos antidepressivos. não indicado em crianças ou adolescentes com idade entre 2 e 18 anos. Consulte o folheto informativo para a lista completa de restrições.
Por que foi aprovado o tartarato de Mirvaso - brimonidina?
O Comité dos Medicamentos para Uso Humano (CHMP) da Agência concluiu que os benefícios do Mirvaso são superiores aos seus riscos e recomendou a sua aprovação para utilização na UE. O CHMP concluiu que o Mirvaso melhora a vermelhidão da pele do rosto em doentes com rosácea. Em relação à segurança, o CHMP reconheceu que o perfil de segurança é aceitável, uma vez que os eventos adversos relatados são distúrbios locais, ou seja, que afetam a pele, e são semelhantes aos geralmente observados com outros medicamentos tópicos usados no tratamento da rosácea.
Que medidas estão a ser adotadas para garantir a utilização segura e eficaz do tartarato de Mirvaso - brimonidina?
Um plano de gerenciamento de risco foi desenvolvido para garantir que o Mirvaso seja usado da forma mais segura possível. Com base neste plano, as informações de segurança foram adicionadas ao resumo das características do medicamento e folheto informativo de Mirvaso, incluindo as precauções adequadas a serem seguidas por profissionais de saúde e pacientes. Mais informações podem ser encontradas no resumo do plano de gerenciamento de riscos.
Mais informações sobre Mirvaso - tartarato de brimonidina
Em 21 de fevereiro de 2014, a Comissão Europeia emitiu uma "Autorização de Introdução no Mercado" para o Mirvaso, válida em toda a União Europeia. Para mais informações sobre a terapia com Mirvaso, leia o Folheto Informativo (incluído no EPAR) ou consulte o seu médico ou farmacêutico. Última atualização deste resumo: 02-2014.
A informação sobre Mirvaso - tartarato de brimonidina publicada nesta página pode estar desatualizada ou incompleta. Para um uso correto dessas informações, consulte a página Isenção de responsabilidade e informações úteis.