Ingredientes ativos: Amoxicilina, ácido clavulânico
Augmentin 875 mg / 125 mg pó para suspensão oral em saquetas
As bulas de Augmentin estão disponíveis para os tamanhos de embalagem:- Augmentin 875 mg / 125 mg pó para suspensão oral em saquetas
- Augmentin Crianças 400 mg / 57 mg pó para suspensão oral em saquetas
- Augmentin crianças 400 mg / 57 mg / 5 ml pó para suspensão oral
- Augmentin 875 mg / 125 mg comprimidos revestidos por película
- Augmentin 1000 mg / 200 mg pó para solução injetável / perfusão, Augmentin 2000 mg / 200 mg pó para solução injetável
Por que o Augmentin é usado? Para que serve?
Augmentin é um antibiótico que age matando as bactérias que causam infecções. Contém dois medicamentos diferentes chamados amoxicilina e ácido clavulânico. A amoxicilina pertence a um grupo de medicamentos denominados “penicilinas”, cuja atividade pode por vezes ser bloqueada (ou seja, tornada inativa) .O outro componente ativo (ácido clavulânico) impede que isso aconteça.
Augmentin é usado em adultos e crianças para tratar as seguintes infecções:
- infecções de ouvido médio e sinusite
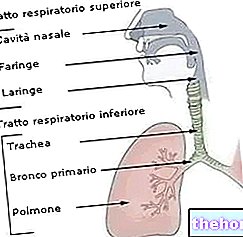
- infecções do trato respiratório
- infecções do trato urinário
- infecções de pele e tecidos moles, incluindo infecções dentárias
- infecções ósseas e articulares
Contra-indicações Quando Augmentin não deve ser usado
Não tome Augmentin:
- se você é alérgico a amoxicilina, ácido clavulânico, penicilina ou qualquer outro componente deste medicamento (listados na seção 6)
- se teve uma reação alérgica grave a qualquer outro antibiótico. Isso pode incluir erupção na pele ou inchaço do rosto ou pescoço
- se alguma vez teve problemas de fígado ou icterícia (pele amarelada) quando tomou um antibiótico.
Precauções de uso O que você precisa saber antes de tomar Augmentin
Tome especial cuidado com Augmentin
Fale com o seu médico, farmacêutico ou enfermeiro antes de tomar este medicamento se:
- tem mononucleose infecciosa
- têm sido tratados para problemas de fígado ou rins
- não urina regularmente.
Se não tem a certeza se alguma das situações anteriores se aplica a si, fale com o seu médico ou farmacêutico antes de tomar Augmentin.
Em alguns casos, seu médico pode fazer uma "pesquisa para avaliar o tipo de bactéria que causou sua infecção. Com base nos resultados, ele pode prescrever uma dosagem diferente de Augmentin ou um medicamento diferente.
Condições que você precisa observar
Augmentin pode piorar algumas condições existentes ou causar efeitos colaterais graves. Estes podem incluir reações alérgicas, convulsões e inflamação do intestino. Deve estar atento a alguns sintomas enquanto estiver a tomar Augmentin para reduzir qualquer risco. Consulte "Condições que você precisa observar.
Exames de sangue e urina
Se estiver a fazer análises ao sangue (como análises aos glóbulos vermelhos ou à função hepática) ou à urina (para glicose), informe o médico ou enfermeiro que está a tomar Augmentin. Isto porque Augmentin pode afetar os resultados deste tipo de exame .
Interações Quais drogas ou alimentos podem alterar o efeito de Augmentin
Informe o seu médico ou farmacêutico se estiver a utilizar ou tiver utilizado recentemente ou se vier a utilizar outros medicamentos, incluindo os disponíveis sem receita médica e produtos à base de plantas.
Se estiver a tomar alopurinol (usado no tratamento da gota) com Augmentin, é muito provável que possa ter uma reação alérgica cutânea.
Se estiver a tomar probenecida (usado para a gota), o seu médico pode decidir alterar a sua dose de Augmentin.
Se estiver a tomar medicamentos (como a varfarina) que ajudam a prevenir a formação de coágulos sanguíneos com Augmentin, pode necessitar de análises sanguíneas adicionais.
Augmentin pode afetar a forma como o metotrexato (um medicamento usado para tratar o câncer ou doenças reumáticas) atua.
Augmentin pode afetar o funcionamento do Micofenolato de Mofetil (um medicamento usado para prevenir a rejeição de órgãos transplantados).
Avisos É importante saber que:
Gravidez, amamentação e fertilidade
Se está grávida ou a amamentar, se pensa estar grávida ou planeia engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Condução e utilização de máquinas
Augmentin pode ter efeitos colaterais e os sintomas podem torná-lo impróprio para dirigir. Não dirija veículos ou use máquinas a menos que se sinta melhor.
Augmentin contém aspartame e maltodextrina
Augmentin contém aspartame (E951), que é uma fonte de fenilalanina. Pode ser prejudicial para pacientes que sofrem de "fenilcetonúria".
Augmentin contém maltodextrina (glicose). Se sabe que tem intolerância a alguns açúcares, consulte o seu médico antes de tomar este medicamento.
Dose, Método e Tempo de Administração Como usar Augmentin: Posologia
Tome este medicamento sempre de acordo com as indicações do seu médico ou farmacêutico. Em caso de dúvida, consulte o seu médico ou farmacêutico.
Adultos e crianças com 40 kg ou mais
875 mg / 125 mg pó para suspensão oral em saquetas
- Dose recomendada - 1 saqueta duas vezes ao dia
- Dose mais alta - 1 sachê três vezes ao dia
Crianças com peso inferior a 40 kg
As saquetas de Augmentin 875 mg / 125 mg não são recomendadas.
Pacientes com problemas renais e hepáticos
- Se você tiver problemas renais, a dose pode ser alterada. O seu médico pode escolher uma dosagem diferente ou um medicamento diferente.
- Se tiver problemas de fígado, pode fazer análises ao sangue mais frequentes para verificar como o seu fígado está a funcionar.
Como tomar Augmentin
- Antes de tomar Augmentin, abra a saqueta e misture o conteúdo com meio copo de água.
- Beba no início da refeição ou imediatamente antes.
- Espace as doses uniformemente ao longo do dia, com pelo menos 4 horas de intervalo. Não tome 2 doses em 1 hora.
- Não tome Augmentin por mais de 2 semanas. Se ainda não se sentir bem, volte ao médico.
Sobredosagem O que fazer se você tiver tomado muito Augmentin
Se você tomar mais Augmentin do que deveria
Se tomar muito Augmentin, os sinais podem incluir dores de estômago (náuseas, vómitos ou diarreia) ou convulsões. Fale com o seu médico o mais rápido possível. Traga a embalagem ou frasco do medicamento para mostrar ao médico.
Se você esquecer de tomar Augmentin
Se você se esquecer de tomar uma dose, tome-a assim que se lembrar. Você não deve tomar a próxima dose muito cedo, mas deve esperar cerca de 4 horas.
Se você parar de tomar Augmentin
Continue a tomar Augmentin até que o tratamento termine, mesmo que se sinta melhor. Você precisa de todas as doses para combater a infecção. Se algumas bactérias sobreviverem, podem fazer com que a infecção volte.
Caso ainda tenha dúvidas sobre a utilização deste medicamento, fale com o seu médico, farmacêutico ou enfermeiro.
Efeitos colaterais Quais são os efeitos colaterais de Augmentin
Como todos os medicamentos, isso pode causar efeitos colaterais, embora nem todas as pessoas os tenham. Os efeitos colaterais que podem ocorrer com este medicamento estão listados abaixo.
Condições que você precisa observar
Reações alérgicas:
- erupções cutâneas
- inflamação dos vasos sanguíneos (vasculite) que pode ser visível como manchas vermelhas ou roxas na pele, mas também pode afetar outras partes do corpo febre, dor nas articulações, glândulas inchadas no pescoço, axilas ou virilha
- inchaço, às vezes da face ou da boca (angioedema), causando dificuldade em respirar
- colapso.
Contacte o seu médico imediatamente se tiver algum destes sintomas. Pare de tomar Augmentin.
Inflamação intestinal
Inflamação do intestino, que causa diarreia aquosa geralmente com sangue e muco, dor de estômago e / ou febre.
Se tiver estes sintomas, contacte o seu médico assim que possível para aconselhamento.
Efeitos colaterais muito comuns
Eles podem afetar mais de 1 em 10 pessoas
- diarreia (em adultos).
Efeitos colaterais comuns
Eles podem afetar até 1 em cada 10 pessoas
- sapinho (candida - uma "infecção por fungos na vagina, boca ou dobras cutâneas)
- náuseas, especialmente ao tomar altas doses
- Ele vomitou
- diarreia (em crianças).
se você sofre disso, tome Augmentin antes das refeições
Efeitos colaterais incomuns
Eles podem afetar até 1 em 100 pessoas
- erupção cutânea, coceira
- erupção cutânea com comichão e aumento (urticária)
- indigestão
- tontura
- dor de cabeça.
Efeitos colaterais incomuns podem aparecer em exames de sangue:
aumento de algumas proteínas (enzimas) produzidas pelo fígado.
Efeitos colaterais raros
Eles podem afetar até 1 em 1000 pessoas
erupção cutânea, que pode aparecer como bolhas e parecer pequenos alvos (mancha escura central cercada por uma "área mais pálida, com um anel escuro ao redor da borda - eritema multiforme)
Se notar algum destes sintomas, contacte o seu médico com urgência
Efeitos colaterais raros podem aparecer em exames de sangue:
- baixo número de células envolvidas na coagulação do sangue
- contagem baixa de glóbulos brancos
Outros efeitos colaterais
Outros efeitos colaterais ocorrem em um número muito limitado de pessoas, mas sua frequência exata não é conhecida.
- Reações alérgicas (veja acima)
- Inflamação do intestino (veja acima)
- Inflamação da membrana protetora que envolve o cérebro (meningite asséptica)
- Reações cutâneas graves:
- erupção cutânea generalizada com bolhas e descamação da pele, particularmente ao redor da boca, nariz, olhos e genitais (síndrome de Stevens-Johnson) e uma forma mais grave, causando descamação extensa da pele (mais de 30% da superfície do corpo - epidérmico tóxico necrólise)
- erupção cutânea vermelha generalizada com pequenas bolhas contendo pus (dermatite esfoliativa bolhosa)
- erupção cutânea, vermelha, com crosta e inchada sob a pele e bolhas (erupção cutânea pustulosa).
Se tiver algum destes sintomas, contacte o seu médico imediatamente.
- inflamação do fígado (hepatite)
- icterícia, causada por um aumento no sangue de bilirrubina (uma substância produzida no fígado) que pode fazer com que a pele e o branco dos olhos pareçam amarelos
- inflamação dos túbulos renais
- o sangue leva mais tempo para coagular
- hiperatividade
- convulsões (em pessoas que tomam altas doses de Augmentin ou que têm problemas renais)
- língua negra que aparece coberta de pelos
- manchas nos dentes (em crianças), geralmente removidas com escovagem.
Efeitos colaterais que podem aparecer em exames de sangue ou urina:
- redução severa no número de glóbulos brancos
- baixo número de glóbulos vermelhos (anemia hemolítica)
- cristais na urina.
Relatório de efeitos colaterais
Se tiver quaisquer efeitos secundários, fale com o seu médico ou farmacêutico, incluindo quaisquer efeitos secundários possíveis não mencionados neste folheto. Você também pode relatar os efeitos colaterais diretamente através do site da Agência Italiana de Medicamentos: http://www.agenziafarmaco.gov.it/it/responsabili.Ao relatar os efeitos colaterais, você pode ajudar a fornecer mais informações sobre a segurança deste medicamento.
Expiração e retenção
Manter fora da vista e do alcance das crianças.
Não utilize este medicamento após o prazo de validade impresso na embalagem. A data de validade refere-se ao último dia do mês.
Armazenar a uma temperatura não superior a 25 ° C.
Armazene no recipiente original para proteger da umidade
Não use este medicamento se a saqueta estiver quebrada ou danificada
Os medicamentos não devem ser eliminados na canalização ou no lixo doméstico. Pergunte ao seu farmacêutico como eliminar os medicamentos que já não utiliza. Isto ajudará a proteger o ambiente.
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
AUGMENTIN
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
AUGMENTIN 875 mg / 125 mg Pó para suspensão oral - saquetas
Cada saqueta contém: amoxicilina tri-hidratada correspondendo a 875 mg de amoxicilina e clavulanato de potássio correspondendo a 125 mg de ácido clavulânico.
Excipentes com efeito conhecido:
contém 24,0 mg de aspartame (E951) por saqueta;
contém maltodextrina (glicose).
AUGMENTIN 400 mg / 57 mg Pó para suspensão oral - saquetas
Cada saqueta contém: amoxicilina tri-hidratada correspondendo a 400 mg de amoxicilina e clavulanato de potássio correspondendo a 57 mg de ácido clavulânico.
Excipentes com efeito conhecido:
contém 11,0 mg de aspartame (E951) por saqueta;
contém maltodextrina (glicose).
Para a lista completa de excipientes, consulte a seção 6.1.
03.0 FORMA FARMACÊUTICA
Pó para suspensão oral.
Pó esbranquiçado.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
Augmentin está indicado para o tratamento das seguintes infecções em adultos e crianças (ver secções 4.2, 4.4 e 5.1):
• Sinusite bacteriana aguda (diagnosticada adequadamente)
• Otite média aguda
• Exacerbações agudas de bronquite crônica (diagnosticada adequadamente)
• Pneumonia adquirida na comunidade
• Cistite
• Pielonefrite
• Infecções da pele e dos tecidos moles, especialmente celulite, mordidas de animais, abscesso dentário grave com celulite disseminada
• Infecções ósseas e articulares, especialmente osteomielite.
As diretrizes oficiais sobre o uso apropriado de agentes antibacterianos devem ser consideradas.
04.2 Posologia e método de administração
As doses são expressas em termos de conteúdo de amoxicilina / ácido clavulânico, exceto quando as doses são definidas em termos de um único componente.
A dose de Augmentin escolhida para o tratamento de cada infecção individual deve levar em consideração:
• Patógenos esperados e sua provável suscetibilidade a agentes antibacterianos (ver seção 4.4)
• Gravidade e local da infecção
• Idade, peso e função renal do paciente, conforme descrito a seguir.
A utilização de formulações alternativas de Augmentin (por exemplo, aquelas que fornecem doses mais elevadas de amoxicilina e / ou diferentes proporções de amoxicilina-ácido clavulânico) deve ser considerada necessária (ver secções 4.4 e 5.1).
Augmentin 875 mg / 125 mg pó para suspensão oral em saquetas
Para adultos e crianças com peso ≥ 40 kg, esta formulação de Augmentin fornece uma dose diária total de 1750 mg de amoxicilina / 250 mg de ácido clavulânico duas vezes ao dia e 2625 mg de amoxicilina / 375 mg de ácido clavulânico para dosagem três vezes ao dia, quando administrado conforme recomendado abaixo.
Augmentin crianças 400 mg / 57 mg pó para suspensão oral em saquetas
Para crianças de peso
A duração da terapia deve ser definida com base na resposta do paciente. Algumas infecções (por exemplo, osteomielite) requerem períodos de tratamento mais longos. O tratamento não deve ser continuado além de 14 dias sem supervisão médica (ver seção 4.4 sobre terapia prolongada).
Adultos e crianças com peso ≥ 40 kg
Doses recomendadas:
• dose padrão: (para todas as indicações) 875 mg / 125 mg duas vezes ao dia.
Dose mais alta (particularmente para infecções como otite média, sinusite, infecções do trato respiratório inferior e infecções do trato urinário): 875 mg / 125 mg três vezes ao dia.
Crianças de peso
Recomenda-se que as crianças sejam tratadas com comprimidos, suspensão ou saquetas pediátricas de Augmentin.
Doses recomendadas:
• de 25 mg / 3,6 mg / kg / dia a 45 mg / 6,4 mg / kg / dia tomados em duas doses divididas;
• até 70 mg / 10 mg / kg / dia em duas doses divididas podem ser considerados para algumas infecções (como otite média, sinusite e infecções do trato respiratório inferior).
Não existem dados clínicos disponíveis para as formulações de Augmentin 7: 1 relacionadas com doses superiores a 45 mg / 6,4 mg por kg por dia em crianças com menos de 2 anos de idade.
Não há dados clínicos disponíveis para as formulações de Augmentin 7: 1 em crianças com menos de 2 meses de idade. Portanto, nenhuma recomendação de dosagem pode ser feita nesta população.
Cidadãos idosos
Nenhum ajuste de dosagem é considerado necessário.
Falência renal
Nenhum ajuste de dose é necessário em pacientes com depuração da creatinina (CrCl) superior a 30 mL / min.
Em pacientes com clearance de creatinina abaixo de 30 mL / min, não há recomendação para o uso de formulações de Augmentin com uma relação amoxicilina-ácido clavulânico de 7: 1, pois não há ajustes posológicos disponíveis.
Insuficiência Hepática
Administre a administração com precaução e monitorize a função hepática em intervalos regulares (ver secções 4.3 e 4.4).
Método de administração
Augmentin é para uso oral.
Administrar no início de uma refeição para minimizar a intolerância gastrointestinal potencial e otimizar a absorção de amoxicilina / ácido clavulânico.
A terapia pode ser iniciada por via parenteral de acordo com o Resumo das Características do Medicamento da formulação IV e continuada com uma preparação oral.
O conteúdo de uma saqueta unidose deve ser dissolvido em meio copo de água antes de ingerir.
04.3 Contra-indicações
Hipersensibilidade à substância ativa, a qualquer penicilina ou a qualquer um dos excipientes mencionados na secção 6.1.
História de reações graves de hipersensibilidade imediata (por exemplo, anafilaxia) a outros agentes beta-lactâmicos (por exemplo, cefalosporinas, carbapenêmicos ou monobactamas).
História de icterícia / insuficiência hepática devido à amoxicilina / ácido clavulânico (ver secção 4.8).
04.4 Advertências especiais e precauções adequadas de uso
Antes de iniciar o tratamento com Augmentin, deve ser realizada uma investigação exaustiva das reações de hipersensibilidade anteriores às penicilinas, cefalosporinas ou outros agentes beta-lactâmicos (ver secções 4.3 e 4.8).
Foram notificadas reações de hipersensibilidade graves e ocasionalmente fatais (reações anafilactóides) em doentes a receber penicilina. Essas reações são mais prováveis de ocorrer em indivíduos com histórico de hipersensibilidade à penicilina e em indivíduos atópicos. Se ocorrer uma reação alérgica, a terapia com amoxicilina / ácido clavulânico deve ser descontinuada e instituída uma terapia alternativa apropriada.
Se for comprovado que uma infecção é causada por um organismo suscetível à amoxicilina, deve-se considerar uma mudança na terapia de amoxicilina / ácido clavulânico para amoxicilina de acordo com as diretrizes oficiais.
Esta formulação de Augmentin não é adequada para uso onde existe um alto risco de que os supostos patógenos tenham sensibilidade ou resistência reduzida a agentes beta-lactâmicos, não mediada por beta-lactamases suscetíveis à inibição pelo ácido clavulânico. Esta formulação não deve ser usada para tratando S. pneumonia resistente à penicilina.
Podem ocorrer convulsões em doentes com compromisso renal ou em doentes a receberem doses elevadas (ver secção 4.8).
A administração de amoxicilina / ácido clavulânico deve ser evitada se houver suspeita de mononucleose infecciosa, pois o uso de amoxicilina foi associado ao aparecimento de erupção cutânea morbiliforme nessa condição.
O uso concomitante de alopurinol durante o tratamento com amoxicilina pode aumentar a probabilidade de reações alérgicas na pele.
O uso prolongado pode ocasionalmente causar o desenvolvimento de organismos resistentes.
O aparecimento de eritema generalizado com pústulas causado por febre durante a fase inicial do tratamento pode ser um sintoma de pustulose exantemática generalizada aguda (PEGA) (ver secção 4.8). Esta reação requer a suspensão de Augmentin e qualquer administração subsequente de amoxicilina é contra-indicada.
Amoxicilina / ácido clavulânico devem ser usados com precaução em doentes com compromisso hepático evidente (ver secções 4.2, 4.3 e 4.8).
Foram notificados acontecimentos hepáticos, particularmente em doentes do sexo masculino e idosos, e podem estar associados a tratamento prolongado. Esses eventos raramente foram relatados em crianças. Em todas as populações, os sinais e sintomas geralmente ocorrem durante ou logo após o tratamento, mas em alguns casos podem ser evidentes apenas várias semanas após a interrupção do tratamento. Esses eventos são geralmente reversíveis. Os eventos hepáticos podem ser graves e, em circunstâncias extremamente raras, ocorreram mortes notificados, que quase sempre ocorreram em doentes com doença grave pré-existente ou que estavam a tomar fármacos conhecidos por terem efeitos hepáticos potenciais (ver secção 4.8).
A colite associada a antibióticos foi notificada com quase todos os agentes antibacterianos e pode ser de gravidade ligeira a potencialmente fatal (ver secção 4.8). Portanto, é importante considerar esse diagnóstico em pacientes que apresentam diarreia durante ou após a administração de qualquer antibiótico. Caso ocorra colite associada a antibióticos, a amoxicilina / ácido clavulânico deve ser descontinuado imediatamente, um médico consultado e iniciada a terapia apropriada. Nessa situação, drogas peristálticas são contra-indicadas.
Durante a terapia prolongada, é aconselhável verificar periodicamente a função sistêmico-orgânica, incluindo a função renal, hepática e hematopoiética.
O prolongamento do tempo de protrombina foi raramente relatado em pacientes recebendo amoxicilina / ácido clavulânico. Deve ser realizada uma monitorização adequada no caso de administração concomitante de anticoagulantes. Pode ser necessário ajustar a dose dos anticoagulantes orais para manter o nível desejado de anticoagulação (ver secções 4.5 e 4.8).
Em doentes com insuficiência renal, a posologia deve ser ajustada de acordo com o grau de insuficiência (ver secção 4.2).
Em pacientes com redução do débito urinário, cristalúria foi observada muito raramente, especialmente com terapia parenteral. Durante a administração de altas doses de amoxicilina, é aconselhável manter a ingestão de líquidos e a produção de urina adequadas para reduzir a possibilidade de cristalúria da amoxicilina. Em doentes com cateteres vesicais, deve ser mantido o controlo regular da permeabilidade (ver secção 4.9).
Durante o tratamento com amoxicilina, métodos enzimáticos com glicose oxidase devem ser usados sempre que testar a presença de glicose na urina, pois podem ocorrer resultados falso-positivos com métodos não enzimáticos.
A presença de ácido clavulânico em Augmentin pode causar uma ligação inespecífica de IgG e albumina pelas membranas dos glóbulos vermelhos, levando a um falso positivo no teste de Coombs.
Resultados de teste positivos foram relatados usando o teste de Platelia da Bio-Rad Laboratories Aspergillus EIA em pacientes recebendo amoxicilina / ácido clavulânico e que, consequentemente, foram encontrados livres de Aspergillus. Com o teste de Platelia da bio-Rad Laboratories Aspergillus EIA, reações cruzadas com não polissacarídeos foram relatadas-Aspergillus e polifuranose. Portanto, os resultados de teste positivos em pacientes recebendo amoxicilina / ácido clavulânico devem ser interpretados com cautela e confirmados por outros métodos de diagnóstico.
Augmentin 875 mg / 125 mg pó para suspensão oral em saquetas contém 24,0 mg de aspartame (E951) por saqueta, que é uma fonte de fenilalanina. Este medicamento deve ser usado com cautela em pacientes com fenilcetonúria.
Augmentin 400 mg / 57 mg pó para suspensão oral em saquetas contém 11,0 mg de aspartame (E951) por saqueta, que é uma fonte de fenilalanina. Este medicamento deve ser usado com cautela em pacientes com fenilcetonúria.
Este medicamento contém maltodextrina (glicose). Os doentes com malabsorção rara de glucose-galactose não devem tomar este medicamento.
04.5 Interações com outros medicamentos e outras formas de interação
Anticoagulantes orais
Os anticoagulantes orais e as penicilinas têm sido amplamente utilizados na prática clínica, sem relatos de interações. Porém, na literatura há casos de razão normalizada internacional aumentada em pacientes mantidos em acenocumarol ou varfarina, aos quais foi prescrito tratamento com amoxicilina. Se a administração concomitante for necessária, o tempo de protrombina ou a razão normalizada internacional devem ser monitorados cuidadosamente em caso de adição ou suspensão da amoxicilina. Além disso, podem ser necessários ajustes de dose de anticoagulantes orais (ver secções 4.4 e 4.8).
Metotrexato
As penicilinas podem reduzir a excreção de metotrexato, causando um aumento potencial da toxicidade.
Probenecida
O uso concomitante de probenecida não é recomendado. Probenecida reduz a secreção tubular renal de amoxicilina. O uso concomitante de probenecida pode resultar em um aumento prolongado dos níveis sanguíneos de amoxicilina, mas não de ácido clavulânico.
Micofenolato de mofetil
Em pacientes tratados com micofenolato de mofetil, após o início do tratamento com amoxicilina e ácido clavulânico oral, houve uma redução da concentração pré-dose do metabólito ativo do ácido micofenólico (AMF) em aproximadamente 50%. -Dose pode não representar com precisão as alterações em exposição geral do MPA. Portanto, normalmente não deve ser necessária uma alteração na dose de micofenolato de mofetil na ausência de sinais clínicos de disfunção do enxerto. No entanto, deve ser realizada uma monitoração clínica cuidadosa durante a combinação e imediatamente após o tratamento com antibióticos.
04.6 Gravidez e lactação
Gravidez
Os estudos em animais não indicam efeitos nefastos diretos ou indiretos no que diz respeito à gravidez, desenvolvimento embrionário / fetal, parto ou desenvolvimento pós-natal (ver secção 5.3). Dados limitados sobre o uso de amoxicilina / ácido clavulânico durante a gravidez em humanos não indicam um risco aumentado de malformações congênitas. Em um único estudo em mulheres com ruptura prematura, pré-termo, da membrana fetal, o tratamento profilático com amoxicilina / ácido clavulânico pode estar associado a um risco aumentado de enterocolite necrosante em neonatos. O uso na gravidez deve ser evitado, a menos que seja considerado essencial pelo médico.
Hora da alimentação
Ambas as substâncias são excretadas no leite materno (não são conhecidos os efeitos do ácido clavulânico no lactente). Como resultado, diarreia e infecções fúngicas da mucosa são possíveis no lactente, de modo que a amamentação deve ser interrompida. Amoxicilina / ácido clavulânico devem ser administrados durante o período de lactação somente após avaliação do risco / benefício pelo médico.
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
Não foram realizados estudos sobre a capacidade de conduzir e utilizar máquinas.No entanto, podem ocorrer efeitos indesejáveis (por exemplo, reações alérgicas, tonturas, convulsões) que podem afetar a capacidade de conduzir e utilizar máquinas (ver secção 4.8).
04.8 Efeitos indesejáveis
As reações adversas (RAMs) mais comumente relatadas são diarreia, náuseas e vômitos.
RAMs de estudos clínicos e investigações pós-comercialização com Augmentin são relatados abaixo de acordo com a classificação MedDRA para Sistemas e Órgãos
A terminologia a seguir foi usada para classificar a frequência dos efeitos indesejáveis.
Muito comum (≥1 / 10)
Comum (≥1 / 100 a
Incomum (≥1 / 1.000 a
Raro (≥1 / 10.000 a
Muito raro (
Desconhecido (não pode ser calculado a partir dos dados disponíveis)
¹ Consulte a seção 4.4
² Ver seção 4.4
³ A náusea está mais frequentemente associada a doses orais mais altas. Se as reações gastrointestinais forem evidentes, podem ser reduzidas tomando Augmentin no início das refeições
4 Incluindo colite pseudomembranosa e colite hemorrágica (ver seção 4.4)
5 Um aumento moderado de AST e / ou ALT foi observado em pacientes tratados com antibióticos da classe de beta-lactâmicos, mas o significado dessas observações é desconhecido.
6 Estes efeitos foram notificados com outras penicilinas e cefalosporinas (ver secção 4.4).
7 Se ocorrer qualquer reação de hipersensibilidade cutânea, o tratamento deve ser interrompido (ver secção 4.4)
8 Ver seção 4.9
9 Ver seção 4.3
10 Ver seção 4.4
11 Mudanças na cor da superfície dentária foram relatadas muito raramente em crianças. Uma boa higiene oral pode ajudar a prevenir a descoloração dos dentes, uma vez que geralmente pode ser eliminada com a escovagem.
Notificação de suspeitas de reações adversas
A notificação de suspeitas de reações adversas que ocorram após a autorização do medicamento é importante, pois permite a monitorização contínua da relação benefício / risco do medicamento. Os profissionais de saúde são solicitados a notificar quaisquer suspeitas de reações adversas através do site da Agência. Agência Italiana de Medicamentos: http : //www.agenziafarmaco.gov.it/it/responsabili
04.9 Overdose
Sintomas e sinais de overdose
Podem ser evidentes sintomas gastrointestinais e perturbações no equilíbrio hídrico e eletrolítico.Tem sido observada cristalúria de amoxicilina, em alguns casos conduzindo a insuficiência renal (ver secção 4.4).
As convulsões podem ocorrer em pacientes com insuficiência renal ou em pacientes recebendo altas doses.
Foi notificada precipitação de amoxicilina em cateteres vesicais, predominantemente após administração intravenosa de grandes doses.O controlo regular da permeabilidade deve ser mantido (ver secção 4.4).
Tratamento de intoxicação
Os sintomas gastrointestinais podem ser tratados sintomaticamente, com atenção ao equilíbrio hídrico e eletrolítico.Amoxicilina / ácido clavulânico podem ser removidos da circulação por hemodiálise.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
Grupo farmacoterapêutico: combinação de penicilinas, incluindo inibidores da beta-lactamase.
Código ATC: J01CR02.
Mecanismo de ação
A amoxicilina, uma penicilina semissintética (antibiótico beta-lactâmico), inibe uma ou mais enzimas (frequentemente referidas como proteínas de ligação à penicilina, PBPs) da via biossintética do peptidoglicano bacteriano, um componente estrutural integral da parede celular bacteriana. do peptidoglicano leva ao enfraquecimento da estrutura, que geralmente é seguido por lise celular e morte bacteriana.
A amoxicilina é suscetível à degradação por beta-lactamases e, portanto, o espectro de atividade da amoxicilina sozinha não inclui organismos que produzem essas enzimas.
O ácido clavulânico é um beta-lactama estruturalmente relacionado às penicilinas. Inativa algumas enzimas beta-lactama, evitando assim a inativação da amoxicilina. O ácido clavulânico sozinho não exerce um efeito antibacteriano clinicamente útil.
Relação PK / PD
O tempo acima da concentração inibitória mínima (T> MIC) é considerado o principal determinante da eficácia da amoxicilina.
Mecanismos de resistência
Os dois principais mecanismos de resistência à amoxicilina / ácido clavulânico são:
• Inativação por beta-lactamases bacterianas que não são inibidas pelo ácido clavulânico, incluindo classes B, C e D.
• Alteração de PBPs, o que reduz a afinidade do agente antibacteriano pelo alvo.
A impermeabilidade das bactérias ou os mecanismos de bomba de efluxo podem causar ou contribuir para a resistência bacteriana, particularmente em bactérias Gram-negativas.
Breakpoints
Os pontos de corte da CIM para amoxicilina / ácido clavulânico são definidos pelo Comitê Europeu de Teste de Suscetibilidade Antimicrobiana (EUCAST).
1 Os valores relatados referem-se às concentrações de amoxicilina. Para efeitos do teste de sensibilidade, a concentração de ácido clavulânico é fixada em 2 mg / l
2 Os valores relatados são para oxacilina
3 valores de ponto de interrupção na tabela são baseados em pontos de interrupção de ampicilina
4 O ponto de quebra de resistência de R> 8 mg / l garante que todos os isolados com mecanismos de resistência sejam relatados como resistentes
5 Os valores de breakpoint na tabela são baseados em breakpoints de benzilpenicilina
§ Suscetibilidade intermediária natural na ausência de mecanismos de resistência adquiridos
£ Todos os estafilococos resistentes à meticilina são resistentes à amoxicilina / ácido clavulânico
1 Streptococcus pneumoniae, que é um microrganismo resistente à penicilina, não deve ser tratado com esta apresentação de amoxicilina / ácido clavulânico (ver secções 4.2 e 4.4).
2 Cepas com suscetibilidade reduzida foram encontradas em muitos países da UE com uma frequência superior a 10%
05.2 Propriedades farmacocinéticas
Absorção
A amoxicilina e o ácido clavulânico se dissociam completamente em solução aquosa em pH fisiológico. Ambos os componentes são rapidamente e bem absorvidos pela via de administração oral. A absorção de amoxicilina / ácido clavulânico é otimizada quando tomada no início de uma refeição. Após a administração oral, a amoxicilina e o ácido clavulânico estão aproximadamente 70% biodisponíveis. Os perfis plasmáticos de ambos os componentes são semelhantes e o tempo para atingir as concentrações plasmáticas máximas (Tmax) em cada caso é de aproximadamente uma hora.
Os resultados farmacocinéticos de estudos separados são apresentados abaixo, nos quais amoxicilina / ácido clavulânico (comprimidos de 875/125 mg administrados duas vezes ao dia) foi administrado em jejum a grupos de voluntários saudáveis.
As concentrações séricas de amoxicilina e ácido clavulânico alcançadas com amoxicilina / ácido clavulânico são semelhantes às produzidas pela administração oral de doses equivalentes de amoxicilina e ácido clavulânico isoladamente.
Distribuição
Cerca de 25% do ácido clavulânico no plasma e 18% da amoxicilina ligam-se às proteínas. O volume aparente de distribuição é de cerca de 0,3-0,4 l / kg para a amoxicilina e cerca de 0,2 l / kg para o ácido clavulânico.
Após administração intravenosa, amoxicilina e ácido clavulânico foram encontrados na vesícula biliar, tecido abdominal, pele, gordura, tecido muscular, fluido sinovial e peritoneal, bile e pus. A amoxicilina não é adequadamente distribuída no líquido cefalorraquidiano.
Os estudos em animais não mostram retenção significativa no tecido de material derivado da droga de qualquer um dos componentes. A amoxicilina, como a maioria das penicilinas, pode ser detectada no leite materno. Podem ser detectados vestígios de ácido clavulânico no leite materno (ver secção 4.6).
A amoxicilina e o ácido clavulânico demonstraram atravessar a barreira placentária (ver secção 4.6).
Biotransformação
A amoxicilina é parcialmente excretada na urina como ácido penicilóico inativo em quantidades equivalentes a até 10-25% da dose inicial. O ácido clavulânico é extensivamente metabolizado em humanos e eliminado na urina e nas fezes, e como dióxido de carbono no exalado ar.
Eliminação
A principal via de eliminação da amoxicilina é por via renal, enquanto para o ácido clavulânico é por meio de mecanismos renais e não renais.
A amoxicilina / ácido clavulânico tem uma meia-vida de eliminação média de aproximadamente uma hora e uma depuração total média de aproximadamente 25 L / hora em indivíduos saudáveis. Aproximadamente 60-70% da amoxicilina e aproximadamente 40-65% do "ácido clavulânico é excretado inalterado na urina durante as primeiras 6 horas após a administração de um único comprimido de 250 mg / 125 mg ou 500 mg / 125 mg de Augmentin. Vários estudos descobriram que a excreção urinária foi de 50-85.% para amoxicilina e entre 27-60% para clavulânico ácido durante um período de 24 horas. No caso do ácido clavulânico, a maior quantidade do fármaco é excretada nas primeiras 2 horas após a administração.
O uso concomitante de probenecida retarda a excreção da amoxicilina, mas não retarda a excreção renal do ácido clavulânico (ver secção 4.5).
Era
A meia-vida de eliminação da amoxicilina é semelhante em crianças com idade aproximada de 3 meses a 2 anos, crianças mais velhas e adultos. Em bebês muito jovens (incluindo aqueles nascidos prematuros) na primeira semana de vida, o intervalo entre as doses não deve exceder duas doses por dia devido à imaturidade do sistema de eliminação renal. Como os pacientes idosos são mais propensos a ter função renal diminuída, pode ser útil monitorar a função renal.
Modelo
Após a administração oral de amoxicilina / ácido clavulânico a indivíduos saudáveis do sexo masculino e feminino, o sexo não tem impacto significativo na farmacocinética da amoxicilina ou do ácido clavulânico.
Falência renal
A depuração sérica total de amoxicilina / ácido clavulânico diminui proporcionalmente com a diminuição da função renal. A redução na depuração da droga é mais pronunciada para amoxicilina do que para ácido clavulânico, pois mais amoxicilina é excretada por rua renal. Portanto, a posologia na insuficiência renal deve prevenir a acumulação excessiva de amoxicilina, mantendo níveis adequados de ácido clavulânico (ver secção 4.2).
Insuficiência Hepática
Os doentes com insuficiência hepática devem ser administrados com precaução e a função hepática monitorizada em intervalos regulares.
05.3 Dados de segurança pré-clínica
Os dados não clínicos não revelam nenhum risco particular para o ser humano, segundo estudos de farmacologia de segurança, genotoxicidade e toxicidade reprodutiva.
Estudos de toxicidade de dose repetida com amoxicilina / ácido clavulânico em cães demonstraram irritação gástrica e vômito e descoloração da língua.
Não foram realizados estudos de carcinogenicidade com Augmentin ou seus componentes.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
Estearato de magnesio
Crospovidona
Sílica coloidal
Aspartame (E951)
Sabor pêssego-limão-morango (contendo maltodextrina)
06.2 Incompatibilidade
Não é relevante.
06.3 Período de validade
2 anos.
06.4 Precauções especiais de armazenamento
Armazene no recipiente original para proteger da umidade
Armazenar a uma temperatura não superior a 25 ° C.
06.5 Natureza da embalagem primária e conteúdo da embalagem
Sachês de 875 mg / 125 mg
Sacos laminados de papel / alumínio / polietileno
Embalagens de 2, 12, 20, 24, 30 ou 500 saquetas
Sachês de 400 mg / 57 mg
Sacos laminados de papel / alumínio / polietileno
Embalagens de 2 ou 12 saquetas
Nem todos os tamanhos de embalagem podem ser comercializados
06.6 Instruções de uso e manuseio
Sem instruções especiais
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
GlaxoSmithKline S.p.A. - Via A. Fleming, 2 - 37135 Verona
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
AUGMENTIN 875 mg / 125 mg: 2 saquetas A.I.C.: 026089324
AUGMENTIN 875 mg / 125 mg: 12 saquetas A.I.C.: 026089108
AUGMENTIN 875 mg / 125 mg: 20 saquetas A.I.C.: 026089351
AUGMENTIN 875 mg / 125 mg: 24 saquetas A.I.C.: 026089336
AUGMENTIN 875 mg / 125 mg: 30 saquetas A.I.C.: 026089363
AUGMENTIN 875 mg / 125 mg: 500 saquetas A.I.C.: 026089348
AUGMENTIN 400 mg / 57 mg: 2 saquetas - crianças A.I.C.: 026089375
AUGMENTIN 400 mg / 57 mg: 12 saquetas - crianças A.I.C.: 026089146
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
AUGMENTIN 875 mg + 125 mg - 12 saquetas
Data da primeira autorização: 27 de abril de 1991
Data da renovação mais recente: 01 de junho de 2010
AUGMENTIN 400 mg + 57 mg - 12 saquetas - crianças
Data da primeira autorização: 18 de março de 2002
Data da renovação mais recente: 01 de junho de 2010
10.0 DATA DE REVISÃO DO TEXTO
16 de julho de 2014
11.0 PARA MEDICAMENTOS DE RÁDIO, PREENCHA OS DADOS NA DOSIMETRIA DE RADIAÇÃO INTERNA
12.0 PARA MEDICAMENTOS DE RÁDIO, INSTRUÇÕES DETALHADAS ADICIONAIS SOBRE PREPARAÇÃO EXEMPORÁRIA E CONTROLE DE QUALIDADE