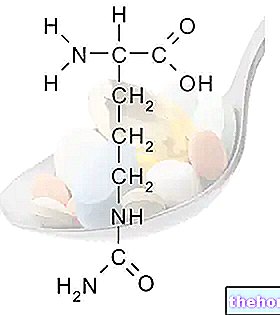
Ingredientes ativos: Norelgestromin / Etinilestradiol
EVRA adesivo transdérmico 203 microgramas de norelgestromina / 24 horas + 33,9 microgramas de etinilestradiol / 24 horas
Por que o Evra é usado? Para que serve?
EVRA contém dois tipos de hormonas sexuais, uma progesterona denominada norelgestromina e um estrogénio denominado etinilestradiol.
Uma vez que contém duas hormonas, EVRA é denominado "contraceptivo hormonal combinado".
É usado para prevenir a gravidez.
Contra-indicações Quando Evra não deve ser usado
Antes de começar a utilizar EVRA, deve ler a informação sobre coágulos sanguíneos na secção 2. É especialmente importante que leia os sintomas de um coágulo sanguíneo (ver secção 2 “Coágulos sanguíneos”).
Não use EVRA:
Não use EVRA se você tiver qualquer uma das condições listadas abaixo. Se você tiver alguma das condições listadas abaixo, entre em contato com seu médico. Seu médico discutirá com você outros métodos anticoncepcionais que podem ser mais adequados para você.
- se tem (ou já teve) um coágulo sanguíneo num vaso sanguíneo da perna (trombose venosa profunda, TVP), pulmão (embolia pulmonar, EP) ou outros órgãos;
- se você sabe que tem um distúrbio que afeta a coagulação do sangue, como deficiência de proteína C, deficiência de proteína S, deficiência de antitrombina-III, fator V de Leiden ou anticorpos antifosfolipídeos;
- se tiver que ser operado ou se vai ficar deitado por muito tempo;
- se você já teve um ataque cardíaco ou derrame;
- se tem (ou já teve) angina de peito (uma doença que causa forte dor no peito e pode ser o primeiro sinal de um ataque cardíaco) ou ataque isquémico transitório (AIT - sintomas de AVC temporário);
- se tiver alguma das seguintes doenças, que podem aumentar o risco de coágulos nas artérias: - diabetes grave com danos nos vasos sanguíneos - tensão arterial muito elevada - nível muito elevado de gordura (colesterol ou triglicéridos) no sangue - uma doença conhecido como hiperhomocisteinemia
- se tem (ou já teve) um tipo de enxaqueca denominado 'enxaqueca com aura';
- se é alérgico a norelgestromina, etinilestradiol ou a qualquer outro componente deste medicamento (listados na seção 6)
- se lhe foi dito que pode ter cancro da mama ou útero, colo do útero ou vagina
- se você já teve tumores ou doença hepática porque seu fígado não está funcionando corretamente
- se você tiver qualquer sangramento vaginal inexplicável. Não use este medicamento se você se encontrar em alguma das situações listadas acima. Se não tiver certeza, pergunte ao seu médico, farmacêutico ou enfermeiro antes de usar este medicamento.
Quando ter cuidado especial com EVRA
Quando você deve consultar um médico?
Contate um médico com urgência
Se notar possíveis sinais de um coágulo sanguíneo que pode indicar que sofre de um coágulo sanguíneo na perna (trombose venosa profunda), um coágulo sanguíneo no pulmão (embolia pulmonar), um ataque cardíaco ou um acidente vascular cerebral (ver seção abaixo "Coágulo de sangue (trombose)").
Precauções de uso O que você precisa saber antes de tomar Evra
Antes de usar este medicamento, você precisará ir ao seu médico para uma consulta.
Informe o seu médico se alguma das seguintes situações se aplicar a você.
Se esta condição aparecer ou piorar enquanto você estiver usando EVRA, você deve informar o seu médico.
- se tem doença de Crohn ou colite ulcerosa (doença intestinal inflamatória crónica); se você tem lúpus eritematoso sistêmico (LES, uma doença que afeta o sistema de defesa natural);
- se tem síndrome hemolítico-urémica (SHU, uma doença da coagulação do sangue que causa insuficiência renal);
- se tem anemia falciforme (uma doença hereditária dos glóbulos vermelhos);
- se tem níveis elevados de gordura no sangue (hipertrigliceridemia), pancreatite (inflamação do pâncreas);
- se tiver que ser operado ou se vai ficar deitado por muito tempo;
- se você acabou de dar à luz, o risco de desenvolver coágulos sanguíneos é maior. Pergunte ao seu médico quanto tempo depois de ter um bebê você pode começar a tomar [nome de fantasia];
- se tem "inflamação das veias sob a pele (tromboflebite superficial);
- se você tem varizes.
COÁGULOS DE SANGUE
Usar um contraceptivo hormonal combinado como EVRA aumenta o risco de desenvolver um coágulo sanguíneo em comparação com o não uso. Em casos raros, um coágulo sanguíneo pode bloquear os vasos sanguíneos e causar problemas graves.
Coágulos sanguíneos podem se desenvolver
- nas veias (denominado "trombose venosa", "tromboembolismo venoso" ou TEV)
- nas artérias (referido como 'trombose arterial', 'tromboembolismo arterial' ou ATE).
A recuperação dos coágulos sanguíneos nem sempre é completa. Raramente, podem ocorrer efeitos graves de longa duração ou, muito raramente, podem ser fatais.
É importante lembrar que o risco geral de um coágulo sanguíneo prejudicial associado a EVRA é baixo.
COMO RECONHECER UM COTO DE SANGUE
Consulte um médico imediatamente se notar algum dos seguintes sinais ou sintomas.
- dor ou sensibilidade na perna que só pode ser sentida ao ficar de pé ou caminhar
- aumento da sensação de calor na perna afetada
- mudança na cor da pele da perna, como ficar pálida, vermelha ou azul
- falta de ar súbita e inexplicável ou respiração rápida;
- tosse súbita sem causa óbvia, possivelmente causando a emissão de sangue;
- dor aguda no peito que pode aumentar com a respiração profunda;
- tontura ou tontura severa;
- batimento cardíaco rápido ou irregular;
- forte dor no estômago
- dor no peito, desconforto, sensação de pressão ou peso
- sensação de aperto ou plenitude no peito, braço ou abaixo do esterno;
- sensação de plenitude, indigestão ou sufocamento;
- desconforto na parte superior do corpo irradiando para as costas, mandíbula, garganta, braços e estômago;
- sudorese, náusea, vômito ou tontura;
- fraqueza extrema, ansiedade ou falta de ar;
- batimentos cardíacos rápidos ou irregulares
- dormência súbita ou fraqueza do rosto, braço ou perna, especialmente em um lado do corpo;
- confusão repentina, dificuldade em falar ou compreender;
- dificuldade repentina de ver em um ou ambos os olhos;
- dificuldade repentina para andar, tontura, perda de equilíbrio ou coordenação;
- enxaqueca súbita, grave ou prolongada sem causa conhecida;
- perda de consciência ou desmaio com ou sem convulsões.
- inchaço e descoloração azul-clara de uma extremidade;
- forte dor de estômago (abdômen agudo)
ENXAGUAMENTOS DE SANGUE EM UMA VEIA
O que pode acontecer se um coágulo de sangue se formar em uma veia?
- O uso de contraceptivos hormonais combinados tem sido associado a um risco aumentado de formação de coágulos sanguíneos nas veias (trombose venosa). No entanto, esses efeitos colaterais são raros. Na maioria dos casos, ocorrem no primeiro ano de uso de um contraceptivo hormonal combinado.
- Se um coágulo de sangue se formar em uma veia da perna ou do pé, pode causar uma trombose venosa profunda (TVP).
- Se um coágulo de sangue sair da perna e se alojar no pulmão, pode causar uma "embolia pulmonar".
- Muito raramente, pode formar-se um coágulo noutro órgão como o olho (trombose da veia retiniana).
Quando é o risco de desenvolver um coágulo sanguíneo em uma veia mais alto?
O risco de desenvolver um coágulo sanguíneo em uma veia é maior durante o primeiro ano de uso de um anticoncepcional hormonal combinado pela primeira vez. O risco pode ser ainda maior se você reiniciar o uso de um contraceptivo hormonal combinado (o mesmo medicamento ou um medicamento diferente) após um intervalo de 4 ou mais semanas.
Após o primeiro ano, o risco diminui, mas é sempre ligeiramente maior do que se você não estivesse usando um anticoncepcional hormonal combinado.
Quando pára de tomar EVRA, o risco de desenvolver um coágulo sanguíneo volta ao normal dentro de algumas semanas.
Qual é o risco de desenvolver um coágulo sanguíneo?
O risco depende do seu risco natural de TEV e do tipo de anticoncepcional hormonal combinado que você está tomando.
O risco geral de desenvolver um coágulo sanguíneo na perna ou no pulmão (TVP ou EP) com EVRA é baixo.
- De cada 10.000 mulheres que não usam nenhum contraceptivo hormonal combinado e que não estão grávidas, cerca de 2 desenvolverão um coágulo sanguíneo em um ano.
- De cada 10.000 mulheres que usam um anticoncepcional hormonal combinado que contém levonorgestrel, noretisterona ou norgestimato, cerca de 5-7 desenvolverão um coágulo sanguíneo em um ano.
- De cada 10.000 mulheres que usam um anticoncepcional hormonal combinado que contém etonorgestrel ou norelgestromina, como EVRA, cerca de 6-12 desenvolverão um coágulo sanguíneo em um ano.
- O risco de formação de um coágulo sanguíneo depende do seu histórico médico
Risco de desenvolver um coágulo sanguíneo em um ano
Mulheres que não estão usando uma combinação de pílula / adesivo / anel de hormônio e que não estão grávidas
Cerca de 2 em 10.000 mulheres
Mulheres que usam pílula anticoncepcional hormonal combinada contendo levonorgestrel, noretisterona ou norgestimato
Cerca de 5 a 7 em cada 10.000 mulheres
Mulheres que usam EVRA
Cerca de 6-12 de 10.000 mulheres
Fatores que aumentam o risco de desenvolver um coágulo sanguíneo em uma veia
O risco de desenvolver um coágulo sanguíneo com EVRA é baixo, mas algumas condições fazem com que ele aumente. Seu risco é maior:
- se tem excesso de peso grave (índice de massa corporal ou IMC superior a 30 kg / m2);
- se um parente próximo teve um coágulo sanguíneo na perna, pulmão ou outro órgão em uma idade jovem (menos de cerca de 50 anos). Neste caso, você pode ter um distúrbio hereditário de coagulação do sangue;
- se for ser operado ou se tiver que ficar deitado por muito tempo devido a uma lesão ou doença, ou se tiver uma perna engessada. Pode ser necessário interromper o tratamento com EVRA algumas semanas antes da cirurgia ou no período em que tem menos mobilidade. Se tiver de parar de tomar EVRA, pergunte ao seu médico quando pode começar a tomá-lo novamente;
- conforme você envelhece (especialmente depois de 35 anos);
- se você deu à luz há menos de algumas semanas.
O risco de desenvolver um coágulo sanguíneo aumenta quanto mais doenças desse tipo você tiver.
As viagens aéreas (com duração> 4 horas) podem aumentar temporariamente o risco de um coágulo sanguíneo, especialmente se você tiver alguns dos outros fatores de risco listados.
É importante que informe o seu médico se algum destes se aplicar a si, mesmo que não tenha a certeza. O seu médico pode decidir que EVRA deve ser interrompido.
Informe o seu médico se alguma das condições acima se alterar durante o uso de EVRA, por exemplo, se um parente próximo tiver trombose sem motivo conhecido ou se você ganhar muito peso.
ENXAGUAMENTOS DE SANGUE EM UMA ARTÉRIA
O que pode acontecer se um coágulo de sangue se formar em uma "artéria"?
Como os coágulos sanguíneos em uma veia, os coágulos em uma artéria podem causar problemas sérios, por exemplo, podem causar um ataque cardíaco ou derrame.
Fatores que aumentam o risco de desenvolver um coágulo sanguíneo em uma artéria
É importante notar que o risco de ataque cardíaco ou acidente vascular cerebral associado ao uso de EVRA é muito baixo, mas pode aumentar:
- com o aumento da idade (acima de 35 anos);
- se você fuma. Ao usar um contraceptivo hormonal combinado como EVRA, você é aconselhado a parar de fumar. Se você não consegue parar de fumar e tem mais de 35 anos, seu médico pode aconselhá-la a usar um tipo diferente de anticoncepcional; se você está acima do peso;
- se você tem pressão alta;
- se um membro da sua família imediata teve um ataque cardíaco ou derrame quando era jovem (menos de 50 anos). Nesse caso, você também pode estar em alto risco de ter um ataque cardíaco ou derrame;
- se você ou um parente próximo tem um alto nível de gordura no sangue (colesterol ou triglicerídeos);
- se sofre de enxaquecas, especialmente enxaquecas com aura;
- se tem problemas cardíacos (defeito na válvula, distúrbio do ritmo cardíaco denominado fibrilhação auricular);
- se você tem diabetes.
Se você tiver mais de uma dessas condições ou se alguma delas for particularmente grave, o risco de desenvolver um coágulo sanguíneo pode ser ainda maior.
Informe o seu médico se alguma das condições acima se alterar enquanto estiver a utilizar EVRA, por exemplo, se começar a fumar, se um familiar próximo tiver trombose sem motivo conhecido ou se ganhar muito peso.
Além disso, fale com o seu médico, farmacêutico ou enfermeiro antes de utilizar EVRA se tiver alguma das seguintes condições, ou se estas condições se desenvolverem ou piorarem: se pensa que está grávida
- se você tem dores de cabeça que pioram ou vêm com mais frequência
- se você pesa 90 kg ou mais
- se você tem pressão alta ou pressão arterial que tende a subir
- se você tem doença da vesícula biliar, incluindo cálculos biliares ou inflamação da vesícula biliar
- se você tem uma doença do sangue chamada "porfiria"
- se você tem uma doença do sistema nervoso que causa movimentos corporais repentinos, chamada de "coréia de Sydenham"
- se você teve uma "erupção cutânea com bolhas (chamada de" herpes gestacional ") durante a gravidez
- se você tem perda auditiva
- se você tem diabetes
- se você tem depressão
- se você tem epilepsia ou qualquer outra condição que pode causar convulsões
- se tem problemas de fígado, incluindo amarelecimento da pele e da parte branca dos olhos (icterícia)
- se tem ou teve "manchas de gravidez". Estas são manchas amarelo-acastanhadas, especialmente na face (chamadas de "cloasma"). Essas manchas podem não desaparecer completamente após a interrupção do EVRA. Proteja sua pele da luz solar ou da radiação ultravioleta. Isso pode ajudar a evitar que essas manchas apareçam ou piorem
- se tiver problemas renais.
Se não tem a certeza se alguma das condições anteriores se aplica a si, fale com o seu médico ou farmacêutico antes de utilizar EVRA.
Doenças sexualmente transmissíveis
Este medicamento não o protegerá da infecção por HIV (AIDS) ou de qualquer outra doença sexualmente transmissível. Incluem clamídia, herpes genital, verrugas acuminadas, gonorréia, hepatite B, sífilis. Sempre use preservativos para se proteger contra essas doenças.
Testes clínicos
Se você precisar fazer um teste de sangue ou urina, informe o médico ou a pessoa que coleta a amostra biológica que você está usando EVRA, pois os anticoncepcionais hormonais podem afetar alguns resultados do teste.
Crianças e adolescentes
EVRA não foi estudado em crianças e adolescentes com menos de 18 anos de idade. EVRA não deve ser utilizado em crianças e adolescentes que ainda não tiveram a primeira menstruação.
Interações Quais drogas ou alimentos podem alterar o efeito do Evra
Informe o seu médico ou farmacêutico se estiver a tomar, tiver tomado recentemente ou se vier a utilizar outros medicamentos.
Alguns medicamentos e remédios à base de ervas podem afetar a eficácia de EVRA. Neste caso, você pode engravidar.
Informe o seu médico se você estiver tomando:
- alguns medicamentos antirretrovirais usados para tratar o HIV / AIDS (como nelfinavir, ritonavir, nevirapina, efavirenz)
- medicamentos usados para tratar infecções (como rifampicina, rifabutina e griseofulvina, penicilinas e tetraciclinas)
- medicamentos para tratar convulsões (alguns exemplos são topiramato, fenorbarbital, fenitoína, carbamazepina, primidona, oxicarbazepina, felbamato, acetato de eslicarbazepina e rufinamida)
- fosaprepitant (um medicamento para tratar náuseas)
- bosentan (um medicamento para tratar a hipertensão nas artérias pulmonares)
- Erva de São João (erva de São João) (um remédio à base de ervas usado para a depressão). A erva de São João não deve ser ingerida ao usar EVRA.
Se você tomar algum desses medicamentos, também deve usar um método contraceptivo adicional (por exemplo, preservativo, diafragma ou espuma espermicida). O efeito de interferência de alguns destes medicamentos pode durar até 28 dias após a interrupção de tomá-los.Pergunte ao seu médico ou farmacêutico sobre outro método contraceptivo se você usar EVRA concomitantemente com qualquer um dos medicamentos acima.
EVRA pode diminuir o efeito de alguns medicamentos, como:
- medicamentos contendo ciclosporina
- lamotrigina, um medicamento usado para epilepsia - pode aumentar o risco de ataques (convulsões)
O seu médico pode necessitar de ajustar a dose de outros medicamentos Consulte o seu médico ou farmacêutico antes de tomar qualquer medicamento.
Avisos É importante saber que:
Gravidez e amamentação
- Não use este medicamento se estiver grávida ou pensar que está grávida
- Pare de usar este medicamento imediatamente se ficar grávida
- Não use este medicamento se estiver amamentando ou planeja amamentar
Se está grávida ou planeia engravidar, consulte o seu médico ou farmacêutico antes de tomar este medicamento.
Condução e utilização de máquinas
Você pode dirigir e operar máquinas enquanto usa este medicamento.
Riscos associados ao uso de anticoncepcionais hormonais combinados
As informações a seguir são baseadas nas informações sobre pílulas anticoncepcionais combinadas. Uma vez que o adesivo transdérmico EVRA contém hormônios semelhantes aos usados nas pílulas anticoncepcionais combinadas, é provável que também tenha os mesmos riscos. Todas as pílulas anticoncepcionais combinadas apresentam riscos que podem causar invalidez ou morte.
Um adesivo transdérmico como EVRA não provou ser mais seguro do que uma pílula anticoncepcional hormonal combinada administrada por via oral.
Contraceptivos hormonais combinados e câncer
Câncer do colo do útero
O câncer cervical ocorre com mais frequência em mulheres que tomam anticoncepcionais hormonais combinados. No entanto, isso pode ser devido a outras causas, incluindo doenças sexualmente transmissíveis.
Câncer de mama
Observou-se que mulheres que usam anticoncepcionais hormonais combinados desenvolvem câncer de mama com mais frequência do que aquelas que não o fazem. No entanto, é possível que o anticoncepcional hormonal combinado não seja a causa disso. Pode ser que as mulheres que tomam anticoncepcionais hormonais combinados consultem o médico com mais frequência. Isso pode significar que há mais chances de diagnosticar câncer de mama. O risco aumentado de câncer de mama diminui gradualmente quando o uso de anticoncepcionais hormonais combinados é interrompido. Após dez anos, as chances de câncer de mama são iguais às de mulheres que nunca usaram anticoncepcionais hormonais combinados.
Câncer de fígado
Raramente, casos não cancerosos e, ainda mais raramente, casos cancerosos de tumores hepáticos foram relatados em mulheres que usam anticoncepcionais hormonais combinados. Esse tipo de tumor pode causar hemorragia interna, com fortes dores abdominais. Se isso acontecer, entre em contato com seu médico imediatamente.
Dose, método e tempo de administração Como usar o Evra: Posologia
Use este medicamento sempre de acordo com as indicações do seu médico ou farmacêutico.
Se ela não fizer isso, ela pode correr um risco maior de engravidar
Se você não tem certeza, consulte o seu médico ou farmacêutico
Guarde outros anticoncepcionais não hormonais (por exemplo, preservativo, espuma ou esponja espermicida) como método de reserva, caso você cometa um erro ao usar o adesivo.
Quantos patches usar
Semanas 1, 2 e 3: aplique apenas um adesivo e guarde-o por exatamente sete dias
semana 4: não use o adesivo esta semana.
Se você não usou um anticoncepcional hormonal durante o ciclo anterior
Você pode iniciar este medicamento no primeiro dia do seu próximo ciclo.
Se já se passaram um ou mais dias desde o início da menstruação, converse com seu médico sobre o uso temporário de um anticoncepcional não hormonal.
Se você mudar da pílula anticoncepcional oral para EVRA
Se você estiver mudando de uma pílula anticoncepcional oral para EVRA:
- espere seu período
- aplique o primeiro adesivo durante as primeiras 24 horas da menstruação.
Se o adesivo for aplicado após o dia 1 do seu período:
Você também usa um anticoncepcional não hormonal até o Dia 8, quando você troca o adesivo.Se a sua menstruação não aparecer nos 5 dias após a ingestão da última pílula anticoncepcional, converse com seu médico antes de começar a usar este medicamento.
Se você mudar da pílula, implante ou método injetável somente de progestágeno para EVRA
- Você pode iniciar este medicamento em qualquer dia após interromper a administração da pílula só de progestagênio ou no dia em que o implante for removido ou no dia programado para a próxima injeção.
- Aplique o adesivo no primeiro dia após parar de usar a pílula só de progestagênio, ou após a remoção do implante ou no dia da próxima injeção.
- Use também um anticoncepcional não hormonal até o dia 8, quando você troca o adesivo.
Após um aborto espontâneo ou induzido antes das 20 semanas de gravidez
- Converse com seu medico
- Você pode começar este medicamento imediatamente
Se um ou mais dias se passaram desde o aborto espontâneo ou induzido quando você começou este medicamento, converse com seu médico sobre o uso temporário de um anticoncepcional não hormonal.
Após um aborto espontâneo ou induzido após 20 semanas de gravidez
- Converse com seu medico
- Você pode decidir iniciar este medicamento no dia 21 após o aborto ou aborto induzido, ou no primeiro dia da menstruação, o que ocorrer primeiro.
Depois de dar à luz
- Converse com seu medico
- Se você teve um bebê e não está amamentando, não deve usar este medicamento por quatro semanas após o parto
- Se começar mais de quatro semanas após o parto, use outro contraceptivo não hormonal além deste medicamento durante os primeiros 7 dias
- Se você fez sexo depois de ter um bebê, aguarde seu primeiro período ou consulte o seu médico para se certificar de que não está grávida antes de iniciar este medicamento
Se você está amamentando
- Converse com seu medico
- Não use este medicamento se estiver amamentando (ver seção 2 gravidez e aleitamento).
Informações importantes a serem consideradas ao usar o patch
- Você muda EVRA no mesmo dia da semana. O adesivo é formulado para funcionar ao longo de 7 dias
- Nunca deixe passar mais de 7 dias consecutivos sem usar o adesivo
- Use apenas um patch de cada vez
- Não corte ou adultere o patch de forma alguma
- Evite aplicar o adesivo na pele vermelha, irritada ou com cortes
- O adesivo deve aderir completamente à pele para funcionar corretamente
- Pressione o remendo com firmeza até que suas bordas adiram bem
- Não use cremes, óleos, loções, talco ou maquiagem na pele onde está aplicando o adesivo ou próximo ao adesivo aplicado. Isso, de fato, pode levar ao desprendimento do patch
- Não aplique um novo adesivo na mesma área da pele que o adesivo que acabou de retirar. Caso contrário, haverá uma chance maior de irritação.
- Verifique todos os dias para se certificar de que o sistema transdérmico não saiu.
- Não pare de usar os adesivos, mesmo que faça sexo raramente.
COMO USAR O PATCH
Se você estiver usando EVRA pela primeira vez, espere até a menstruação.
- Aplique o primeiro adesivo durante as primeiras 24 horas do seu período
- Se o adesivo for aplicado após o dia 1 da menstruação, você precisará usar um método contraceptivo não hormonal até o dia 8, quando você troca o adesivo.
- O dia em que aplicar o primeiro adesivo será o dia 1. O "Dia de troca do adesivo" será no mesmo dia, todas as semanas.
Escolha um local em seu corpo para aplicar o adesivo.
- Sempre aplique o adesivo na pele limpa, seca e sem pelos
- Aplique o adesivo nas nádegas, abdômen, parte superior do braço ou parte superior das costas, onde não será esfregado por roupas apertadas.
- Nunca coloque o adesivo em seus seios.
Usando os dedos, abra a saqueta de alumínio.
- Abra-o rasgando ao longo da borda (não use tesouras)
- Agora pegue um canto do adesivo com firmeza e remova-o com cuidado do sachê do adesivo
- Às vezes, os adesivos podem aderir ao interior do sachê: tenha cuidado para não descascar acidentalmente a película aderente ao remover o adesivo
- Agora, conforme mostrado na figura, retire metade da película protetora transparente.
- Evite tocar na superfície adesiva.
- Coloque o adesivo na pele.
- Só então você retira a outra metade da película protetora
- Pressione com força o patch com a palma da sua mão por 10 segundos
- Certifique-se de que as bordas se encaixam perfeitamente.
Você usa o adesivo por 7 dias (uma semana).
- No "Dia de troca do adesivo", que é o dia 8, remova o adesivo usado
- Aplique um novo patch imediatamente.
- No dia 15 (semana 3) remova o adesivo usado
- Aplique um novo adesivo.
Ao todo, são três semanas em que os adesivos são usados.
Para evitar irritação, não aplique o novo adesivo exatamente no mesmo local do adesivo anterior.
Não use nenhum adesivo na semana 4 (dia 22 ao dia 28).
- Você deve ter seu período durante este tempo
- Durante esta semana, você estará protegida da gravidez, mas apenas se começar a usar o próximo adesivo a tempo.
Para iniciar o próximo ciclo de quatro semanas
- Aplique um novo adesivo no seu "dia de troca de adesivo" normal, que é um dia após o dia 28
- Não importa em que dia seu período começa ou termina.
Se quiser alterar o "Dia de troca do adesivo" para outro dia da semana, fale com o seu médico.
Você precisa completar seu ciclo atual e remover o terceiro adesivo no dia correto. Durante a semana 4, você pode escolher um novo "Dia de troca do adesivo" e aplicar o primeiro adesivo desse dia. Você não deve passar mais de 7 dias consecutivos sem usar o adesivo.
Se quiser atrasar a menstruação, aplique também um adesivo no início da semana 4 (dia 22). Você pode ter manchas ou sangramento intermenstrual. Não use mais de 6 adesivos consecutivos (portanto, por não mais de 6 semanas). você usou 6 adesivos consecutivos (ou seja, por 6 semanas consecutivas), não aplique o adesivo da semana 7. Após 7 dias sem o adesivo, aplique um novo adesivo e reinicie o ciclo considerando-o como o dia 1. Consulte o seu médico antes de decidir adiar seu período.
Atividades diárias durante o uso do patch
- Atividades normais, como tomar banho, ducha, sauna ou exercícios, não devem afetar a eficácia do adesivo.
- O patch é formulado para permanecer no lugar durante esses tipos de atividades
- No entanto, é aconselhável verificar se o patch não saiu depois de participar dessas atividades
Se você precisar aplicar o adesivo em um novo local em um dia diferente do seu "Dia de troca de adesivo"
Se o adesivo que você está usando se tornar desconfortável ou causar irritação:
- você pode retirá-lo e substituí-lo por um novo adesivo aplicado em um lugar diferente, até o próximo "Dia de troca de adesivo"
- você só precisa usar um patch por vez.
Se você achar difícil se lembrar de trocar o patch EVRA
Fale com o seu médico, farmacêutico ou profissional de saúde sobre como pode facilitar a substituição dos adesivos ou sobre a utilização de outro método contraceptivo.
Se o adesivo está descascando ou caiu por menos de um dia (até 24 horas):
tente reaplicá-lo imediatamente ou aplique um novo adesivo imediatamente, nenhum método anticoncepcional adicional é necessário
- não adere mais
- ele se ligou a si mesmo ou a outra superfície
- outros materiais aderiram a ele
- é a segunda vez que ele se solta ou se solta.
Por mais de um dia (24 horas ou mais) ou se você não tiver certeza de quanto tempo:
- iniciar um novo ciclo de quatro semanas imediatamente aplicando um novo adesivo
- agora terá um novo Dia 1 e um novo "Dia de troca de adesivo"
- durante a primeira semana do seu novo ciclo, você também precisará usar um método contraceptivo não hormonal
Você pode engravidar se não seguir estas instruções.
Se você se esquecer de substituir o adesivo transdérmico
No início de qualquer ciclo de aplicação de patch (Semana 1 (Dia 1)):
Se se esquecer de aplicar o adesivo, pode correr um risco particularmente elevado de engravidar.
- Em seguida, você precisará usar um método anticoncepcional não hormonal por mais uma semana
- Aplique o primeiro adesivo do novo ciclo assim que se lembrar
- Agora você terá um novo "Dia de troca de adesivo" e um novo dia 1.
No meio do ciclo de aplicação do patch (semana 2 ou semana 3):
Se você se esquecer de substituir o adesivo por um ou dois dias (até 48 horas):
- aplique um novo patch assim que se lembrar
- aplique o próximo adesivo no seu "Dia de troca de adesivo" regular. Nenhum contraceptivo adicional é necessário.
Por mais de dois dias (48 horas ou mais):
- se você se esquecer de substituir o adesivo por mais de 2 dias, você pode ficar grávida
- comece um novo ciclo de quatro semanas assim que se lembrar, a aplicação de um novo adesivo agora terá um "dia de troca de adesivo" diferente e um novo dia 1
- você também precisará usar um método contraceptivo adicional durante a primeira semana do seu novo ciclo.
No final do ciclo de aplicação do patch (semana 4):
Se você se esquecer de remover o patch:
- remova o adesivo assim que se lembrar
- você inicia o próximo ciclo no seu "Dia de troca de adesivo" normal, que é um dia após o dia 28.
Nenhum contraceptivo adicional é necessário.
Se você não tem sangramento ou sangramento irregular com EVRA
Este medicamento pode causar sangramento vaginal inesperado ou manchas durante as semanas em que você estiver usando o adesivo
- Isso geralmente termina após os primeiros ciclos
- Erros no uso dos adesivos podem causar manchas ou sangramento leve
- Continue a usar este medicamento e se a hemorragia durar mais do que os três primeiros ciclos, fale com o seu médico ou farmacêutico.
Se a sua menstruação não aparecer durante a semana em que não está usando EVRA (semana 4), você deve continuar a aplicar um novo adesivo no seu "Dia de troca de adesivo" normal.
- Se você estiver usando este medicamento corretamente e não tiver menstruação, isso não significa necessariamente que esteja grávida
- No entanto, se a sua menstruação não ocorrer durante dois ciclos consecutivos, fale com o seu médico ou farmacêutico, pois pode estar grávida.
Overdose O que fazer se você tiver tomado muito Evra
Se você usar mais EVRA do que deveria (mais de um patch EVRA por vez)
Remova os adesivos e entre em contato com o seu médico imediatamente. Usar muitos patches pode causar:
- mal-estar (náuseas, vômitos)
- sangramento vaginal.
Se você parar de tomar EVRA
Você pode ter um período de luz irregular ou nenhum. Isso geralmente acontece durante os primeiros 3 meses, especialmente se seus períodos não eram regulares antes de começar a usar este medicamento.
Caso ainda tenha dúvidas sobre a utilização deste medicamento, fale com o seu médico, farmacêutico ou enfermeiro.
Efeitos colaterais Quais são os efeitos colaterais do Evra
Como todos os medicamentos, EVRA pode causar efeitos secundários, embora nem todas as pessoas os tenham. Se tiver quaisquer efeitos secundários, especialmente se forem graves ou persistentes, ou se houver qualquer alteração na sua saúde que pensa poder ser devido a EVRA, informe o seu médico.
Um risco aumentado de desenvolver coágulos sanguíneos nas veias (tromboembolismo venoso (TEV)) ou coágulos sanguíneos nas artérias (tromboembolismo arterial (ATE)) está presente em todas as mulheres que tomam contraceptivos hormonais combinados. Para obter informações mais detalhadas sobre os diferentes riscos de "tomar anticoncepcionais hormonais combinados, consulte a seção 2" O que você precisa saber antes de usar EVRA ".
Efeitos colaterais muito comuns (afetam mais de 1 em cada 10 mulheres):
- Dor de cabeça
- Náusea
- Desconforto na mama.
Efeitos colaterais comuns (afetam menos de 1 em cada 10 mulheres):
- Infecções vaginais por fungos, às vezes chamadas de candidíase
- Transtornos de humor, como depressão, alterações de humor, alterações de humor, ansiedade, choro
- Tontura
- Enxaqueca
- Dor de estômago ou inchaço do estômago
- Vômito ou diarreia
- Acne, erupção cutânea, coceira ou irritação da pele
- Espasmos musculares
- Problemas mamários, como dor, aumento ou caroços nos seios
- Mudanças nas características de sangramento menstrual, cólicas uterinas, períodos dolorosos, corrimento vaginal
- Reações no local de aplicação, como vermelhidão, irritação, coceira ou erupção na pele. Cansaço ou mal-estar geral
- Ganho de peso.
Efeitos colaterais incomuns (afetam menos de 1 em 100 mulheres):
- Reação alérgica, urticária
- Inchaço devido à retenção de água
- Níveis elevados de gordura no sangue (como colesterol ou triglicerídeos)
- Distúrbios do sono (insônia)
- Perda de libido
- Eczema, vermelhidão da pele
- Produção anormal de leite materno
- Síndrome pré-menstrual
- Secura vaginal
- Outras reações no local de aplicação do adesivo
- Inchaço
- Pressão alta ou aumento da pressão arterial
- Aumento do apetite
- Perda de cabelo
- Sensibilidade à luz solar.
Efeitos colaterais raros (afetam menos de 1 em 1.000 mulheres):
- coágulos sanguíneos prejudiciais em uma veia ou artéria, por exemplo: em uma perna ou pé (TVP)
- em um pulmão (PE)
- ataque cardíaco
- golpe
- mini-AVC ou sintomas temporários semelhantes aos de AVC, conhecidos como ataque isquêmico transitório (AIT)
- coágulos sanguíneos no fígado, estômago / intestinos, rins ou olhos.
- A chance de desenvolver um coágulo sanguíneo pode ser maior se você tiver qualquer outra condição que aumente esse risco
- Câncer de mama, colo do útero ou fígado
- Problemas causados pelo contato do adesivo com a pele, como erupção na pele com bolhas ou úlceras
- Tumores de mama ou fígado não cancerosos (benignos)
- Miomas uterinos (útero)
- Raiva ou um sentimento de frustração
- Aumento da libido
- Alteração de gosto
- Problemas ao usar lentes de contato
- Aumento repentino e acentuado da pressão arterial (crise hipertensiva)
- Inflamação da vesícula biliar ou cólon
- Células alteradas no colo do útero
- Manchas acastanhadas ou manchas no rosto
- Cálculos biliares ou bloqueio do ducto biliar
- Amarelecimento da pele e do branco dos olhos
- Níveis anormais de açúcar no sangue ou insulina
- Inchaço da face, boca, garganta ou língua
- Erupção cutânea com nódulos vermelhos dolorosos nas canelas e nas pernas
- Coceira
- Pele escamosa, escamosa, coceira e vermelha
- Amamentação suprimida
- Corrimento vaginal
- Retenção de fluidos nas pernas
- Retenção de fluidos
- Inchaço dos braços, mãos, pernas ou pés.
Se você tem dor de estômago
- A quantidade de hormônios liberados por EVRA não deve ser afetada por vômitos ou diarreia
- Você não precisa usar métodos contraceptivos adicionais se tiver problemas de estômago.
Você pode sentir manchas, sangramento leve, desconforto mamário ou mal-estar durante os primeiros 3 ciclos. O problema geralmente desaparece, mas se persistir, consulte o seu médico ou farmacêutico.
Se tiver quaisquer efeitos secundários, fale com o seu médico, farmacêutico ou enfermeiro.Isto inclui quaisquer possíveis efeitos secundários não mencionados neste folheto.
Expiração e retenção
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após o prazo de validade impresso na embalagem após “EXP”. A data de validade refere-se ao último dia desse mês.
Armazene na embalagem original para proteger os adesivos da luz e da umidade.
Não refrigerar ou congelar.
Os adesivos usados ainda contêm hormônios ativos. Para proteger o meio ambiente, eles devem ser descartados com cuidado. Para descartar o adesivo usado, você deve:
- levante a etiqueta a ser usada para descarte localizada na parte externa do sachê
- coloque o adesivo usado dentro da etiqueta de descarte, abra de forma que a superfície pegajosa cubra a área sombreada
- feche a etiqueta selando o adesivo usado dentro e descarte-o fora do alcance das crianças.
Não deite quaisquer medicamentos na canalização ou no lixo doméstico. Pergunte ao seu farmacêutico como deitar fora os medicamentos que já não utiliza. Isto ajudará a proteger o ambiente.
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
EVRA TRANSDERMAL PATCH 203 mcg / 24 HORAS + 33,9 mcg / 24 HORAS
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Cada adesivo transdérmico de 20 cm2 contém 6 mg de norelgestromina (NGMN) e 600 mcg de etinilestradiol (EE).
Cada adesivo transdérmico libera uma média de 203 mcg de NGMN e 33,9 mcg de EE em 24 horas. A exposição ao medicamento é mais apropriadamente caracterizada pelo perfil farmacocinético (ver secção 5.2).
Para a lista completa de excipientes, consulte a seção 6.1.
03.0 FORMA FARMACÊUTICA
Sistema transdérmico.
Sistema transdérmico de matriz fino, composto por três camadas.
A parte externa da camada de reforço é de cor bege e possui a inscrição "EVRA" termicamente impressa.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
Contracepção feminina.
EVRA destina-se a mulheres em idade fértil. Sua eficácia e segurança foram estabelecidas em mulheres com idade entre 18 e 45 anos.
A decisão de prescrever EVRA deve ter em consideração os fatores de risco individuais atuais da mulher, particularmente aqueles relacionados com tromboembolismo venoso (VTE) e a comparação entre o risco de VTE associado a EVRA e o associado a outros CHCs (ver secções 4.3 e 4.4).
04.2 Posologia e método de administração
Dosagem
Para atingir a eficácia contraceptiva máxima, informe as pacientes de que elas precisarão usar EVRA exatamente como prescrito. Para obter instruções sobre como começar, consulte "Primeiros passos com EVRA" abaixo.
Apenas um adesivo transdérmico deve ser usado por vez.
Cada adesivo transdérmico usado deve ser removido e imediatamente substituído por um novo no mesmo dia da semana (dia da mudança) no dia 8 e no dia 15 do ciclo. Você pode trocar o adesivo transdérmico a qualquer hora do dia no dia da troca. Na quarta semana, começando no dia 22 do ciclo, o adesivo transdérmico não é usado.
Um novo ciclo anticoncepcional começa um dia após a semana sem um adesivo transdérmico; o próximo adesivo transdérmico EVRA também deve ser aplicado se não houver sangramento ou se o sangramento ainda não tiver parado.
Você nunca deve deixar mais de 7 dias sem um adesivo transdérmico entre os ciclos. Se passarem mais de 7 dias, a usuária pode não estar protegida da gravidez. Neste caso, um contraceptivo não hormonal deve ser usado concomitantemente por 7 dias. O risco de ovulação aumenta a cada dia além do período recomendado sem anticoncepcionais. No caso de relações sexuais durante um intervalo tão prolongado sem adesivo transdérmico, deve ser considerada a possibilidade de gravidez.
Populações especiais
Peso corporal igual ou superior a 90 kg
A eficácia contraceptiva pode ser reduzida em mulheres com peso igual ou superior a 90 kg.
Falência renal
EVRA não foi estudado em mulheres com insuficiência renal. Nenhum ajuste de dose é necessário, mas como a literatura médica sugere que a fração livre de etinilestradiol é maior, EVRA deve ser administrado a essa população cuidadosamente monitorada.
Insuficiência Hepática
EVRA não foi estudado em mulheres com insuficiência hepática. EVRA está contra-indicado em mulheres com compromisso hepático (ver secção 4.3).
Mulheres pós-menopáusicas
EVRA não é indicado em mulheres na pós-menopausa e não deve ser usado como terapia de reposição hormonal.
População pediátrica
A segurança e eficácia não foram estabelecidas em adolescentes com idade inferior a 18 anos. Não existe utilização relevante de EVRA em crianças e adolescentes antes da menarca.
Método de administração
EVRA deve ser aplicado em pele limpa, seca, sem pêlos, intacta e saudável, nas nádegas, abdômen, braço ou tronco, em um local onde não será friccionado por roupas apertadas. EVRA não deve ser aplicado em seios ou pele vermelha, irritada ou com cortes Cada adesivo transdérmico EVRA consecutivo deve ser aplicado numa parte diferente da pele para evitar irritação, mas pode permanecer na mesma área anatómica.
Pressione firmemente o adesivo transdérmico até que as bordas adiram bem.
Para evitar a interferência com as propriedades adesivas do adesivo transdérmico, nenhum make-up, creme, loções, talco ou outros produtos tópicos devem ser aplicados na área da pele onde o adesivo transdérmico é aplicado ou onde se destina a ser aplicado .
Recomenda-se que os usuários inspecionem visualmente o adesivo transdérmico todos os dias para garantir a adesão adequada.
O adesivo transdérmico EVRA não deve ser cortado, danificado ou alterado de forma alguma, pois pode comprometer a sua eficácia contraceptiva.
Os adesivos transdérmicos usados devem ser descartados cuidadosamente de acordo com as instruções fornecidas na seção 6.6.
Como iniciar EVRA
Se nenhum contraceptivo hormonal foi usado no ciclo anterior
A contracepção com EVRA começa no primeiro dia da menstruação. Um único adesivo transdérmico é aplicado e usado por uma semana inteira (7 dias). O dia em que o primeiro adesivo transdérmico é aplicado (dia 1 / dia de início) determina os próximos dias de substituição. O dia de troca do adesivo transdérmico será o mesmo dia da semana (dia 8, 15, 22 do ciclo e dia 1 do próximo ciclo). O adesivo transdérmico não é usado na quarta semana, começando no dia 22 do ciclo.
Apenas para o primeiro ciclo de tratamento, se a terapia do ciclo 1 começar após o primeiro dia de menstruação, um contraceptivo não hormonal deve ser usado simultaneamente durante os primeiros 7 dias consecutivos.
Se você mudar de um anticoncepcional oral combinado
O tratamento com EVRA deve começar no primeiro dia da hemorragia de privação. Se não houver hemorragia de privação nos 5 dias após a toma do último comprimido ativo (contendo hormonas), a possibilidade de gravidez deve ser excluída antes de iniciar o tratamento. é iniciado após o primeiro dia de hemorragia de privação, devem ser utilizados meios contracetivos não hormonais concomitantemente com EVRA durante 7 dias.
Se mais de 7 dias se passaram desde que tomou a última pílula anticoncepcional oral ativa, é possível que a mulher tenha ovulado. Portanto, informe-o de que deve consultar o seu médico antes de iniciar o tratamento com EVRA. Se a mulher teve relações sexuais durante esse intervalo prolongado sem pílula, a possibilidade de gravidez deve ser considerada.
Se você mudar de um método somente de progestagênio
O usuário pode mudar da pílula somente de progestagênio em qualquer dia (desde o dia da remoção, no caso de um implante, e a partir do dia em que a injeção deveria ser feita, no caso de um método anticoncepcional injetável), porém nos primeiros 7 dias você precisará usar um método de barreira adicional de contracepção.
Após aborto induzido ou espontâneo
Após um aborto induzido ou espontâneo que ocorreu antes de 20 semanas de gestação, a usuária pode começar a usar EVRA imediatamente. Se EVRA for iniciado imediatamente, não há necessidade de medidas anticoncepcionais adicionais. Observe que a ovulação pode ocorrer dentro de 10 dias após uma ou aborto espontâneo.
No caso de um aborto induzido ou espontâneo ocorrido na 20ª semana de gestação ou mais tarde, EVRA pode ser iniciado no dia 21 após o aborto, ou no primeiro dia da primeira menstruação espontânea, o que ocorrer primeiro. Conhece a incidência de ovulação em dia 21 após o aborto (na 20ª semana de gestação).
Depois de dar à luz
As usuárias que optam por não amamentar devem iniciar a terapia anticoncepcional com EVRA antes de 4 semanas após o parto. Posteriormente, informe a usuária da necessidade de usar um método de barreira adicional nos primeiros 7 dias. No entanto, se já tiver ocorrido relação sexual, descarte a possibilidade de gravidez antes de iniciar EVRA ou aguarde o primeiro período.
Para mulheres que amamentam, ver seção 4.6.
O que fazer se o adesivo transdérmico se soltar parcial ou totalmente
Se o adesivo transdérmico EVRA se desprender parcial ou totalmente e permanecer destacado, a quantidade de medicamento administrada não será suficiente.
Se EVRA permanecer, mesmo que apenas parcialmente destacado:
• por menos de um dia (até 24 horas): deve ser aplicado novamente no mesmo local ou substituído imediatamente por um novo adesivo transdérmico EVRA. Nenhuma outra medida anticoncepcional é necessária. Aplique o próximo adesivo transdérmico EVRA no seu "dia de mudança" habitual.
• por mais de um dia (24 horas ou mais) ou se a usuária não souber quando o adesivo transdérmico se levantou ou se soltou: a usuária pode não estar protegida contra a gravidez. A usuária deve interromper o ciclo anticoncepcional e iniciar um novo imediatamente, aplicando um novo adesivo transdérmico EVRA. Agora há um novo "dia 1" e um novo "dia de troca". Um método anticoncepcional não hormonal também deve ser usado simultaneamente , apenas durante os primeiros 7 dias do novo ciclo.
Um adesivo transdérmico não deve ser reaplicado se não for mais adesivo, substitua-o imediatamente por um novo. Nenhum outro adesivo ou curativo deve ser usado para segurar o adesivo transdérmico EVRA no lugar.
Em caso de atrasos nos dias subsequentes de substituição dos adesivos transdérmicos EVRA
No início de qualquer ciclo de adesivo transdérmico (primeira semana / dia 1):
A usuária pode não estar protegida da gravidez. Ela deve aplicar o primeiro adesivo transdérmico do novo ciclo assim que se lembrar. Agora há um novo "Dia de mudança" e um novo "Dia 1". Hormonal para os primeiros 7 dias de o novo ciclo No caso de relações sexuais durante um período tão prolongado sem adesivo transdérmico, deve ser considerada a possibilidade de gravidez.
Meio do ciclo (segunda semana / dia 8 ou terceira semana / dia 15):
• por um ou dois dias (até 48 horas): O usuário deve aplicar um novo adesivo transdérmico EVRA imediatamente. O próximo adesivo transdérmico EVRA deve ser aplicado no "dia de troca" usual. Se durante os 7 dias anteriores ao primeiro dia, se o adesivo transdérmico não foi aplicado, a usuária usou o adesivo corretamente, nenhuma outra medida anticoncepcional é necessária.
• por mais de dois dias (48 horas ou mais): A "usuária pode não estar protegida da gravidez. Ela deve interromper seu ciclo anticoncepcional atual e iniciar imediatamente um novo ciclo de quatro semanas, aplicando um novo adesivo transdérmico EVRA. Agora você fará tenha um novo "dia 1" e um novo "dia de reposição". Um contraceptivo não hormonal deve ser usado simultaneamente durante os primeiros 7 dias consecutivos do novo ciclo.
• no final do ciclo (semana 4 / dia 22): Se a usuária não remover o adesivo transdérmico EVRA no início da semana 4 (dia 22), ela deve removê-lo o mais rápido possível. O próximo ciclo deve começar com o "dia de reposição" normal, que é um dia após o 28º dia. Não são necessárias medidas anticoncepcionais adicionais.
Para alterar o dia de substituição
Se a usuária desejar adiar a menstruação uma vez, ela deve aplicar outro adesivo transdérmico no início da semana 4 (dia 22), não observando o intervalo sem adesivo. Você pode ter sangramento ou manchas. Após usar o adesivo transdérmico por 6 semanas consecutivas, deve haver um intervalo sem adesivo de 7 dias, após o qual a aplicação regular de EVRA é reiniciada.
Se a usuária desejar mudar o dia de troca, ela deve terminar o ciclo atual removendo o terceiro adesivo transdérmico EVRA no dia correto. Durante o intervalo sem um adesivo transdérmico, ela pode escolher um novo dia de mudança aplicando o primeiro adesivo transdérmico EVRA .do ciclo seguinte assim que chegar o dia pretendido. Nunca mais de 7 dias devem ficar sem o adesivo transdérmico. Quanto mais curto for o intervalo sem adesivo, maior o risco de o usuário não ter sangramento de privação e, em vez disso, ter metrorragia e manchas durante o próximo ciclo de tratamento.
Em caso de irritação leve da pele
Se o uso do adesivo transdérmico causar uma "irritação persistente, um novo adesivo transdérmico pode ser aplicado em outra parte" até o dia seguinte de substituição. Apenas um adesivo transdérmico deve ser usado por vez.
04.3 Contra-indicações
Contraceptivos hormonais combinados (anticoncepcionais hormonais combinados, COC) não deve ser usado nas seguintes condições. Se algum desses sintomas ocorrer durante o uso de EVRA, interrompa o uso imediatamente.
• Presença ou risco de tromboembolismo venoso (TEV)
• Tromboembolismo venoso - atual (com ingestão de anticoagulante) ou TEV anterior (por exemplo, trombose venosa profunda [TVP] ou embolia pulmonar [PE])
• Predisposição hereditária ou adquirida conhecida ao tromboembolismo venoso, como resistência à proteína C ativada (incluindo fator V de Leiden), deficiência de antitrombina III, deficiência de proteína C, deficiência de proteína S
• Cirurgia de grande porte com imobilização prolongada (ver seção 4.4)
• Alto risco de tromboembolismo venoso devido à presença de múltiplos fatores de risco (ver seção 4.4)
• Presença ou risco de tromboembolismo arterial (ATE)
• Tromboembolismo arterial - tromboembolismo arterial atual ou anterior (por exemplo, infarto do miocárdio) ou condições prodrômicas (por exemplo, angina de peito)
• Doença cerebrovascular - AVC atual ou anterior ou condições prodrômicas (por exemplo, ataque isquêmico transitório (ataque isquêmico transitório, TIA))
• Predisposição hereditária ou adquirida conhecida ao tromboembolismo arterial, como hiperhomocisteinemia e anticorpos antifosfolipídeos (anticorpos anticardiolipina, anticoagulante lúpico)
• História de enxaqueca com sintomas neurológicos focais
• Um alto risco de tromboembolismo arterial devido à presença de múltiplos fatores de risco (ver seção 4.4) ou a presença de um fator de risco grave, como:
• diabetes mellitus com sintomas vasculares
• hipertensão grave
• dislipoproteinemia grave
• Hipersensibilidade às substâncias ativas ou a qualquer um dos excipientes listados na secção 6.1.
• Câncer de mama conhecido ou suspeito
• Câncer endometrial ou outras neoplasias dependentes de estrogênio conhecidas ou suspeitas
• Função hepática alterada relacionada à doença hepatocelular aguda ou crônica
• Adenomas ou carcinomas hepáticos
• Sangramento genital anormal não diagnosticado
04.4 Advertências especiais e precauções adequadas de uso
Avisos
Se alguma das condições ou fatores de risco mencionados abaixo estiverem presentes, a adequação de EVRA deve ser discutida com a mulher.
Em caso de agravamento ou aparecimento inicial de qualquer um destes fatores ou condições de risco, a mulher deve contactar o seu médico para determinar se o uso de EVRA deve ser descontinuado.
Não há evidências clínicas que indiquem que um adesivo transdérmico seja mais seguro do que os COCs em qualquer aspecto.
EVRA não está indicado na gravidez (ver secção 4.6).
Risco de tromboembolismo venoso (TEV)
O uso de qualquer contraceptivo hormonal combinado (COC) resulta em um risco aumentado de tromboembolismo venoso (TEV) em comparação com o não uso. Produtos que contêm levonorgestrel, norgestimato ou noretisterona estão associados a um risco menor de TEV. O risco associado a outros. Produtos como EVRA também pode ser duplo. A decisão de usar um produto diferente daqueles associados a um menor risco de TEV só deve ser tomada após discussão com a mulher para garantir que ela compreende o risco de TEV associado a EVRA, a forma como você os fatores de risco atuais influenciam esse risco e o fato de que o risco de desenvolver um TEV é maior no primeiro ano de uso. Também há alguma evidência de que o risco aumenta quando se retoma um COC após um intervalo de 4 ou mais semanas.
Cerca de 2 em cada 10.000 mulheres que não usam um CHC e que não estão grávidas desenvolverão um TEV durante o período de um ano. Em uma mulher solteira, entretanto, o risco pode ser muito maior, dependendo de seus fatores de risco subjacentes (veja abaixo).
Estima-se que em cada 10.000 mulheres que usam uma dose baixa de CHC contendo levonorgestrel, cerca de 6 [1] desenvolverão um TEV em um ano. Estudos sugeriram que a incidência de TEV em mulheres que usaram EVRA é até duas vezes maior do que em usuárias de COCs que contêm levonorgestrel.Estes valores são de aproximadamente 6-12 TEV por ano para 10.000 mulheres usando EVRA.
[1] Valor médio da faixa de 5-7 por 10.000 mulheres / ano, com base em um risco relativo de aproximadamente 2,3-3,6 de COCs contendo levonorgestrel em comparação com o não uso
Em ambos os casos, o número de TEVs por ano é menor do que o esperado em mulheres grávidas ou puérperas.
O TEV pode ser fatal em 1-2% dos casos.
Muito raramente, trombose foi relatada em usuários de CHC em outros vasos sanguíneos, por exemplo, veias e artérias hepáticas, mesentéricas, renais ou retinais.
Fatores de risco para TEV
O risco de complicações tromboembólicas venosas em usuários de CHC pode aumentar substancialmente se fatores de risco adicionais estiverem presentes, especialmente se houver mais de um fator de risco (ver tabela).
EVRA está contra-indicado se a mulher tiver múltiplos fatores de risco que aumentam o risco de trombose venosa (ver secção 4.3). Se uma mulher tem mais de um fator de risco, é possível que o risco aumentado seja maior do que a soma dos fatores individuais; neste caso, seu risco total de TEV deve ser considerado. Se a relação risco-benefício for considerada negativa , um COC não deve ser prescrito (ver seção 4.3).
Tabela: Fatores de risco para TEV
Não há acordo sobre o possível papel das veias varicosas e da tromboflebite superficial no aparecimento e progressão da trombose venosa.
O risco aumentado de tromboembolismo na gravidez, particularmente no período de 6 semanas do puerpério, deve ser considerado (para informações sobre “Gravidez e aleitamento” ver secção 4.6.
Sintomas de TEV (trombose venosa profunda e embolia pulmonar)
Se ocorrerem sintomas desse tipo, as mulheres devem procurar atendimento médico imediato e informá-las de que estão tomando um CHC.
Os sintomas de trombose venosa profunda (TVP) podem incluir:
• inchaço unilateral da perna e / ou pé ou ao longo de uma veia da perna;
• dor ou sensibilidade na perna que só pode ser sentida ao ficar em pé ou ao caminhar;
• aumento da sensação de calor na perna afetada; pele da perna vermelha ou descolorida.
Os sintomas de embolia pulmonar (EP) podem incluir:
• início súbito e inexplicável de falta de ar e respiração rápida;
• tosse súbita que pode estar associada a hemoptise;
• dor aguda no peito;
• tonturas ou tonturas graves;
• batimento cardíaco rápido ou irregular.
Alguns desses sintomas (como "falta de ar" e "tosse") são inespecíficos e podem ser mal interpretados como eventos mais comuns ou menos graves (por exemplo, infecções do trato respiratório).
Outros sinais de oclusão vascular podem incluir: dor súbita, inchaço ou descoloração azul-clara de uma das extremidades.
Se a oclusão ocorrer no olho, os sintomas podem variar de visão turva indolor à perda de visão. Às vezes, a perda de visão ocorre quase imediatamente.
Risco de tromboembolismo arterial (ATE)
Os estudos epidemiológicos associaram a utilização de CHCs a um risco aumentado de tromboembolismo arterial (enfarte do miocárdio) ou de acidentes cerebrovasculares (por exemplo, ataque isquémico transitório, AVC). Os acontecimentos tromboembólicos arteriais podem ser fatais.
Fatores de risco de ATE
O risco de complicações tromboembólicas arteriais ou acidente vascular cerebral em usuárias de CHC aumenta na presença de fatores de risco (ver tabela). EVRA está contra-indicado se a mulher tiver um fator de risco grave ou múltiplos fatores de risco para ATE que aumentem o risco de trombose arterial (ver secção 4.3). Se uma mulher tem mais de um fator de risco, é possível que o aumento do risco seja maior do que a soma dos fatores individuais; neste caso, seu risco total deve ser considerado. Se a relação risco-benefício for considerada negativa, um CHC não deve ser prescrito (ver seção 4.3).
Tabela: Fatores de risco de ATE
Sintomas de ATE
Se ocorrerem sintomas deste tipo, as mulheres devem contactar um profissional de saúde imediatamente e informá-los de que estão a tomar um CHC.
Os sintomas de um acidente vascular cerebral podem incluir:
• dormência ou fraqueza repentina da face, braço ou perna, especialmente em um lado do corpo;
• dificuldade repentina para andar, tonturas, perda de equilíbrio ou coordenação;
• confusão repentina, dificuldade em falar ou compreender;
• dificuldade repentina de ver em um ou ambos os olhos;
• enxaqueca súbita, grave ou prolongada sem causa conhecida;
• perda de consciência ou desmaio com ou sem convulsões.
Os sintomas temporários sugerem que é um ataque isquêmico transitório (AIT).
Os sintomas de infarto do miocárdio podem incluir:
• dor, desconforto, pressão, peso, sensação de aperto ou plenitude no peito, braço ou abaixo do esterno;
• desconforto irradiando para as costas, mandíbula, garganta, braços, estômago;
• sensação de plenitude, indigestão ou sufocamento;
• suores, náuseas, vômitos ou tonturas;
• fraqueza extrema, ansiedade ou falta de ar;
• batimentos cardíacos rápidos ou irregulares.
Mulheres que usam anticoncepcionais combinados devem consultar o médico em caso de possíveis sintomas de trombose.Se houver suspeita de trombose ou se houver suspeita de trombose, interrompa o uso do anticoncepcional hormonal. Inicie a contracepção adequada devido à teratogenicidade da terapia anticoagulante (cumarinas).
Tumores
Um risco aumentado de câncer cervical em usuárias de AOC de longo prazo foi relatado em alguns estudos epidemiológicos, mas o grau em que esse achado pode ser atribuído ao efeito de confusão do comportamento sexual e outros fatores, como o papilomavírus humano, continua a ser controverso (HPV )
Uma meta-análise de 54 estudos epidemiológicos relatou um risco ligeiramente maior (RR = 1,24) de diagnóstico de câncer de mama entre mulheres que atualmente usam COCs. O risco excessivo desaparece gradualmente ao longo dos 10 anos após a interrupção do uso de COC. Como o câncer de mama é raro em mulheres com menos de 40 anos, o maior número de diagnósticos de câncer de mama entre as usuárias atuais e COCs recentes é limitado em relação ao risco geral de câncer de mama. O câncer de mama diagnosticado em mulheres que usaram COC tende a ser menos avançado clinicamente do que os cânceres encontrados em mulheres que nunca tomaram COC: o padrão de risco mais alto observado pode ser devido a um diagnóstico precoce de câncer de mama em usuárias de COC, os efeitos biológicos de COCs, ou uma combinação de ambos.
Em raras circunstâncias, tumores hepáticos benignos e, em circunstâncias ainda mais raras, tumores hepáticos malignos foram relatados entre usuários de COC. Em casos isolados, esses tumores causaram hemorragias intra-abdominais com risco de vida. Portanto, considere a possibilidade de câncer de fígado no diagnóstico diferencial quando um usuário de EVRA apresentar forte dor abdominal superior, aumento do fígado ou sinais de hemorragia intra-abdominal.
Outras condições
• A eficácia contraceptiva pode ser reduzida em mulheres com peso igual ou superior a 90 kg (ver secções 4.2 e 5.1).
• Mulheres com hipertrigliceridemia, ou histórico familiar, podem apresentar risco aumentado de pancreatite durante o uso de anticoncepcionais hormonais combinados.
• Embora pequenos aumentos na pressão arterial tenham sido relatados em muitas mulheres que tomam anticoncepcionais hormonais, aumentos clinicamente significativos são raros. Não foi estabelecida uma relação definitiva entre o uso de contraceptivos hormonais e hipertensão clínica. Se, durante o uso de um contraceptivo hormonal combinado na presença de hipertensão pré-existente, a pressão arterial alta ou um aumento significativo da pressão arterial não responder adequadamente ao tratamento anti-hipertensivo, interrompa o uso do contraceptivo hormonal combinado. Esse uso pode ser retomado se for possível obter valores normotensos por meio da terapia anti-hipertensiva.
• O aparecimento, ou deterioração, das seguintes condições foi relatado com a gravidez e o uso de COC. No entanto, a evidência de uma associação com o uso de COC não é conclusiva: icterícia e / o prurido associado a colestase; doença da vesícula biliar incluindo colecistite e colelitíase; porfiria; lúpus eritematoso sistêmico; síndrome hemolítico-urêmica; coreia de Sydenham; herpes gestacional; perda auditiva associada à otosclerose.
• Os distúrbios agudos ou crônicos da função hepática podem exigir a interrupção dos anticoncepcionais hormonais combinados até que os marcadores da função hepática voltem aos valores normais. Exigir a descontinuação dos anticoncepcionais hormonais combinados.
• Embora os anticoncepcionais hormonais combinados possam ter um efeito na resistência periférica à insulina e na tolerância à glicose, não há evidências de que o regime de tratamento precise ser alterado em pacientes diabéticos durante o uso de anticoncepcionais hormonais combinados. No entanto, as mulheres diabéticas devem ser vigiadas cuidadosamente, especialmente nas fases iniciais de utilização de EVRA.
• O agravamento da depressão endógena, epilepsia, doença de Crohn e colite ulcerosa foi relatado durante o uso de COC.
• O cloasma pode surgir ocasionalmente com o uso de contracepção hormonal, especialmente em usuárias com histórico de cloasma gravídico. As usuárias com tendência ao cloasma devem evitar a exposição ao sol ou à radiação ultravioleta durante o uso de EVRA. Freqüentemente, o cloasma não é completamente reversível.
Exames médicos / visitas
Antes de iniciar ou retomar o uso de EVRA, uma história médica completa (incluindo história familiar) deve ser obtida e a gravidez deve ser excluída. A pressão arterial deve ser medida e um exame clínico, guiado por contra-indicações, deve ser realizado (ver seção 4.3) e advertências (ver seção 4.4) .É importante chamar a atenção da mulher para informações relacionadas à trombose venosa ou arterial, incluindo o risco associado a EVRA em comparação com outros CHCs, sintomas de TEV e ATE, fatores de risco conhecidos e o que fazer em caso de suspeita de trombose.
A mulher também deve ser avisada sobre a necessidade de ler atentamente o folheto informativo e de seguir os seus conselhos. A frequência e o tipo de exames devem ser baseados em diretrizes estabelecidas e devem ser adaptados a cada mulher.
As mulheres devem ser avisadas de que os anticoncepcionais orais não protegem contra infecções por HIV (AIDS) e outras doenças sexualmente transmissíveis.
Sangramento irregular
Tal como acontece com todos os contraceptivos hormonais combinados, pode ocorrer perda de sangue irregular (manchas ou sangramento), particularmente nos primeiros meses de uso. Por este motivo, uma opinião médica sobre a perda de sangue irregular só será útil após um período de ajuste de aproximadamente três ciclos. Se a hemorragia persistir ou ocorrer após ciclos regulares anteriores, quando EVRA foi utilizado no regime recomendado., Uma causa diferente EVRA deve ser considerado. Considere causas não hormonais e, se necessário, tome medidas de diagnóstico adequadas para descartar a presença de doença orgânica ou gravidez. Essas medidas podem incluir curetagem. Em algumas mulheres pode não haver sangramento da suspensão no intervalo de uso do adesivo transdérmico. Se EVRA foi administrado de acordo com as instruções da secção 4.2, é improvável que a mulher esteja grávida. No entanto, se EVRA não foi administrado de acordo com estas instruções antes do primeiro sangramento de privação ignorado, ou se a mulher não teve dois sangramentos de privação consecutivos, a gravidez deve ser descartada antes de continuar a usar EVRA.
Algumas usuárias podem ter amenorreia ou oligomenorreia após interromper a contracepção hormonal, principalmente se essas condições já existissem.
04.5 Interações com outros medicamentos e outras formas de interação
Observação: Consulte as informações de prescrição de medicamentos concomitantes para identificar possíveis interações.
Influência de outros medicamentos em EVRA
As interações entre os anticoncepcionais orais e outros medicamentos podem levar à perda de sangue e / ou falha da proteção anticoncepcional. As seguintes interações foram relatadas na literatura.
Metabolismo hepático
Podem ser observadas interações com medicamentos indutores de enzimas hepáticas, que podem levar ao aumento da depuração de hormônios sexuais (por exemplo, fenobarbital, primidona, rifampicina, rifabutina, bosentano, (fos) aprepitante), alguns antiepilépticos (por exemplo, carbamazepina), acetato de eslicarbazepina, felbamato, oxicarbazepina, fenitoína, rufinamida, topiramato) e alguns medicamentos para o tratamento do HIV (por exemplo, nelfinavir, ritonavir, nevirapina, efavirenz) e possivelmente também griseofulvina e produtos contendo erva de São João (Hypericum perforatum) A indução enzimática máxima geralmente ocorre em cerca de 10 dias, mas pode ser mantida por pelo menos 4 semanas após a descontinuação da terapia.
Não use preparações à base de ervas que contenham erva de São João (Hypericum perforatum) ao usar EVRA.
Interferência com o círculo enterohepático
Também foram relatados casos de falha contraceptiva com antibióticos, como penicilinas e tetraciclinas. O mecanismo desse efeito ainda não está claro. Num estudo de interação farmacocinética, a administração oral de cloridrato de tetraciclina, 500 mg quatro vezes / dia durante 3 dias antes do período de aplicação de EVRA e durante 7 dias durante esse período, não afetou significativamente a farmacocinética da norelgestromina ou do etinilestradiol.
Gestão
Mulheres em tratamento de curto prazo com qualquer um dos medicamentos pertencentes a uma das classes acima ou com substâncias ativas que induzem enzimas hepáticas (exceto rifampicina), devem usar temporariamente um método de barreira além de EVRA, ou seja, durante o período de uso concomitante desses medicamentos e por 7 dias após sua interrupção. Para mulheres em tratamento com rifampicina, um método de barreira deve ser usado além de EVRA em conjunto com o período de rifampicina e por 28 dias após sua interrupção.
Para mulheres em terapia de longo prazo com qualquer um dos medicamentos pertencentes a uma das classes acima, é recomendado o uso de outro método de contracepção não hormonal eficaz.
Mulheres em tratamento com antibióticos (exceto rifampicina, veja acima) precisarão usar o método de barreira por até 7 dias após a interrupção do medicamento.
Se a medicação concomitante continuar após o final da semana de tratamento do adesivo, o novo adesivo deve ser aplicado imediatamente, iniciando um novo curso de tratamento, sem observar o intervalo normal sem adesivo.
Inibição do metabolismo do etinilestradiol
O etoricoxib demonstrou aumentar os níveis plasmáticos de etinilestradiol (50 a 60%) quando tomado concomitantemente com um contraceptivo hormonal oral trifásico. Pensa-se que o etoricoxib aumenta os níveis de etinilestradiol ao inibir a atividade da sulfotransferase, inibindo assim o metabolismo do etinilestradiol.
Influência de EVRA em outros medicamentos
Os anticoncepcionais hormonais podem afetar o metabolismo de alguns ingredientes ativos. Consequentemente, as concentrações plasmáticas e teciduais podem aumentar (por exemplo, ciclosporina). Pode ser necessário ajustar a dose do medicamento concomitante.
Lamotrigina: os contraceptivos hormonais combinados demonstraram uma diminuição significativa nas concentrações plasmáticas de lamotrigina quando coadministrada, possivelmente devido à indução da glucuronidação da lamotrigina.Isto pode reduzir o controlo das crises; portanto, pode ser necessário um ajuste da dose de lamotrigina.
Teste de laboratório
O uso de hormônios esteróides contraceptivos pode influenciar os resultados de alguns testes laboratoriais, incluindo parâmetros bioquímicos relacionados à função hepática, tireoidiana, adrenal e renal, níveis plasmáticos de proteínas (transportadoras), como, por exemplo, os corticosteróides e lipídeos de globulina de ligação ao sangue / frações de lipoproteínas, parâmetros do metabolismo de carboidratos e parâmetros de coagulação e fibrinólise As variações geralmente permanecem dentro dos limites laboratoriais normais.
04.6 Gravidez e lactação
Gravidez
EVRA não é indicado durante a gravidez.
Estudos epidemiológicos indicam que não há maior risco de defeitos congênitos em crianças nascidas de mulheres que usaram COCs antes da gravidez. Além disso, os estudos mais recentes não indicaram um efeito teratogênico quando os AOCs são usados inadvertidamente durante os estágios iniciais da gravidez.
Os dados limitados disponíveis sobre os resultados de gravidezes expostas em mulheres tratadas com EVRA não permitem conclusões sobre a segurança do adesivo transdérmico durante a gravidez.
Os estudos em animais revelaram efeitos indesejáveis durante a gravidez e o aleitamento (ver secção 5.3) .Com base nestes dados em animais, não podem ser excluídos os efeitos indesejáveis devidos à ação hormonal dos compostos ativos. No entanto, a experiência geral com AOCs durante a gravidez não forneceu evidências de um efeito adverso real em humanos.
Se você engravidar enquanto toma EVRA, pare de usar EVRA imediatamente.
O risco aumentado de TEV durante o período pós-parto deve ser considerado ao reiniciar EVRA (ver secções 4.2 e 4.4).
Hora da alimentação
A amamentação pode ser influenciada pelos anticoncepcionais hormonais combinados, pois podem reduzir o volume e alterar a composição do leite materno, portanto, o uso de EVRA não é recomendado em mães que amamentam até que o bebê esteja totalmente desmamado.
Fertilidade
Nas mulheres, pode haver um atraso na concepção após a interrupção do EVRA.
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
EVRA não tem ou tem uma influência negligenciável sobre a capacidade de conduzir ou utilizar máquinas.
04.8 Efeitos indesejáveis
Resumo do perfil de segurança
As reações adversas notificadas com mais frequência em ensaios clínicos foram cefaleias, náuseas e desconforto mamário, ocorrendo em aproximadamente 21,0%, 16,6% e 15,9% das mulheres, respetivamente.
As reações adversas que podem ocorrer no início do tratamento, mas geralmente diminuem após os três primeiros ciclos, incluem sangramento, desconforto mamário e náuseas.
Descrição de algumas reações adversas
Um risco aumentado de eventos trombóticos e tromboembólicos arteriais e venosos, incluindo enfarte do miocárdio, acidente vascular cerebral, ataques isquémicos transitórios, trombose venosa e embolia pulmonar, foi observado em utilizadores de CHC e este risco é discutido com mais detalhe na secção 4.4.
Tabela com lista de reações adversas
A segurança foi avaliada em 3.322 mulheres sexualmente ativas que participaram de três ensaios clínicos de Fase III destinados a avaliar a eficácia contraceptiva. Essas pacientes receberam seis ou 13 ciclos de contracepção (EVRA ou um contraceptivo oral como comparador)., Tomaram pelo menos uma dose do estudo medicamento e dados de segurança fornecidos. A Tabela 1 abaixo reflete as reações adversas notificadas em ensaios clínicos e na experiência pós-comercialização. Convenção MedDRA sobre frequência: muito comum (≥ 1/10); comum (≥ 1/100 y
04.9 Overdose
Nenhum efeito colateral sério foi relatado após a ingestão acidental de grandes quantidades de anticoncepcionais orais. A sobredosagem pode causar náuseas e vômitos. Algumas mulheres podem ter sangramento vaginal. Se houver suspeita de sobredosagem, elimine todos os sistemas. De contracepção transdérmica e administração de tratamento sintomático.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
Grupo farmacoterapêutico: Hormônios sexuais e moduladores do sistema genital, progestogênios e estrogênios, associação fixa. Código ATC: G03AA13.
Mecanismo de ação
EVRA atua através do mecanismo de supressão da gonadotropina através da ação estrogênica e progestógena do etinilestradiol e da norelgestromina. O principal mecanismo de ação é a inibição da ovulação, mas também as alterações do muco cervical e do endométrio podem contribuir para a eficácia do produto.
Eficácia clínica e segurança
Índices de pérolas (ver tabela):
*: DSG 150 mcg + 20 mcg EE
**: 50 mcg LNG +30 mcg EE para os dias 1-6, 75 mcg LNG + 40 mcg EE para os dias 7-11, 125 mcg LNG + 30 mcg EE para os dias 12-21
Análises exploratórias foram realizadas para determinar se nos estudos de fase III (n = 3319) as características da população de idade, raça e peso poderiam estar associadas à gravidez. As análises não indicaram qualquer associação de idade e raça com a gravidez, mas, por peso, 5 das 15 gravidezes relatadas com EVRA ocorreram em mulheres com peso corporal igual ou superior a 90 kg no início do estudo, o que constituiu
Com o uso de AOC em doses mais altas (50 mcg de etinilestradiol), o risco de câncer de endométrio e ovário é reduzido.Resta saber se isso também se aplica a anticoncepcionais hormonais combinados de dose mais baixa.
05.2 Propriedades farmacocinéticas
Absorção
Após a aplicação de EVRA, os níveis séricos de norelgestromina e etinilestradiol atingem um patamar em aproximadamente 48 horas. curso estável de norelgestromina e EE durante uma semana de uso do adesivo transdérmico são aproximadamente 0,8 ng / mL e 50 pg / mL, respectivamente. Em estudos de dose múltipla, as concentrações séricas e AUC para norelgestromina e EE aumentaram. apenas ligeiramente ao longo do tempo, quando comparados à semana 1 do ciclo 1.
A absorção de norelgestromina e etinilestradiol após aplicação de EVRA foi estudada nas condições encontradas no ginásio (sauna, jacuzzi, passadeira e outros exercícios aeróbicos) e no banho de água fria. Os resultados indicam que para a norelgestromina não houve efeitos de tratamento significativos para CSS ou AUC em comparação com o uso normal. Para EE, observou-se um ligeiro aumento da esteira e outros exercícios aeróbicos, mas os valores de CSS após esses tratamentos permaneceram dentro da faixa de referência.Não houve efeito significativo da água fria sobre esses parâmetros.
Os resultados de um estudo com EVRA sobre o uso prolongado de um único adesivo transdérmico por 7 dias e 10 dias indicaram que o CSS alvo para norelgestromina e etinilestradiol foi mantido por um prolongamento de 3 dias de uso de EVRA. (10 dias) Estes resultados sugerem que a eficácia clínica deve ser mantida mesmo se o adesivo for esquecido por até 2 dias inteiros.
Distribuição
A norelgestromina e o norgestrel (um metabólito sérico da norelgestromina) são altamente ligados (> 97%) às proteínas séricas. A norelgestromina está ligada à albumina e não à SHBG, enquanto o norgestrel está principalmente ligada à SHBG, o que limita sua atividade biológica. O etinilestradiol liga-se fortemente à albumina sérica.
Biotransformação
A norelgestromina é metabolizada pelo fígado e seus metabólitos incluem norgestrel, que se liga extensivamente ao SHGB, e vários metabólitos hidroxilados e conjugados. O etinilestradiol também é metabolizado em vários produtos hidroxilados e seus conjugados com glucuronídeos e sulfatos.
Eliminação
Após a remoção do adesivo transdérmico, as meias-vidas de eliminação da norelgestromina e do etinilestradiol foram de aproximadamente 28 horas e 17 horas, respectivamente. Os metabólitos de norelgestromina e etinilestradiol são eliminados por via renal e nas fezes.
Contraceptivos transdérmicos versus anticoncepcionais orais
Os perfis farmacocinéticos dos contraceptivos hormonais transdérmicos e orais combinados são diferentes e deve-se ter cuidado ao fazer uma comparação direta entre os parâmetros farmacocinéticos dessas duas formulações.
Em um estudo comparando EVRA com um contraceptivo oral contendo norgestimato (precursor de norelgestromina) 250 mcg / etinilestradiol 35 mcg, os valores de Cmax foram 2 vezes maiores para norelgestromina e etinilestradiol em indivíduos que receberam o contraceptivo oral em comparação com EVRA, enquanto a exposição total (AUC e Css) foi comparável à dos indivíduos tratados com EVRA.
A variabilidade interindividual (% CV) nos parâmetros farmacocinéticos de EVRA foi superior à observada com contraceptivos orais.
Efeitos da idade, peso corporal e área de superfície corporal
Os efeitos da idade, peso corporal e área de superfície corporal na farmacocinética de norelgestromina e etinilestradiol foram avaliados em 230 mulheres saudáveis em nove estudos farmacocinéticos com aplicações únicas de EVRA por 7 dias. Aumentos na idade, peso e área de superfície corporal foram associados a leves diminuições nos valores de Css e AUC para norelgestromina e EE. No entanto, apenas uma pequena porcentagem (10-20%) da variabilidade geral na farmacocinética de norelgestromina e EE após a aplicação de EVRA pode estar associada a alguns ou todos os acima dos parâmetros demográficos.
05.3 Dados de segurança pré-clínica
Os dados não clínicos não revelam riscos especiais para o ser humano, segundo estudos convencionais de farmacologia de segurança, toxicidade de dose repetida, genotoxicidade e potencial carcinogênico. Em relação à toxicidade reprodutiva, a norelgestromina demonstrou toxicidade fetal em coelhos, porém a margem de segurança para esse efeito foi suficientemente alta. Não existem dados sobre a toxicidade reprodutiva da combinação de norelgestromina com etinilestradiol. Os dados para a combinação de norgestimato (o precursor da norelgestromina) com etinilestradiol indicam uma redução da fertilidade e eficácia em animais fêmeas. Implantação (ratos), um aumento na reabsorção fetal (ratos, coelhos) e, em altas doses, uma diminuição na viabilidade e fertilidade de partos femininos (ratos). A relevância destes dados para a exposição humana é desconhecida, uma vez que os efeitos foram considerados relacionados com ações farmacodinâmicas ou ações específicas para estas espécies animais de natureza já conhecida.
Estudos conduzidos para examinar os efeitos dérmicos de EVRA indicam que este sistema não tem potencial para produzir sensibilização e pode causar irritação moderada quando aplicado à pele de coelho.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
Camada de reforço
camada externa de polietileno pigmentado de baixa densidade, camada interna de poliéster.
Camada intermediária
poliisobutileno / polibuteno adesivo, crospovidona, tecido não tecido de poliéster, lauril lactato.
Terceira camada
filme de tereftalato de polietileno (PET), revestimento de polidimetilsiloxano.
06.2 Incompatibilidade
Não é relevante.
06.3 Período de validade
2 anos.
06.4 Precauções especiais de armazenamento
Conservar na embalagem original para proteger os sistemas transdérmicos da luz e da humidade.
Não refrigerar ou congelar.
06.5 Natureza da embalagem primária e conteúdo da embalagem
Material de embalagem primária
Cada saqueta consiste em quatro camadas: um filme de polietileno de baixa densidade (a camada mais interna), uma folha de alumínio, um filme de polietileno de baixa densidade e uma camada externa de papel branqueado.
Material de embalagem secundário
Os saquinhos são acondicionados em caixa de papelão.
Cada embalagem contém 3, 9 ou 18 adesivos transdérmicos EVRA em saquetas reforçadas individuais.
Os sachês são acondicionados, em grupos de três, em filme plástico transparente perfurado e acondicionados em caixa de papelão.
Nem todos os tamanhos de embalagem podem ser comercializados.
06.6 Instruções de uso e manuseio
O sistema transdérmico deve ser aplicado imediatamente após a remoção da saqueta protetora.
Para evitar a interferência com as propriedades adesivas de EVRA, não devem ser aplicados cremes, loções ou talco na área da pele onde o adesivo transdérmico EVRA será aplicado.
Após o uso, o adesivo transdérmico ainda contém uma quantidade considerável de ingredientes ativos. Os ingredientes ativos hormonais residuais do adesivo transdérmico podem ter efeitos nocivos se atingirem o ambiente aquático.Portanto, o adesivo transdérmico usado deve ser descartado com cuidado. O rótulo a ser usado para exclusão. colocado do lado de fora da saqueta, deve ser levantado. O adesivo transdérmico usado deve ser colocado dentro da etiqueta de descarte aberta de forma que a superfície adesiva cubra a área sombreada do sachê. O rótulo deve então ser fechado lacrando o adesivo transdérmico usado dentro. Os medicamentos não usados e os resíduos derivados desses medicamentos devem ser eliminados de acordo com os regulamentos locais. Os adesivos transdérmicos usados não devem ser eliminados na casa de banho ou na eliminação de resíduos por meio de líquidos.
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
JANSSEN-CILAG INTERNATIONAL N.V.
Turnhoutseweg, 30
B-2340 Beerse
Bélgica
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
EU / 1/02/223/001
035684012
EU / 1/02/223/002
035684024
EU / 1/02/223/003
035684036
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
Data da primeira autorização: 22 de agosto de 2002
Data da última renovação: 22 de agosto de 2012
10.0 DATA DE REVISÃO DO TEXTO
01/2014












.jpg)