Ingredientes ativos: Nistatina
MYCOSTATIN 100.000 UI / ml suspensão oral
Por que a Micostatina é usada? Para que serve?
Grupo Farmacoterapêutico
Anti-infecciosos intestinais. Antibióticos.
Indicações terapêuticas
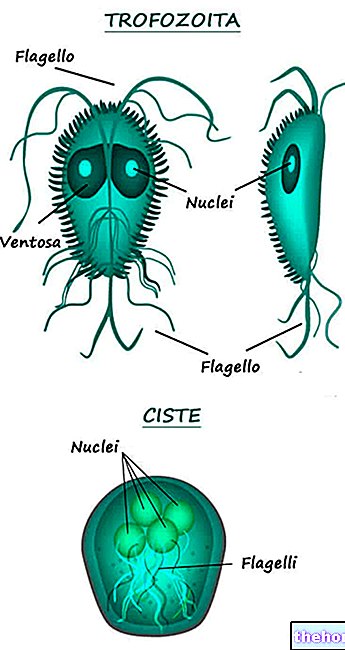
A Suspensão Oral de MYCOSTATIN (pronta para uso) é indicada na prevenção e tratamento de infecções por candidíase (monilíase) da cavidade oral, exógena e do trato intestinal. Também realiza uma profilaxia eficaz contra a candidíase oral (aftas) de recém-nascidos, especialmente naqueles cujas mães tiveram culturas positivas da secreção vaginal.
Contra-indicações Quando a micostatina não deve ser usada
Hipersensibilidade à substância ativa ou a qualquer um dos excipientes.
Precauções de uso O que você precisa saber antes de tomar Micostatina
A MICOSTATINA não deve ser usada no tratamento de micoses sistêmicas, pois sua atividade é essencialmente local. Em caso de irritação ou alergia, recomenda-se interromper o tratamento.
O uso de métodos diagnósticos é recomendado para confirmar o diagnóstico de candidíase e descartar infecções causadas por outros patógenos.
Informação para o paciente
- Os pacientes que recebem MYCOSTATIN devem seguir estritamente a prescrição do médico.
- Se os sintomas melhorarem durante os primeiros dias de tratamento, o paciente não deve interromper ou suspender o tratamento até que a terapia seja concluída.
- Se ocorrer irritação, o paciente deve notificar o médico assistente imediatamente.
- Ao prescrever MYCOSTATIN, alertar o paciente sobre a importância de uma boa higiene bucal, mesmo no caso de próteses e dentaduras.
Interações Quais medicamentos ou alimentos podem modificar o efeito da micostatina
Informe o seu médico ou farmacêutico se tiver tomado recentemente quaisquer outros medicamentos, mesmo sem receita.
Nenhum conhecido.
Avisos É importante saber que:
Para quem pratica atividades esportivas, o uso de medicamentos contendo álcool etílico pode determinar testes antidoping positivos em relação aos limites de concentração de álcool indicados por algumas federações esportivas.
Gravidez e Amamentação
Consulte o seu médico ou farmacêutico antes de tomar qualquer medicamento.
Não foram realizados estudos de reprodução animal com nistatina. Não foi estabelecido se a nistatina pode causar danos fetais quando administrada durante a gravidez ou se diminui a capacidade reprodutiva. A nistatina só deve ser administrada durante a gravidez se o benefício potencial para a mãe superar o risco potencial para o feto.
Não foi estabelecido se a nistatina é excretada no leite humano. Embora a absorção gastrointestinal seja insignificante, deve-se ter cuidado ao prescrever nistatina durante a lactação.
Informações importantes sobre alguns dos excipientes
O medicamento contém para-hidroxibenzoatos que podem causar reações alérgicas (incluindo retardadas) e, excepcionalmente, broncoespasmo.
Este medicamento contém pequenas quantidades de etanol (álcool), menos de 100 mg por dose.
MYCOSTATIN contém 500 mg de sacarose por ml, a ter em consideração em pessoas com diabetes mellitus.
Se foi informado pelo seu médico que tem intolerância a alguns açúcares, contacte-o antes de tomar este medicamento.
Dose, método e tempo de administração. Como usar micostatina: posologia
Bebês: a dose terapêutica usual é de 2 ml (1 ml de cada lado da boca), igual a 200.000 U.I., quatro vezes ao dia; se necessário, a dosagem também pode ser aumentada
Se administrado em combinação com um antibacteriano oral, é aconselhável prolongar a administração de MYCOSTATIN pelo menos tanto quanto a do antibacteriano.
Para a profilaxia do recém-nascido, a dosagem média recomendada é de 1 ml uma vez ao dia, instilada diretamente na boca com o conta-gotas.
Crianças e adultos: a dosagem terapêutica usual para candidíase oral é 4-6 ml (400.000-600.000 UI) quatro vezes ao dia; coloque metade da dose em cada lado da boca e mantenha-a nessa posição durante o maior tempo possível antes de engolir. Se necessário, a dosagem também pode ser aumentada.
Para prevenir recaídas, é aconselhável continuar o tratamento por pelo menos 48 horas após a recuperação clínica.
Se os sintomas piorarem ou persistirem (após 14 dias de tratamento), o paciente deve ser submetido a supervisão médica para uma prescrição de terapia alternativa.
AGITAR ANTES DE USAR.
Duração do tratamento
Conforme prescrição médica.
Sobredosagem O que fazer se você tiver tomado demasiada micostatina
Doses orais de nistatina maiores que 5 milhões de unidades por dia causaram náuseas e distúrbios gastrointestinais.
Em caso de ingestão acidental / ingestão de uma dose excessiva de MYCOSTATIN, avise o seu médico imediatamente ou dirija-se ao hospital mais próximo.
SE VOCÊ TIVER ALGUMA DÚVIDA SOBRE O USO DE MYCOSTATIN, CONTATE SEU MÉDICO OU FARMACÊUTICO.
Efeitos colaterais Quais são os efeitos colaterais da micostatina
Como todos os medicamentos, MYCOSTATIN pode causar efeitos colaterais, embora nem todas as pessoas os sintam.
A nistatina é geralmente bem tolerada por pacientes de todas as idades, incluindo bebês debilitados, mesmo com tratamento prolongado. Doses orais altas causaram diarreia, desconforto abdominal, náuseas e vômitos (veja Superdosagem).
Efeitos colaterais incomuns (podem afetar até 1 em 100 pessoas):
- Diarréia
- Desconforto abdominal
- Náusea
- Ele vomitou
- Irritação na pele
Efeitos colaterais raros (podem afetar até 1 em 1000 pessoas):
- Hipersensibilidade
- Angioedema, incluindo edema facial
- Síndrome de Stevens-Johnson
- Urticária
O cumprimento das instruções contidas no folheto informativo reduz o risco de efeitos indesejáveis.
Relatório de efeitos colaterais
Se tiver quaisquer efeitos secundários, fale com o seu médico ou farmacêutico, incluindo quaisquer efeitos secundários possíveis não mencionados neste folheto. Os efeitos colaterais também podem ser relatados diretamente através do sistema nacional de notificação em https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse Ao relatar os efeitos colaterais, você pode ajudar a fornecer mais informações sobre a segurança deste medicamento.
Expiração e retenção
Validade: veja a data de validade indicada na embalagem.
Atenção: não use o medicamento após expirar o prazo de validade indicado na embalagem.
O prazo de validade refere-se ao produto em embalagem intacta, corretamente armazenado.
Precauções especiais de conservação do medicamento: Conservar a uma temperatura não superior a 25 ° C.
Os medicamentos não devem ser eliminados na canalização ou no lixo doméstico. Pergunte ao seu farmacêutico como eliminar os medicamentos que já não utiliza. Isto ajudará a proteger o ambiente.
MANTENHA O MEDICAMENTO FORA DO ALCANCE E DA VISTA DAS CRIANÇAS
Composição
Um ml de suspensão oral contém:
ingrediente ativo: nistatina 100.000 I.U.
excipientes: sacarose, glicerol, sacarina sódica, carmelose sódica, fosfato dibásico de sódio, para-hidroxibenzoato de metila, para-hidroxibenzoato de propila, álcool etílico, aroma de cereja, óleo de hortelã-pimenta, cinamaldeído, água purificada.
Forma farmacêutica e conteúdo
Suspensão oral pronta a usar.Cada ml contém 100.000 I.U. de ingrediente ativo.
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
MYCOSTATIN 100.000 IU / ML
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Um ml de suspensão oral contém:
ingrediente ativo: nistatina 100.000 I.U.
Excipientes:
MYCOSTATIN contém 500 mg de sacarose por ml.
Para a lista completa de excipientes, consulte a seção 6.1.
03.0 FORMA FARMACÊUTICA
Suspensão oral.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
MYCOSTATIN suspensão oral é indicada na prevenção e tratamento de infecções por candidíase (monilíase) da cavidade oral, esôfago e trato intestinal. Também realiza uma profilaxia eficaz contra a candidíase oral (sapinho) de recém-nascidos, especialmente naqueles cujas mães tiveram culturas positivas de a secreção vaginal.
04.2 Posologia e método de administração
Bebês: a dosagem terapêutica usual é de 2 ml (1 ml de cada lado da boca) igual a 200.000 U.I., quatro vezes ao dia; se necessário, a dosagem também pode ser aumentada.
Se administrado em combinação com um antibiótico oral, é aconselhável prolongar a administração de MYCOSTATIN pelo menos o tempo do antibacteriano.
Para a profilaxia neonatal, a dosagem média recomendada é de 1 ml uma vez ao dia, instilada diretamente na boca com o conta-gotas.
Crianças e adultos: a dosagem terapêutica usual para candidíase oral é 4 - 6 ml (400.000 - 600.000 UI) quatro vezes ao dia; coloque metade da dose em cada lado da boca e mantenha-a nessa posição durante o maior tempo possível antes de engolir.
Se necessário, a dosagem também pode ser aumentada.
Para prevenir recaídas, é aconselhável continuar o tratamento por pelo menos 48 horas após a recuperação clínica.
Se os sintomas piorarem ou persistirem (após 14 dias de tratamento), o paciente deve ser submetido a supervisão médica para uma prescrição de terapia alternativa.
Agitar antes de usar.
04.3 Contra-indicações
Hipersensibilidade à substância ativa ou a qualquer um dos excipientes.
04.4 Advertências especiais e precauções adequadas de uso
A MICOSTATINA não deve ser usada no tratamento de micoses sistêmicas, pois sua atividade é essencialmente local. Em caso de irritação ou alergia, recomenda-se interromper o tratamento.
O uso de esfregaço de KOH (hidróxido de potássio), culturas ou outros métodos diagnósticos é recomendado para confirmar o diagnóstico de candidíase e para descartar infecções causadas por outros patógenos.
MYCOSTATIN contém sacarose, portanto, pacientes com diabetes mellitus, problemas hereditários raros de intolerância à frutose, má absorção de glicose-galactose ou insuficiência de sacarase isomaltase não devem tomar este medicamento.
Este medicamento contém pequenas quantidades de etanol (álcool), menos de 100 mg por dose.
O medicamento contém para-hidroxibenzoatos que podem causar reações alérgicas (incluindo retardadas) e, excepcionalmente, broncoespasmo.
Informação para o paciente
1. Os pacientes que recebem MYCOSTATIN devem seguir estritamente a prescrição do médico.
2. Se os sintomas melhorarem durante os primeiros dias de tratamento, o paciente não deve interromper ou suspender o tratamento até que a terapia seja concluída.
3. Se ocorrer irritação, o paciente deve notificar o médico assistente imediatamente.
4. Ao prescrever MYCOSTATIN, alertar o paciente sobre a importância de uma boa higiene bucal, mesmo no caso de próteses e dentaduras.
04.5 Interações com outros medicamentos e outras formas de interação
Nenhum conhecido.
04.6 Gravidez e lactação
Gravidez: Não foram realizados estudos de reprodução animal com nistatina. Não foi estabelecido se a nistatina pode causar danos fetais quando administrada durante a gravidez ou se diminui a capacidade reprodutiva. A nistatina só deve ser administrada durante a gravidez se o benefício potencial para a mãe superar o risco potencial para o feto.
Hora da alimentação: Não foi estabelecido se a nistatina é excretada no leite humano. Embora a absorção gastrointestinal seja insignificante, deve-se ter cuidado ao prescrever nistatina durante a lactação.
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
Ninguém.
04.8 Efeitos indesejáveis
A nistatina é geralmente bem tolerada por pacientes de todas as idades, incluindo bebês debilitados, mesmo com tratamento prolongado. Doses orais elevadas causaram diarreia, desconforto abdominal, náuseas e vómitos (ver secção 4.9).
A tabela abaixo lista as reações adversas notificadas por classes de sistemas de órgãos e frequência, utilizando as seguintes convenções: muito frequentes (≥1 / 10), frequentes (≥1 / 100,
REAÇÕES ADVERSAS RELATADAS DURANTE ESTUDOS CLÍNICOS
OU EXPERIÊNCIA PÓS-MARKETING
Notificação de suspeitas de reações adversas
A notificação de suspeitas de reações adversas que ocorram após a autorização do medicamento é importante, uma vez que permite a monitorização contínua da relação benefício / risco do medicamento.Os profissionais de saúde são solicitados a notificar quaisquer suspeitas de reações adversas por meio do sistema nacional de notificação em https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdose
Doses orais de nistatina maiores que 5 milhões de unidades por dia causaram náuseas e distúrbios gastrointestinais.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
Grupo farmacoterapêutico: anti-infecciosos intestinais, antibióticos.
Código ATC: A07AA02.
A nistatina é um antibiótico antifúngico, fungistático e fungicida in vitro contra uma ampla variedade de leveduras e fungos semelhantes a leveduras. Provavelmente atua ligando-se aos esteróis da membrana celular do fungo, alterando sua permeabilidade e permitindo o escape dos componentes intracelulares.
05.2 Propriedades farmacocinéticas
A nistatina é um antibiótico polieno de estrutura indeterminada, obtido do Streptomyces noursei: representa o primeiro antibiótico antifúngico bem tolerado e comprovado no tratamento de infecções cutâneas, orais e intestinais causadas por Candida (monilia) albicans e outras espécies de Candida. Não exerce qualquer atividade apreciável sobre bactérias, protozoários ou vírus.
Após a administração oral, a nistatina é muito pouco absorvida; nas doses recomendadas, não é possível determinar as taxas plasmáticas. A maior parte da dose administrada por via oral é excretada inalterada nas fezes.
05.3 Dados de segurança pré-clínica
Não foram realizados estudos de longo prazo em animais para avaliar o potencial carcinogênico da nistatina, nem para determinar a mutagenicidade da nistatina ou seus efeitos na fertilidade masculina ou feminina.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
Sacarose, glicerol, sacarina sódica, carmelose sódica, fosfato dibásico de sódio, para-hidroxibenzoato de metila, para-hidroxibenzoato de propila, álcool etílico, sabor de imitação de cereja, óleo de hortelã-pimenta, cinamaldeído, água purificada.
06.2 Incompatibilidade
Nenhum conhecido.
06.3 Período de validade
3 anos.
06.4 Precauções especiais de armazenamento
Armazenar a uma temperatura não superior a 25 ° C.
06.5 Natureza da embalagem primária e conteúdo da embalagem
Frasco de 100 ml em polietileno. Um conta-gotas calibrado para 1 ml é anexado a cada frasco.
06.6 Instruções de uso e manuseio
Nenhum.
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
BRISTOL-MYERS SQUIBB S.r.l. Via Virgilio Maroso, 50 - Roma
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
MYCOSTATIN 100.000 UI / ml suspensão oral: A.I.C. N ° 010058030
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
Maio de 2010.
10.0 DATA DE REVISÃO DO TEXTO
Março 2014