Ingredientes ativos: condroitina (sulfato de condroitina de sódio)
CONDRAL 400 mg cápsulas duras
CONDRAL 400mg granulado para solução oral
CONDRAL 800 mg granulado para solução oral
Por que o Condral é usado? Para que serve?
O que é CONDRAL
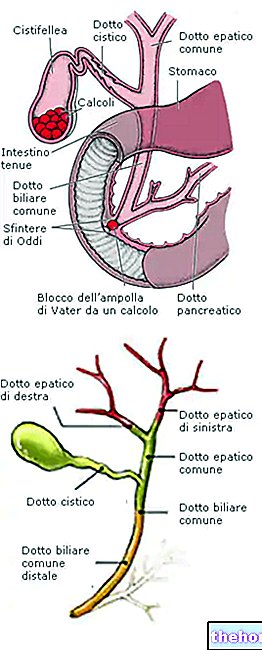
CONDRAL é um medicamento à base de sulfato de condroitina sódico que pertence à classe dos polissacarídeos. O sulfato de condroitina é um componente importante das cartilagens, os tecidos de suporte presentes nas articulações
Para que serve
CONDRAL é indicado em adultos para o tratamento dos sintomas da osteoartrose do joelho e da anca.
O que é osteoartrite?
A osteoartrite é uma doença muito comum, principalmente em adultos, causada por uma alteração do tecido cartilaginoso das articulações.
Os sintomas da osteoartrite são: dores nas articulações, rigidez após o repouso, capacidade reduzida de mover as articulações e, em alguns casos, deformação das articulações.
Contra-indicações Quando Condral não deve ser usado
Não tome CONDRAL:
- se tem alergia ao sulfato de condroitina de sódio ou a substâncias quimicamente semelhantes, ou a qualquer outro componente de CONDRAL (ver secção “Qual a composição de CONDRAL”).
Precauções de uso O que você precisa saber antes de tomar Condral
Fale com o seu médico antes de tomar CONDRAL
- se sofre de algum tipo de alergia.
Crianças e adolescentes
O uso de CONDRAL em crianças e adolescentes com menos de 18 anos não está indicado, uma vez que a segurança e eficácia não foram estabelecidas neste grupo de doentes.
Interações Quais drogas ou alimentos podem modificar o efeito de Condral
Informe o seu médico ou farmacêutico se estiver a tomar, tiver tomado recentemente ou se vier a tomar outros medicamentos, incluindo medicamentos obtidos sem receita médica. Até o momento, nenhuma interação com outros medicamentos é conhecida.
Avisos É importante saber que:
Se está grávida ou a amamentar, se pensa estar grávida ou planeia engravidar, consulte o seu médico ou farmacêutico antes de tomar este medicamento.
Se estiver grávida ou amamentando, use este medicamento apenas quando for absolutamente necessário e sob supervisão médica direta.
Condução e utilização de máquinas
CONDRAL não afeta a capacidade de conduzir e utilizar máquinas.
Grânulos CONDRAL contém:
- sorbitol: se foi informado pelo seu médico que tem "intolerância a alguns açúcares (por exemplo, sorbitol), contacte o seu médico antes de tomar este medicamento;
- amarelo-sol (E110): pode causar reações alérgicas;
- sódio: deve ser levado em consideração em pessoas com função renal reduzida ou que seguem uma dieta com baixo teor de sódio. Em particular, os grânulos de 400 mg contêm 1,65 mmol (38 mg) de sódio por dose, enquanto os grânulos de 800 mg contêm 3,30 mmol (76 mg) de sódio por dose.
As cápsulas CONDRAL contêm:
- sódio, 1,59 mmol (37 mg) por dose: deve ser tido em consideração em pessoas com função renal reduzida ou em dieta com baixo teor de sódio.
Dose, método e tempo de administração Como usar Condral: Posologia
Tome CONDRAL sempre de acordo com as indicações do médico. Em caso de dúvida, consulte o seu médico ou farmacêutico.
A dose recomendada, a menos que seja prescrita de outra forma, é:
- Cápsulas de 400 mg: 2 a 3 cápsulas por dia por via oral
- Saquetas de 400 mg: 2 a 3 saquetas por dia por via oral
- Sachês de 800 mg: uma saqueta por dia por via oral.
O conteúdo das saquetas deve ser dissolvido em água antes da ingestão.
A duração do tratamento não deve ser inferior a 3 semanas.
Overdose O que fazer se você tiver tomado Condral demais
Se você tomar mais CONDRAL do que deveria
Se tomar mais CONDRAL do que deveria, contacte o seu médico ou dirija-se ao hospital mais próximo.
Se você esquecer de levar CONDRAL
Não tome uma dose a dobrar para compensar uma dose esquecida.
Se você parar de tomar CONDRAL
Caso ainda tenha dúvidas sobre a utilização deste medicamento, fale com o seu médico ou farmacêutico.
Efeitos colaterais Quais são os efeitos colaterais do Condral
Como todos os medicamentos, CONDRAL pode causar efeitos secundários, embora nem todas as pessoas os tenham.
Reações como náusea, diarreia, dor, desconforto abdominal e reações cutâneas podem aparecer no início da terapia, mas geralmente são raras e de gravidade leve.
Os seguintes efeitos colaterais foram relatados durante o tratamento com CONDRAL, listados de acordo com a frequência:
Raros (podem afetar até 1 em 1000 pessoas):
- tontura
- dor na parte superior do abdômen
- diarréia
- náusea
- distúrbios estomacais e intestinais
- vermelhidão da pele (eritema)
- erupção cutânea incluindo manchas vermelhas e bolhas (erupção maculopapular e erupção na pele).
Muito raro (menos de 1 em 10.000 pessoas):
- vermelhidão da pele acompanhada de coceira (urticária)
- inflamação da pele acompanhada de coceira (eczema)
- coceira
- inchaço (edema).
Relatório de efeitos colaterais
Se tiver quaisquer efeitos secundários, fale com o seu médico, incluindo quaisquer efeitos secundários possíveis não mencionados neste folheto. Você também pode relatar efeitos colaterais diretamente por meio do sistema de notificação nacional em https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Ao relatar os efeitos colaterais, você pode ajudar a fornecer mais informações sobre a segurança deste medicamento.
Expiração e retenção
Cápsulas CONDRAL: Não conservar acima de 30 ° C.
Granulado CONDRAL: este medicamento não requer quaisquer condições especiais de conservação.
Não utilize este medicamento após o prazo de validade impresso na embalagem exterior. A data de validade refere-se ao último dia desse mês.
Não deite quaisquer medicamentos na canalização ou no lixo doméstico. Pergunte ao seu farmacêutico como deitar fora os medicamentos que já não utiliza. Isto ajudará a proteger o ambiente.
Mantenha este medicamento fora da vista e do alcance das crianças.
O que CONDRAL contém
CONDRAL cápsulas duras
- O ingrediente ativo é o sulfato de condroitina de sódio. Cada cápsula contém 400 mg de sulfato de condroitina de sódio.
- Os outros componentes são: estearato de magnésio, gelatina, dióxido de titânio (E171), índigo carmim (E132), amarelo de quinolina (E104).
Grânulos CONDRAL
- O ingrediente ativo é o sulfato de condroitina de sódio. Cada saqueta contém 400 mg ou 800 mg de sulfato de condroitina sódico.
- Os outros componentes são: ácido cítrico, sacarina sódica (ver seção "CONDRAL granulado contém sódio"), sabor de laranja, amarelo-sol (E 110) (ver seção "CONDRAL granulado contém amarelo sunset (E110)"), sorbitol (ver seção " O granulado CONDRAL contém sorbitol "), sílica coloidal anidra.
Qual a aparência de CONDRAL e conteúdo da embalagem
As cápsulas CONDRAL são azul esverdeadas, embaladas em blisters. Eles estão disponíveis em embalagens contendo 20 cápsulas.
CONDRAL granulado para solução oral de 400 mg é acondicionado em saquetas. Estão disponíveis em embalagens com 20 saquetas.
CONDRAL granulado para solução oral de 800 mg é acondicionado em saquetas. Estão disponíveis em embalagens com 20 saquetas.
Nem todos os tamanhos de embalagem podem ser comercializados.
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
CONDRAL
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Cada capsula contém
Princípio ativo:
400 mg de sulfato de condroitina de sódio
Cada saqueta de grânulos contém
Princípio ativo:
400 mg de sulfato de condroitina de sódio
Cada saqueta de grânulos contém
Princípio ativo:
800 mg de sulfato de condroitina de sódio
Para a lista completa de excipientes, consulte a seção 6.1.
03.0 FORMA FARMACÊUTICA
Cápsulas duras.
Granulado para solução oral.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
Tratamento sintomático da osteoartrose do joelho e quadril.
04.2 Posologia e método de administração
A menos que seja prescrito de outra forma, o seguinte esquema de dosagem é recomendado, a ser seguido por um período não inferior a 3 semanas:
Cápsulas e saquetas de 400 mg: de 2 a 3 cápsulas ou sachês via oral / dia, conforme a gravidade da doença;
saquetas de 800 mg: 1 saqueta por via oral / dia.
O conteúdo das saquetas deve ser dissolvido em água antes da ingestão.
Uso em crianças
Não há evidências que apóiem o uso de sulfato de condroitina em crianças de até 18 anos de idade. O uso de sulfato de condroitina em crianças, portanto, não é recomendado.
04.3 Contra-indicações
Hipersensibilidade à substância ativa ou a outras substâncias intimamente relacionadas do ponto de vista químico e / ou a qualquer um dos excipientes.
04.4 Advertências especiais e precauções adequadas de uso
O uso da preparação não é aconselhável em indivíduos particularmente propensos a alergias.
CONDRAL granulado para solução oral contém sorbitol. Pacientes com problemas hereditários raros de intolerância à frutose não devem receber este medicamento.
04.5 Interações com outros medicamentos e outras formas de interação
Não há interações conhecidas ou incompatibilidades com outros medicamentos.
Não foram realizados estudos de interação.
04.6 Gravidez e lactação
Em mulheres grávidas e lactantes, o produto deve ser administrado apenas em casos de real necessidade e sob a supervisão direta do médico.
Gravidez: Não há dados clínicos disponíveis sobre a exposição durante a gravidez para o produto.
Os estudos em animais não indicam efeitos prejudiciais diretos ou indiretos relacionados com a gravidez, o desenvolvimento embriofetal, o parto e o desenvolvimento pós-natal.
Prescreva o medicamento com cautela na gravidez.
Aleitamento: Não se sabe se o produto é excretado no leite humano nem se sua excreção no leite foi estudada em animais. A decisão de continuar ou interromper a amamentação ou de continuar ou descontinuar a terapia com CONDRAL deve ser tomada considerando o benefício do medicamento .a amamentação para o bebê e o benefício da terapia com o produto para a mãe.
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
CONDRAL não afeta a capacidade de conduzir ou utilizar máquinas.
04.8 Efeitos indesejáveis
As reações adversas são raras (náuseas, diarreia, dor, desconforto abdominal e reações cutâneas podem aparecer com o início da terapia, mas geralmente são raras e de gravidade leve.
As reações adversas observadas durante a vigilância pós-comercialização são apresentadas na tabela seguinte.
Em cada categoria, as reações adversas são classificadas de acordo com a frequência de início e gravidade, usando a seguinte convenção: muito frequentes (> 1/10); comum (> 1/100, 1 / 1.000, 1 / 10.000,
O termo MedDRA mais apropriado foi usado para descrever as reações listadas acima.Sinónimos ou condições relacionadas não estão listados, mas ainda devem ser considerados.
04.9 Overdose
Nenhum caso de sobredosagem foi relatado.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
Grupo farmacoterapêutico: outros medicamentos para doenças do sistema musculoesquelético. Código ATC: M09AX.
O ingrediente ativo sulfato de condroitina de CONDRAL pertence à classe dos polissacarídeos, mais precisamente dos glicosamino-glicanos. São um dos principais elementos constituintes da cartilagem, onde se encontram ligados às proteínas para formar os chamados proteoglicanos, que garantem as propriedades mecânico-elásticas da própria cartilagem. Nos processos degenerativos articulares do tipo artrítico, observa-se diminuição do conteúdo de sulfato de condroitina cartilaginoso com consequente redução do poder de fixação da água e consequente deterioração progressiva da função articular devido à degeneração da própria cartilagem.
O suprimento de sulfato de condroitina exógeno compensa o déficit de cartilagem, permitindo uma interrupção ou desaceleração do processo degenerativo e uma realização ideal dos processos reparadores espontâneos.
Ao nível da cartilagem articular, de facto, o sulfato de condroitina é capaz de antagonizar os processos degenerativos articulares, sobretudo através da inibição das enzimas líticas cartilaginosas e da estimulação da biossíntese de proteoglicanos.
No animal experimental os principais efeitos do princípio ativo foram a ação no reparo ósseo e a atividade antiartrítica.
05.2 "Propriedades farmacocinéticas
Do ponto de vista farmacocinético, após administração oral única no homem, destacaram-se as concentrações plasmáticas de sulfato de condroitina, avaliadas como atividade lipoproteína-lipase, já após 15 "da administração, com pico detectável em torno de 30" e persistindo por mais 12 horas após a administração administração.
05.3 Dados de segurança pré-clínica
Os dados não clínicos não revelam riscos especiais para o ser humano, segundo estudos convencionais de farmacologia de segurança, toxicidade de dose repetida, genotoxicidade, potencial carcinogênico, toxicidade reprodutiva.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
Cápsulas duras
Conteúdo da cápsula:
Estearato de magnesio
Concha da cápsula:
Geléia
Dióxido de titânio
E 132
E 104.
Grânulos para solução oral
Ácido Cítrico
Sacarina sódica
Aroma de laranja
E 110
Sorbitol
Sílica coloidal anidra (Aerosil 200).
06.2 Incompatibilidade
Não é relevante.
06.3 Período de validade
3 anos.
06.4 Precauções especiais de armazenamento
Cápsulas duras: armazenar a uma temperatura não superior a 30 ° C.
Grânulos para solução oral: sem condições particulares de armazenamento.
06.5 Natureza da embalagem primária e conteúdo da embalagem
Cápsulas duras: blister de alumínio - PVDC. Caixa de papelão contendo 20 cápsulas.
Granulado para solução oral: saquetas de papel-alumínio-polietileno seladas a quente. Caixa de cartão com 20 saquetas.
06.6 Instruções de uso e manuseio
Sem instruções especiais.
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
SPA - Antibiotic Products Company S.p.A. - Via Biella, 8 - 20143 Milão.
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
400 mg cápsulas 20 cápsulas AIC 026776017
Grânulos de 400 mg para solução oral 20 saquetas AIC 026776029
Grânulos de 800 mg para solução oral 20 saquetas AIC 026776031
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
20 cápsulas 400 mg 1/2/1990
20 sachês granulados 400 mg 1/2/1990
20 grânulos, sachês de 800 mg 29/10/1994
Última renovação: 1/6/2010.
10.0 DATA DE REVISÃO DO TEXTO
Janeiro de 2012.